
| A. | 该反应是氧化还原反应 | B. | Cu是氧化剂 | ||
| C. | CO是还原剂 | D. | 该反应中有电子转移 |
分析 该反应中C元素化合价由+2价变为+4价、Cu元素化合价由+2价变为0价,
A.有电子转移的化学反应是氧化还原反应;
B.失电子化合价升高的反应物是还原剂、得电子化合价降低的反应物是氧化剂;
C.失电子化合价升高的反应物是还原剂、得电子化合价降低的反应物是氧化剂;
D.有元素化合价变化的化学反应一定有电子转移.
解答 解:该反应中C元素化合价由+2价变为+4价、Cu元素化合价由+2价变为0价,
A.该反应中有元素化合价升降,所以有电子转移,则该反应是氧化还原反应,故A正确;
B.失电子化合价升高的反应物是还原剂、得电子化合价降低的反应物是氧化剂,Cu是氧化剂对应的产物,为还原产物,故B错误;
C.失电子化合价升高的反应物是还原剂、得电子化合价降低的反应物是氧化剂,CO失电子为还原剂,故C正确;
D.有元素化合价变化的化学反应一定有电子转移,该反应中有化合价升降,所以一定有电子转移,故D正确;
故选B.
点评 本题考查氧化还原反应,为高频考点,侧重考查基本概念和基本计算,明确元素化合价变化与基本概念之间关系是解本题关键,熟悉常见元素化合价.


 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:高中化学 来源: 题型:选择题
| A. | pH=3的HNO 3与pH=11的KOH溶液 | |
| B. | pH=3的HNO 3与pH=11的氨水 | |
| C. | pH=3的H 2SO 4与pH=11的NaOH溶液 | |
| D. | pH=3的CH 3COOH与pH=11的Ba(OH) 2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
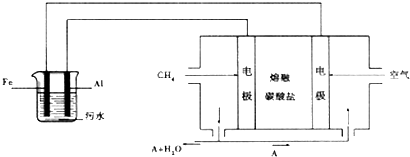
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2L的CH2Cl2所含的分子数为0.5NA | |
| B. | 28g乙烯所含共用电子对数目为4NA | |
| C. | 常温常压下,16gO2和O3的混合气体含有的氧原子数为NA | |
| D. | 1molCaC2所含阴离子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
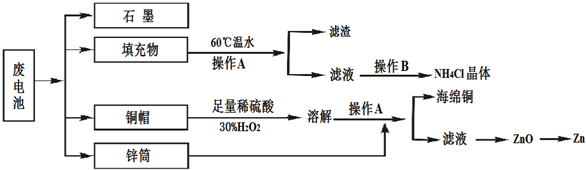
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 加压后,该反应平衡向左移 | B. | 加压后,c(I2)增大 | ||
| C. | 压强变化时,c(HI)不变 | D. | 加压后,颜色变浅 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com