
| A. | HClO的电子式 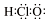 | B. | 丙烷分子的比例模型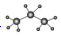 | ||
| C. | 对氯甲苯的结构简式 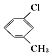 | D. | 乙醇的分子式C2H6O |
分析 A.HClO为共价化合物,分子中存在1个氧氢键和1个Cl-O键;
B.比例模型能够体现出原子体积的相对大小,题中为丙烷的球棍模型;
C.对氯甲苯中甲基和氯原子处于对位关系来分析;
D.是分子式是用元素符号表示纯净物(单质、化合物)分子的组成及相对分子质量的化学式,分子中同种元素的原子合并得到的式子.
解答 解:A.HClO为共价化合物,分子中存在1个氧氢键和1个Cl-O键,次氯酸的电子式为: ,故A错误;
,故A错误;
B. 为丙烷的球棍模型,丙烷的比例模型为:
为丙烷的球棍模型,丙烷的比例模型为: ,故B错误;
,故B错误;
C.对氯甲苯中甲基和氯原子处于对位关系,结构简式: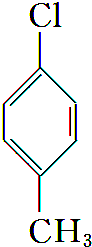 ,故C错误;
,故C错误;
D.乙醇的分子式为C2H6O,故D正确;
故选D.
点评 本题考查电子式、结构简式、分子式的书写,掌握常见的化学用语的概念及正确表示方法,明确球棍模型和比例模型的区别,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 乙烯能发生加聚反应,可用于制塑料 | |
| B. | 硝酸具有酸性,可用于实验室制氢气 | |
| C. | 氨气易溶于水,可作制冷剂 | |
| D. | 蛋白质遇CuSO4溶液发生凝聚,可用于提纯蛋白质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
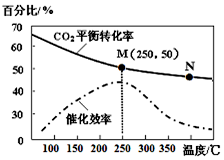 甲醇是一种可再生能源,由CO2制备甲醇的过程可能涉及的反应如下:
甲醇是一种可再生能源,由CO2制备甲醇的过程可能涉及的反应如下:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
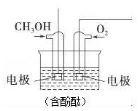 将甲醇与氧气分别通入如图所示的装置的电极中,可构成甲醇燃料电池,请回答下列问题:
将甲醇与氧气分别通入如图所示的装置的电极中,可构成甲醇燃料电池,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
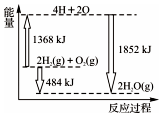
| A. | H2(g)和O2(g)反应生成H2O(g),这是个吸热过程 | |
| B. | 由2 mol H2和1 mol O2变成4 mol H、2 mol O原子,这是个放热过程 | |
| C. | 2 mol H2(g)和1 mol O2(g)反应生成2 mol H2O(g),共放出484 KJ能量 | |
| D. | 4 mol H、2 mol O生成2 mol H2O(g),共放出484 KJ能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它在周期表的第5周期,第IA族 | |
| B. | 氢氧化铷是弱碱,是一种离子化合物 | |
| C. | 铷的一种核素${\;}_{37}^{86}$Rb原子核内的中子数与电子数之差49 | |
| D. | 在钠、钾、铷三种单质中,铷的熔点最高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 变成
变成 ,现有某溴代烷A,分子式为C4H9Br,在NaOH醇溶液中加热得到有机物B,B被酸性高锰酸钾溶液氧化后不可能得到的产物是( )
,现有某溴代烷A,分子式为C4H9Br,在NaOH醇溶液中加热得到有机物B,B被酸性高锰酸钾溶液氧化后不可能得到的产物是( )| A. | 只有CH3COOH | B. | CO2和 CH3COCH3 | ||
| C. | CO2和CH3CH2COOH | D. | HCOOH和CH3CH2COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溴苯中的Br2(氢氧化钠溶液) | B. | 苯中的甲苯(浓溴水) | ||
| C. | 乙烷中的乙烯(酸性高锰酸钾) | D. | 甲烷中的乙炔 (H2) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com