
”¾ĢāÄæ”æĻņ20mL 1molL©1µÄAl2£ØSO4£©3ČÜŅŗÖŠ¼ÓČė20mLNaOHČÜŅŗ£¬³ä·Ö·“Ó¦æɵĆ1.56g³Įµķ£¬Ōņ¼ÓČėµÄNaOHČÜŅŗµÄĪļÖŹµÄĮæÅضČæÉÄÜŹĒ____”¢____£®
”¾“š°ø”æ 3mol/L 7mol/L
”¾½āĪö”æ·ÖĒéæöĢÖĀŪ£ŗ1”¢ĒāŃõ»ÆÄĘ²»×ćĮ棬ĒāŃõøłČ«²æ×Ŗ»ÆĪŖ³Įµķ£»2”¢ĒāŃõ»ÆÄĘ¹żĮ棬ĻČÉś³É³Įµķ£¬ŗó³Įµķ²æ·ÖČܽā”£
(1)ĒāŃõ»ÆÄĘ²»×ćĮ棬ĒāŃõøłČ«²æ×Ŗ»ÆĪŖ³Įµķ£¬Éč NaOHČÜŅŗµÄĪļÖŹµÄĮæÅØ¶ČŹĒxmol/L£¬
3OH-+Al3+=Al(OH)3”ż
3mol 78g
0.02xmol 1.56g
![]() £½
£½![]() £¬Ōņ£ŗx=3
£¬Ōņ£ŗx=3
(2)ĮņĖįĀĮ²»×ćĮ棬ĻČÉś³É³Įµķ£¬ŗó³Įµķ²æ·ÖČܽā”£ĮņĖįĀĮÖŠAl3+µÄĪļÖŹµÄĮæĪŖ2”Į1mol/L”Į0.02L=0.04mol£¬1.56g³ĮµķŠčŅŖAl3+µÄĪļÖŹµÄĮæĪŖ![]() =0.02mol£¬×Ŗ±ä³ÉAlO2-µÄAl3+µÄĪļÖŹµÄĮæĪŖ0.02mol”£ÉčNaOHČÜŅŗµÄĪļÖŹµÄĮæÅØ¶ČŹĒymol/L£¬
=0.02mol£¬×Ŗ±ä³ÉAlO2-µÄAl3+µÄĪļÖŹµÄĮæĪŖ0.02mol”£ÉčNaOHČÜŅŗµÄĪļÖŹµÄĮæÅØ¶ČŹĒymol/L£¬
3OH-+Al3+=Al(OH)3”ż
3 mol 1mol
0.06mol 0.02mol
4OH- + Al3+=AlO2-+2H2O
4mol 1mol
0.08mol 0.02mol
ĖłŅŌNaOHČÜŅŗµÄĪļÖŹµÄĮæÅØ¶ČŹĒy=![]() =
=![]() =7mol/L£¬¹Ź“š°øĪŖ£ŗ3mol/L£»7mol/L”£
=7mol/L£¬¹Ź“š°øĪŖ£ŗ3mol/L£»7mol/L”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌēŌŚ1807Äź»Æѧ¼Ņ“÷Ī¬ÓƵē½āČŪČŚĒāŃõ»ÆÄĘÖʵĆÄĘ£ŗ4NaOH£ØČŪČŚ£© ![]() 4Na£«O2”ü£«2H2O£»ŗóĄ“øĒ”¤ĀĄČųæĖÓĆĢśÓėČŪČŚĒāŃõ»ÆÄĘ×÷ÓĆŅ²ÖʵĆÄĘ£¬·“Ó¦ŌĄķĪŖ3Fe£«4NaOH£ØČŪČŚ£©
4Na£«O2”ü£«2H2O£»ŗóĄ“øĒ”¤ĀĄČųæĖÓĆĢśÓėČŪČŚĒāŃõ»ÆÄĘ×÷ÓĆŅ²ÖʵĆÄĘ£¬·“Ó¦ŌĄķĪŖ3Fe£«4NaOH£ØČŪČŚ£© ![]() Fe3O4£«2H2”ü£«4Na”ü”£ĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ
Fe3O4£«2H2”ü£«4Na”ü”£ĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ

A. µē½āČŪČŚĒāŃõ»ÆÄĘÖĘÄĘ£¬Ńō¼«·¢ÉśµÄµē¼«·“Ó¦ĪŖ2OH££2e£===H2”ü£«O2”ü
B. øĒ”¤ĀĄČųæĖ·ØÖĘÄĘŌĄķŹĒĄūÓĆĢśµÄ»¹ŌŠŌ±ČÄĘĒæ
C. Čō“÷Ī¬·ØÓėøĒ”¤ĀĄČųæĖ·ØÖʵƵČĮæµÄÄĘ£¬ŌņĮ½·“Ó¦ÖŠ×ŖŅʵĵē×Ó×ÜŹżŅ²ĻąĶ¬
D. ÄæĒ°¹¤ŅµÉĻ³£ÓƵē½āČŪČŚĀČ»ÆÄĘ·ØÖĘÄĘ£ØČēÉĻĶ¼£©£¬µē½ā²ŪÖŠŹÆÄ«ĪŖŃō¼«£¬ĢśĪŖŅõ¼«
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ׏ĮĻĻŌŹ¾£ŗŠæÓėÅØĮņĖį¹²ČČ³żÉś³É¶žŃõ»ÆĮņĘųĢåĶā£¬»¹æÉÄܲśÉśĒāĘų£»ŌŚ¼ÓČȵÄĢõ¼žĻĀ¶žŃõ»ÆĮņæɱ»CuOŃõ»Æ”£ĪŖŃéÖ¤øĆ·“Ó¦µÄĘųĢå²śĪļ¼°ŠŌÖŹ£¬Éč¼ĘĮĖČēĻĀĶ¼ĖłŹ¾µÄŹµŃé×°ÖĆ£ØÉčŠæÓėÅØĮņĖį¹²ČČŹ±²śÉśµÄĘųĢåĪŖX£©”£

(1)ÉĻŹö×°ÖƵÄĮ¬½ÓĖ³ŠņĪŖ£ŗĘųĢåX”śA”ś____”śA”ś ”ś ”ś ”śD;
(2)·“Ó¦æŖŹ¼ŗ󣬹Ū²ģµ½µŚŅ»øö×°ÖĆAÖŠµÄĘ·ŗģČÜŅŗĶŹÉ«£¬ŹµŃé½įŹųŗóČ”ŹŹĮæøĆČÜŅŗÓŚŹŌ¹ÜÖŠ²¢¼ÓČČ£¬ĻÖĻóĪŖ_______________________________________£»
(3)×°ÖĆ CÖŠµÄNaOHČÜŅŗÄÜÓĆĻĀĮŠ____“śĢę£»
a.ĖįŠŌKMnO4ČÜŅŗ b.CaCl2ČÜŅŗ c.±„ŗĶNaHSO3ČÜŅŗ
×°ÖĆDµÄ×÷ÓĆŹĒ____________________________
(4)ĘųĢåXÖŠæÉÄÜŗ¬ÓŠH2µÄŌŅņŹĒ____________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÄ³ČŻ»żĪŖ1LµÄĆܱÕČŻĘ÷ÖŠĶØČė1mol CO2ŗĶ3mol H2£¬·¢Éś·“Ó¦£ŗCO2(g)£«3H2(g)![]() CH3OH(g)£«H2O(g) ¦¤H£¼0”£ĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ
CH3OH(g)£«H2O(g) ¦¤H£¼0”£ĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ
A. øĆ·“Ó¦ŌŚøßĪĀĻĀ²ÅÄÜ×Ō·¢½ųŠŠ
B. ŌŁ¼ÓČėŅ»¶ØĮæCO2£¬Ōņn(CH3OH)/n(CO2)¼õŠ”
C. ĪĀ¶ČÉżøߣ¬·“Ó¦µÄĘ½ŗā³£ŹżKŌö“ó
D. µ±CO2ŗĶH2×Ŗ»ÆĀŹĻąµČŹ±£¬øĆ·“Ó¦“ļµ½»ÆŃ§Ę½ŗā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æA”¢B”¢C”¢D¾łĪŖ֊ѧ»Æѧ³£¼ūĪļÖŹ£¬ĒŅ¾łŗ¬ÓŠĶ¬Ņ»ÖÖŌŖĖŲ£¬ĖüĆĒÖ®¼äÓŠČēĻĀ×Ŗ»Æ£¬ĘäÖŠAŹĒµ„ÖŹ”£
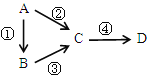
£Ø1£©ČōCŹĒµ»ĘÉ«¹ĢĢå³£ÓĆÓŚŗōĪüĆę¾ßÖŠµÄ¹©Ńõ¼Į£¬DŹĒŅ»ÖÖĒæ¼ī”£ŌņC×÷¹©Ńõ¼ĮŹ±ÓėCO2·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ_______________________£»ĘäÖŠ»¹Ō¼ĮŹĒ________£¬Ńõ»Æ²śĪļŹĒ___________£¬7.8g C²Ī¼Ó·“Ó¦Ź±×ŖŅʵĵē×ÓŹżŹĒ___________”£
£Ø2£©ČōB”¢D¼ČÄÜČÜÓŚĒæĖįČÜŅŗ£¬ÓÖÄÜČÜÓŚĒæ¼īČÜŅŗ£¬·“Ó¦¢Ś¢Ū¾łŠčŅŖĒæ¼īŠŌČÜŅŗ£¬·“Ó¦¢ÜæÉŅŌĶعżµĪ¼ÓÉŁĮæĻ”ŃĪĖįŹµĻÖ”£¾Ż“ĖŠ“³öAŌŖĖŲµÄŌ×Ó½į¹¹Ź¾ŅāĶ¼ŹĒ______”£ĒėŠ“³öAÓĆÓŚŗø½ÓĢś¹ģµÄ»Æѧ·½³ĢŹ½___________________________”£ĒėŠ“³ö¢ŚµÄĄė×Ó·½³ĢŹ½_____________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĢ¼ŗĶµŖµÄ»ÆŗĻĪļÓėČĖĄąÉś²ś”¢Éś»īĆÜĒŠĻą¹Ų£®

£Ø1£©ŌŚŅ»ŗćĪĀ”¢ŗćČŻĆܱÕČŻĘ÷ÖŠ·¢Éś·“Ó¦£ŗNi £Øs£©+4CO£Øg£©![]() Ni£ØCO£©4£Øg£©£¬”÷H£¼0£®ĄūÓĆøĆ·“Ó¦æÉŅŌ½«“ÖÄų×Ŗ»ÆĪŖ“æ¶Č“ļ99.9%µÄøß“æÄų£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ £ØĢī×ÖÄø±ąŗÅ£©£®
Ni£ØCO£©4£Øg£©£¬”÷H£¼0£®ĄūÓĆøĆ·“Ó¦æÉŅŌ½«“ÖÄų×Ŗ»ÆĪŖ“æ¶Č“ļ99.9%µÄøß“æÄų£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ £ØĢī×ÖÄø±ąŗÅ£©£®
A£®Ōö¼ÓNiµÄĮææÉĢįøßCOµÄ×Ŗ»ÆĀŹ£¬NiµÄ×Ŗ»ÆĀŹ½µµĶ
B£®ĖõŠ”ČŻĘ÷ČŻ»ż£¬Ę½ŗāÓŅŅĘ£¬”÷H¼õŠ”
C£®·“Ó¦“ļµ½Ę½ŗāŗ󣬳äČėCOŌŁ“Ī“ļµ½Ę½ŗāŹ±£¬COµÄĢå»ż·ÖŹż½µµĶ
D£®µ±4vÕż[Ni£ØCO£©4]=vÕż£ØCO£©Ź±»ņČŻĘ÷ÖŠ»ģŗĻĘųĢåĆÜ¶Č²»±äŹ±£¬¶¼æÉĖµĆ÷·“Ó¦ŅŃ“ļ»ÆŃ§Ę½ŗāדĢ¬
£Ø2£©COÓėÄų·“Ó¦»įŌģ³Éŗ¬Äų“߻ƼĮµÄÖŠ¶¾£®ĪŖ·ĄÖ¹Äų“߻ƼĮÖŠ¶¾£¬¹¤ŅµÉĻ³£ÓĆSO2½«COŃõ»Æ£¬¶žŃõ»ÆĮņ×Ŗ»ÆĪŖµ„ÖŹĮņ£®
ŅŃÖŖ£ŗCO£Øg£©+1/2QUOTE\*MERGEFORMATO2£Øg£©=CO2£Øg£©”÷H=©Q1 kJmol©1
S£Øs£©+O2£Øg£©=SO2£Øg£©”÷H=©Q2 kJmol©1
ŌņSO2£Øg£©+2CO £Øg£©=S£Øs£©+2CO2£Øg£©”÷H= £®
£Ø3£©¶ŌÓŚ·“Ó¦£ŗ2NO£Øg£©+O2ØT2NO2£Øg£©£¬ĻņÄ³ČŻĘ÷ÖŠ³äČė10molµÄNOŗĶ10molµÄO2£¬ŌŚĘäĖūĢõ¼žĻąĶ¬Ź±£¬·Ö±š²āµĆNOµÄĘ½ŗā×Ŗ»ÆĀŹŌŚ²»Ķ¬Ń¹Ēæ£ØP1”¢P2£©ĻĀĖęĪĀ¶Č±ä»ÆµÄĒśĻߣØČēĶ¼1£©£®
¢Ł±Č½ĻP1”¢P2µÄ“󊔹ŲĻµ£ŗ £®
¢Ś700”ꏱ£¬ŌŚŃ¹ĒæĪŖP2Ź±£¬¼ŁÉčČŻĘ÷ĪŖ1L£¬ŌņŌŚøĆĢõ¼žĘ½ŗā³£ŹżµÄŹżÖµĪŖ £Ø×ī¼ņ·ÖŹżŠĪŹ½£©
£Ø4£©NO2”¢O2ŗĶČŪČŚNaNO3æÉÖĘ×÷Č¼ĮĻµē³Ų£¬ĘäŌĄķČēĶ¼2ĖłŹ¾£®øƵē³ŲŌŚŹ¹ÓĆ¹ż³ĢÖŠŹÆÄ«Iµē¼«ÉĻÉś³ÉŃõ»ÆĪļY£¬ÄĒĆ“ŹÆÄ«II¼«µē¼«·“Ó¦Ź½ĪŖ £®ČōøĆČ¼ĮĻµē³ŲŹ¹ÓĆŅ»¶ĪŹ±¼äŗ󣬹²ŹÕ¼Æµ½20mol Y£¬ŌņĄķĀŪÉĻŠčŅŖĻūŗıź×¼×“æöĻĀŃõĘųµÄĢå»żĪŖ L£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ³£ĪĀŹ±£¬Mg(OH)2µÄČܶȻż³£ŹżKsp£½5.6”Į10£12£¬Č”ŹŹĮæµÄMgCl2ČÜŅŗ£¬¼ÓČėŅ»¶ØĮæµÄÉÕ¼īČÜŅŗ“ļµ½³ĮµķČܽāĘ½ŗā£¬²āµĆpH£½13.0£¬ŌņĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ(””””)
A. ĖłµĆČÜŅŗÖŠµÄc(H£«)£½1.0”Į10£13 mol”¤L£1
B. ĖłµĆČÜŅŗÖŠÓÉĖ®µēĄė²śÉśµÄc(H£«)£½1.0”Į10£13 mol”¤L£1
C. Ėł¼ÓµÄÉÕ¼īČÜŅŗpH£½13.0
D. ĖłµĆČÜŅŗÖŠµÄc(Mg2£«)£½5.6”Į10£10 mol”¤L£1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠŠšŹöÕżČ·µÄŹĒ£Ø £©
A.½«40g NaOHČÜÓŚĖ®Åä³É1LČÜŅŗ£¬ĘäĪļÖŹµÄĮæÅضČĪŖ1mol”¤L-1
B.±ź×¼×“æöĻĀ£¬18gĖ®µÄĢå»żŌ¼ĪŖ22.4L
C.ĮņĖįµÄĦ¶ūÖŹĮæŹĒ98 g
D.³£ĪĀ³£Ń¹ĻĀ£¬1 molŃõĘųµÄĢå»żĪŖ22.4 L
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æI£®ČÕ³£Éś»īÖŠ³“¹ż²ĖµÄĢś¹ųĪ“¼°Ź±Ļ“¾»£¬²»¾Ć»įŅņøÆŹ“¶ų³öĻÖŗģŗÖÉ«Šā°ß”£Ēė»Ų“š£ŗ
¢ŁĢś¹ųµÄŠāŹ“Ö÷ŅŖŹĒŠĪ³ÉĮĖ_____________Ģī£Ø”°Ōµē³Ų”±»ņ”°µē½ā³Ų”±)£¬·¢Éś__________øÆŹ“£ØĢī”°ĪöĒā”±»ņ”°ĪüŃõ”±£©”£
¢ŚŠ“³öĢś¹ųøÆŹ“Ź±Õż¼«µÄµē¼«·“Ó¦Ź½£ŗ _______________________________
II£®¢ŁÄ³Ķ¬Ń§ÓĆĢ¼°ō”¢Ķ°ōŗĶĻ”ĮņĖį”¢µ¼ĻßµČĪŖŌ²ÄĮĻ£¬ŹµĻÖĮĖĶس£Ģõ¼žĻĀ²»ÄÜ·¢ÉśµÄ·“Ó¦£ŗCu+H2SO4(Ļ”)£½CuSO4+H2”ü”£ĒėŌŚæņĶ¼æհד¦»³öÄܹ»ŹµĻÖÕāŅ»·“Ó¦µÄµē»ÆѧװÖĆĶ¼£¬²¢ŌŚĶ¼ÖŠ½ųŠŠ±ŲŅŖµÄ±ź×¢”£_______________________
¢ŚÄ³Ķ¬Ń§ŌŚ×öŅ»¶ØĢõ¼žĻĀĶÓėĻ”ĮņĖįµÄ·“Ó¦ŹµŃ鏱£¬æ“µ½Ģ¼°ōÉĻÓŠĘųÅŻ²śÉś£¬¶ųĶ°ōȓƻӊ±»øÆŹ“”£ĒėÄć·ÖĪöĘäŌŅņ£ŗ_______________________
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com