
【题目】Ⅰ.下列物质中:
(1)互为同分异构体的有_______ (2)互为同素异形体的有_______
(3)属于同位素的有__________ (4)属于同一种物质的有______。(填序号)
①液氯和氯气 ②白磷和红磷 ③ 和
和![]() ④3717Cl和3517Cl ⑤(CH3)2CHCH3和CH3(CH2)2CH3 ⑥ CH4和CH3CH2CH3
④3717Cl和3517Cl ⑤(CH3)2CHCH3和CH3(CH2)2CH3 ⑥ CH4和CH3CH2CH3
Ⅱ.现有6种物质:①MgCl2 ②HCl ③SO2 ④K2CO3 ⑤CaO ⑥NaOH。请根据下列标准,对上述物质进行分类(填序号):
(1)属于共价化合物是_______。
(2)含共价键的离子化合物是______。
【答案】③⑤ ② ④ ① ②③ ④⑥
【解析】
Ⅰ.①液氯是液态的氯气,所以液氯和氯气属于同种物质;
②白磷和红磷都是由磷元素组成的不同单质,属于同素异形体;
③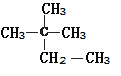 和
和![]() 分子式相同,结构不同,属于同分异构体;
分子式相同,结构不同,属于同分异构体;
④3717Cl和3517Cl质子数都为17,质量数分别为37和35,属于同位素;
⑤(CH3)2CHCH3和CH3(CH2)2CH3分子式相同,结构不同,属于同分异构体;
⑥ CH4和CH3CH2CH3结构相似,组成上相差2个CH2,属于同系物;
故答案为:(1). ③⑤ (2). ② (3). ④ (4). ①;
Ⅱ.①MgCl2中只含有离子键,属于离子化合物;②HCl中只含有共价键,属于共价化合物;③SO2中只含共价键,属于共价化合物;④K2CO3中钾离子与碳酸根以离子键结合,碳酸根中碳原子与氧原子之间以共价键结合,属于离子化合物;⑤CaO中只含离子键,属于离子化合物;⑥NaOH中钠离子与氢氧根以离子键结合,氢氧根中氢原子与氧原子以共价键结合,属于离子化合物;故属于共价化合物是②③;含共价键的离子化合物是④⑥。


科目:高中化学 来源: 题型:
【题目】常温下,向10mL0.1mol·L-1CuCl2溶液中滴入0.1ml·L-1的Na2S溶液,滴加过程中溶液中-1gc(Cu2+)随滴人的Na2S溶液体积的变化如图所示。下列叙述正确的是
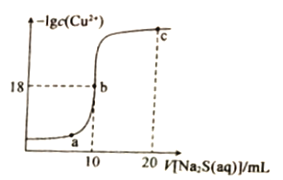
A. Na2S溶液中:c(S2-)+c(HS-)+c(H2S)==2c(Na+)
B. Ksp(CuS)的数量级为10-36
C. a、b、c三点溶液中,b点水的电离程度最大
D. c点溶液中:c(C1-)=2c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A. 氯气溶于水:Cl2+H2O![]() 2H++Cl-+ClO-
2H++Cl-+ClO-
B. 钠与水反应:Na+2H2O===Na+2OH+H2↑
C. 氧化亚铁溶于稀硝酸:FeO+2H+===Fe2++H2 O
D. 向碳酸氢铵溶液中加入足量石灰水:NH4++HCO3-+Ca2++2OH-===CaCO3 ↓+NH3·H2O+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物M 的结构简式如下:下列有关M 叙述不正确的是( )
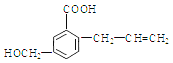
A. M的分子式为C11H12O3
B. 能使溴的四氯化碳溶液褪色
C. 一定条件下,M能生成高分子化合物
D. 能发生加成反应不能发生取代反应
【答案】D
【解析】
试题A.根据物质的结构简式可知M的分子式是C11H12O3,正确; B.该物质的分子中含有碳碳双键,因此能使溴的四氯化碳溶液褪色,正确;C. 该物质的分子中含有碳碳双键,在一定条件下发生加聚反应形成高聚物,正确;D. 化合物M含有碳碳双键,因此能发生加成反应,含有醇羟基、羧基,因此可以发生取代反应,错误。
考点:考查有机物的结构与性质的关系的知识。
【题型】单选题
【结束】
22
【题目】下列有关金属腐蚀与防护的说法不正确的是( )
A. 钢铁发生电化学腐蚀时,若表面水膜呈中性,则正极发生的反应为:2H2O+O2+4e一= 4OH一
B. 在潮湿的空气中,黄铜(铜锌合金)制品比纯铜制品更易产生铜绿
C. 金属制品在海水中比淡水中更容易发生腐蚀
D. 从本质上看,金属腐蚀是金属原子失去电子变成阳离子被氧化的过程
【答案】B
【解析】A、钢铁发生电化学腐蚀时,若表面水膜呈中性发生吸氧腐蚀,则正极发生的反应为:2H2O+O2+4e一=4OH一,A正确;B、在潮湿的空气中易发生电化学腐蚀,锌的金属性强于铜,因此黄铜(铜锌合金)制品比纯铜制品更不易产生铜绿,B错误;C、海水中含电解质浓度大,淡水中含电解质浓度小,故金属制品在海水中比淡水中更容易发生腐蚀,C正确;D、从本质上看,金属腐蚀是金属原子失去电子变成阳离子被氧化的过程,D正确;答案选B。
【题型】单选题
【结束】
23
【题目】下列说法不正确的是
A. 麦芽糖及其水解产物均能发生银镜反应
B. 用溴水即可鉴别苯酚溶液,2,4-已二烯和甲苯
C. 在酸性条件下,![]() 的水解产物是
的水解产物是![]() 和
和![]()
D. 用甘氨酸![]() 和丙氨酸
和丙氨酸![]() 缩合最多可形成4种二肽
缩合最多可形成4种二肽
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某有机物的结构简式为![]() ,判断下列说法中不正确的是( )
,判断下列说法中不正确的是( )
A. 它可以使酸性KMnO4溶液褪色
B. 它可发生取代反应、加成反应、加聚反应、氧化反应
C. 1mol该有机物与氢气发生加成反应,最多可以消耗5mol氢气
D. 该有机物分子式为C14H17
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇燃料电池中采用磺酸类质子溶剂,在200℃左右时供电,电池总反应为:C2H5OH+3O2=2CO2+3H2O,电池示意如图。下列说法中,正确的是
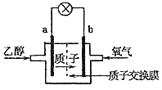
A. 电池工作时,H+向电池的负极迁移
B. 电池工作时,电流由a极沿导线流向b极
C. a极上发生的电极反应是:C2H5OH+3H2O+12e-=2CO2+12H+
D. b极上发生的电极反应是:4H++O2+4e-=2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有甲、乙两个化学小组利用两套相同装置,通过测定产生相同体积气体所用时 间长短来探究影响 H2O2 分解速率的因素(仅一个条件改变)。甲小组有如下实验设计方 案。
实验编号 | 温度 | 催化剂 | 浓度 |
甲组实验Ⅰ | 25 ℃ | 三氧化二铁 | 10 mL 5% H2O2 |
甲组实验Ⅱ | 25 ℃ | 二氧化锰 | 10 mL 5% H2O2 |
甲、乙两小组得出如下图数据。
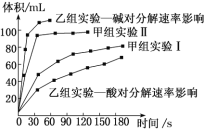
(1)甲小组实验得出的结论是_____。
(2) 由乙组研究的酸、碱对 H2O2 分解影响因素的数据分析,相同条件下 H2O2 在______(填“酸”或“碱”)性环境下放出气体速率较快;由此,乙组提出可以用BaO2 固体与硫酸溶液反应制 H2O2,其反应的离子方程式为___________________________;支持这一方案的理由是_____。
(3)已知过氧化氢是一种极弱的二元酸:H2O2![]() H++HO2- (Ka1=2.4×10-12)。当稀 H2O2溶液在碱性环境下分解时会发生反应 H2O2+OH-
H++HO2- (Ka1=2.4×10-12)。当稀 H2O2溶液在碱性环境下分解时会发生反应 H2O2+OH-![]() HO2-+H2O,该反应中,正反应速率为 v 正=k正·c(H2O2)·c(OH-),逆反应速率为 v 逆=k 逆·c(H2O)·c(HO2- ),其中 k 正、k 逆为速率常数,则 k 正与 k 逆的比值为_________________________________________(保留 3 位有效数字)。
HO2-+H2O,该反应中,正反应速率为 v 正=k正·c(H2O2)·c(OH-),逆反应速率为 v 逆=k 逆·c(H2O)·c(HO2- ),其中 k 正、k 逆为速率常数,则 k 正与 k 逆的比值为_________________________________________(保留 3 位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳元素是组成生物体的最基本元素,这是因为碳元素在生物体中
A. 所含的能量最多 B. 最容易被吸收利用
C. 所起的作用最大 D. 构成有机物的基本骨架
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(题文)某有机物有如下转化关系: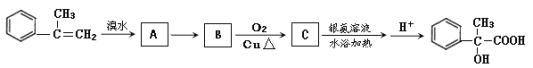
(1)写出反应A→B的反应条件是____________________,C中的官能团是________________(写结构简式)。
(2)写出反应B→C 的化学方程式和反应类型:____________, 反应类型为__________ 。
写出1mol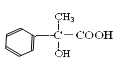 在浓硫酸加热条件下生成某一有机合物和1molH2O的化学方程式和反应类型:_______________________,反应类型为__________ 。
在浓硫酸加热条件下生成某一有机合物和1molH2O的化学方程式和反应类型:_______________________,反应类型为__________ 。
(3)写出一种符合下列条件的C的同分异构体的结构简式_______________________。
①属于芳香族化合物,苯环上有两个取代基
②与碳酸氢钠溶液反应放出二氧化碳气体
③苯环上的一氯代物有两种
(4)根据已学知,写出以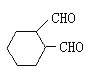 和CH3CH2Cl,为原料合成重要的化工产品
和CH3CH2Cl,为原料合成重要的化工产品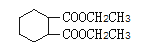 的路线流程图(无机试剂任选)。________________合成路线流程图示例如下:
的路线流程图(无机试剂任选)。________________合成路线流程图示例如下: 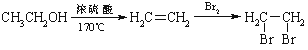
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com