
化学反应A2+B2═2AB的能量变化如图所示,则下列说法正确的是()
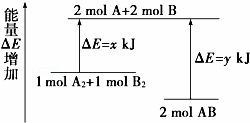
A. 该反应是吸热反应
B. 断裂1 mol A﹣A键和1 mol B﹣B键能放出x kJ能量
C. 形成2 mol A﹣B键需要放出y kJ的能量
D. 2 mol AB的总能量高于1 mol A2和1 mol B2的总能量
考点: 反应热和焓变.
专题: 化学反应中的能量变化.
分析: A、根据反应物的能量高于生成物的能量时,反应是放热反应;
B、根据旧键的断裂吸收能量,新键的形成释放能量;
C、根据旧键的断裂吸收能量,新键的形成释放能量;
D、根据图象可判断反应物与生成物的总能量.
解答: 解:A、因反应物的能量高于生成物的能量时,反应是放热反应,故A错误;
B、因旧键的断裂吸收能量,而不是释放能量,故B错误;
C、因旧键的断裂吸收能量,由图可知形成2molA﹣B键需要放出ykJ能量,故C正确;
D、由图可知,1molA2和1molB2的总能量高于2molAB的总能量,故D错误;
故选C.
点评: 本题考查学生有关化学反应中的能量变化知识,可以根据所学知识来进行,难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
X、Y、Z、W四种金属,当X、Y组成原电池时,Y为负极;当Z、W组成原电池时,W为正极;W能将Y从其盐溶液中置换出来,则几种金属的活动性顺序为()
A. Z>W>X>Y B. X>Y>W>Z C. Z>W>Y>X D. X>Y>Z>W
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y代表两种非金属元素,下列不能说明非金属性X比Y强的是()
A. Y的阴离子Y﹣的还原性强于X的阴离子X﹣
B. X的氢化物的水溶液的酸性比Y的氢化物的水溶液的酸性强
C. X的单质X2能将Y的阴离子Y﹣氧化成Y2
D. X、Y的单质分别与Fe化合,产物中前者Fe为+3价,后者Fe为+2价
查看答案和解析>>
科目:高中化学 来源: 题型:
反应H2(g)+I2(g)⇌2HI(g)在体积固定的密闭容器中进行,达到平衡状态的标志是()
①单位时间内断裂n mol H﹣H键的同时形成2n mol H﹣I键
②单位时间内生成n molI2的同时生成2n molHI
③2v正(H2)=v逆(HI)
④HI分子数不再改变
⑤混合气体颜色不再改变
⑥混合气体压强不再改变.
A. ②④⑤⑥ B. ②③④⑤ C. ①③④⑤ D. 全部
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D四种短周期元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体甲;D的L层电子数等于K、M两个电子层上的电子数之和.
(1)写出A的原子结构示意图 .
(2)D的质子数和中子数相等,D的原子组成符号为 .
(3)用电子式表示A、D两元素形成AD2的过程: ;写出C2B2的电子式 .
(4)氢元素与B、D 均可以形成原子个数比为2:1的化合物,H2B的熔沸点高于H2D的原因是 .
(5)写出甲和A的最高价氧化物反应的化学方式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作中数据合理的是()
A. 用10 mL 量筒量取5.2 mL盐酸
B. 用广泛pH试纸测得某溶液的pH值为12.5
C. 用托盘天平称取25.12gNaCl固体
D. 用100 mL容量瓶配制50mL0.1 mol/L的盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中,既属于化合反应,又属于氧化还原反应的是()
A. H2+Cl2 2HCl B. 2H2O2
2HCl B. 2H2O2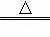 2H2O+O2↑
2H2O+O2↑
C. CaO+H2O=Ca(OH)2 D. Zn+H2SO4=ZnSO4+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
铯原子钟300年误差不超过5秒.铯元素在周期表的信息如图,下列说法正确的是( )

|
| A. | 铯元素属于非金属元素 |
|
| B. | 铯原子的质子数是55 |
|
| C. | 铯元素符号为CS |
|
| D. | 铯原子的相对原子质量为132.9g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com