
����������ȷ����
A��H2(g)��ȼ������285.8 kJ��mol��1����2H2O(g)=2H2(g)��O2(g) ��H����285.8 kJ��mol��1
B�����ڷ�Ӧ2H2O2==2H2O��O2���������¶��ܼ���O2����������
C����֪2C(s)��2O2(g)��2CO2(g) ��H1�� 2C(s)��O2(g)��2CO(g) ��H2����H1>��H2
D����CuCl2ˮ��Һ�д�������ƽ�⣺[Cu(H2O)4]2+(��)+4Cl��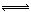 [CuCl4]2��(��)+4H2O��������Һ�м���ʳ�ο�������ʹ��Һ������ɫ
[CuCl4]2��(��)+4H2O��������Һ�м���ʳ�ο�������ʹ��Һ������ɫ

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ʡ����Ͽ�и߶���ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ������
���������Һ�У��������µ���ƽ�⣺HF H++F��
H++F��
��1���������NaOH������ƽ���� ��Ӧ�����ƶ���c��H+�� ��
��2���������NaF������ƽ���� ��Ӧ�����ƶ���c��H+�� ��
��3�������¶ȣ�����ƽ���� ��Ӧ�����ƶ���c��H+�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016���㽭ʡ������ѧ�����в������ۻ�ѧ�Ծ��������棩 ���ͣ������
��X��Y��Z��R���ֶ���������Ԫ�أ�Y��Z��Rͬ���ڡ������Ϣ���£�
�����Ϣ | |
X | ����Ϊ˫ԭ�ӷ��ӡ�����������Һ̬����������е�ϵͿ��Ȼ��X�ĵ��� |
Y | ��YԪ�ص�������ɫ��ӦΪ��ɫ |
Z | ͬ����Ԫ����ԭ�Ӱ뾶��С |
R | RԪ��ԭ�ӵ�������������K���������3�� |
I����1��ZԪ�������ڱ���λ���� ��Y��Z��R�����ӵİ뾶�Ӵ�С��˳���� �������ӷ��ű�ʾ����
��2����X��Z����Ԫ����ɵĻ�����ף�������Ϊ�ӷ��ĵ���ɫҺ�壬���ӹ���Ϊ�����Σ��ҷ�����X��Z����ԭ���������ﵽ8�����ӵ��ȶ��ṹ������ˮ���γ�һ�ֳ�����Ư�������ʡ���ĽṹʽΪ ��
��3���������ң�Y2R����Һ�ڿ����г��ڷ��ã���������Ӧ��������������ƵĽṹ�ͻ�ѧ�������Ƶ�����Y2R2������Һ�Ի�ɫ����Y2R2�ĵ���ʽΪ ��д������Һ�ڿ����б�������Y2R2�Ļ�ѧ����ʽ ��
II��Ԫ��X������γɶ��ֻ��������������졣
��4����ΪһԪ���ᣬ������������ƣ�����ʮ���ȶ�����ײ���ͱ�ը��8.6 g����ը�ֽ�����H2��6.72 L(�����)X2��д���䱬ը�Ļ�ѧ����ʽ ��
��5����Ϊ���ӻ������ˮ��Ӧ����H2�������죬���������ܶ�Ϊ0.76 g��L��1�������ʶ��Ļ�ѧʽΪ ��
��6�����ڸ����������ܻ�ԭFe2O3���������ֵ��ʣ�д���÷�Ӧ�Ļ�ѧ����ʽ ������������ɵIJ����п��ܻ���FeO�������ʵ�鷽����֤(�û�ѧ����) ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ�Ϻӿ��и�����ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����������Ͷ��һ��Ũ�ȵ��Ȼ������Ȼ�ͭ�Ļ����Һ�У���ַ�Ӧ����Һ��ʣ������������������۵�������ͬ����ԭ��Һ���Ȼ������Ȼ�ͭ��Ũ��֮��Ϊ
A��2��7 B��3��4 C��4��7 D��2��3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�������и߶���ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ������
700��ʱ�����ݻ�Ϊ2L���ܱ������г���һ������CO��H2O,������Ӧ��
CO(g)��H2O(g)  CO2(g)��H2(g)��Ӧ�����вⶨ�IJ������ݼ��±�
CO2(g)��H2(g)��Ӧ�����вⶨ�IJ������ݼ��±�
��Ӧʱ��/min | n(CO)/mol | n(H2O)/ mol |
0 | 1.20 | 0.60 |
t1 | 0.80 | |
t2 | 0.20 |
��������ش��������⣺
��1����Ӧ��t1min�ڵ�ƽ������Ϊv(H2)�� mol��L��1��min��1
��2�������������������䣬��ʼʱ�������г���0.60molCO(g)��0.30 molH2O(g)������ƽ��ʱ��n(CO2)�� mol��
��3�������������������䣬��ƽ����ϵ����ͨ��H2O(g) ��CO2(g)��0.10mol���ﵽ��ƽ��ʱCO2(g)���������Ϊ ��
��4�����¶�����800�棬������Ӧƽ�ⳣ��Ϊ0.64��������ӦΪ ��Ӧ������ȡ������ȡ� ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ��ʡ�߶���ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ԭ�ӹ����ʾʽ�У���ʾ��ԭ�ӵĻ�̬���ӹ���Ų�ʽ��ȷ����
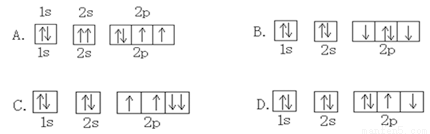
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꽭��ʡ��������У�߶���ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ʵ����
�屽��һ�ֳ��õĻ���ԭ�ϡ�ʵ�����Ʊ��屽��ʵ�鲽�����£�
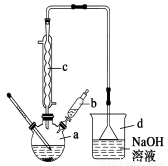
����1����a�м���15 mL����������м���ٽ�b��4.0 mLҺ���������뵽a�У���ַ�Ӧ��
����2����a�м���10 mLˮ��Ȼ����˳�ȥδ��Ӧ����м��
����3����Һ������10 mLˮ��8 mL 10%��NaOH��Һ��10 mL ˮϴ�ӣ���Һ�ô��屽��
����4����ֳ��Ĵ��屽�м�����������ˮ�Ȼ��ƣ����á����˼��ôֲ�Ʒ��
��1������1����a�з�������Ҫ��Ӧ��
��2������d��������
��3����b�е�Һ���������뵽a�У������ܿ��ټ����ԭ����
��4������c��������������������������Ҫ������ ���ѧʽ��
�� | �� | �屽 | |
�ܶ�/g��cm��3 | 0.88 | 3.10 | 1.50 |
�е�/�� | 80 | 59 | 156 |
��ˮ�е��ܽ�� | �� | �� | �� |
��5������4�õ��Ĵֲ�Ʒ�л��������ʱ�����֪�����屽���й������������ϱ�����Ҫ��һ���ᴿ�ֲ�Ʒ����������е�ʵ����������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ��ʡ�������������߶���ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����ΪVL�ĺ����ܱ�������ʢ��һ����H2��ͨ��Br2��g��������Ӧ��H2��g��+Br2��g�� 2HBr��g������H��0�����¶ȷֱ�ΪT1��T2��ƽ��ʱ��H2�����������Br2��g�������ʵ����仯��ϵ��ͼ��ʾ������˵������ȷ����
2HBr��g������H��0�����¶ȷֱ�ΪT1��T2��ƽ��ʱ��H2�����������Br2��g�������ʵ����仯��ϵ��ͼ��ʾ������˵������ȷ����
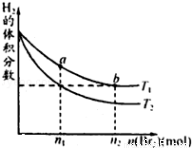
A��a��b����ķ�Ӧ���ʣ�b��a
B��T1��T2
C��T1ʱ������Br2��g�����룬ƽ��ʱHBr�����������������
D��Ϊ�����Br2��g����ת���ʣ��ɲ�ȡ��HBrҺ������ʱ���ߵķ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ������ʡ��һ��ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ���ǣ�NA��ʾ�����ӵ�������ֵ����
��28 g���������е�ԭ����ĿΪNA
��4 g�����Ʊ�ɸ�����ʱʧȥ�ĵ�����ĿΪ0.1 NA
���ڳ��³�ѹ�£�11.2 L N2���еķ�����Ϊ0.5 NA
���ڱ�״���£� 1 mol�������е�ԭ����ΪNA
��0.5 mol���������������ᷴӦת�Ƶ�����Ϊ1.5NA
�ޱ�״���£�1 Lˮ����������Ϊ1/22.4NA
��17 g��������������ĿΪ10NA
A���٢ڢݢޢ� B���٢ڢܢݢ� C���ݢ� D���ܢݢ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com