
| ѡ�� | �������� | ʵ��ԭ�� |
| A | �����л����������ۣ�����Ũ����������Һ������ | ����������������Һ��Ӧ�����۲�������������Һ��Ӧ |
| B | �Ȼ�������Һ�л����Ȼ�������������ͭ�ۣ����� | ͭ�ܽ�Fe3+��ԭ��Fe2+��ͭ��Fe2+����Ӧ |
| C | ���������л��������ƣ��ڿ��������չ��� | �������������ڼ������������ɹ������� |
| D | �Ȼ�����Һ�л����Ȼ�þ������������������������ | �Ȼ�þˮ���������ᣬ����������������Ӧ���ٽ�Mg2+��ȫˮ�� |
| A�� | A | B�� | B | C�� | C | D�� | D |
���� A����������������Һ��Ӧ������������������Һ��Ӧ��
B��ͭ�������ӷ�Ӧ�����������ӣ��������µ����ʣ�
C�����������ܹ��������ˮ��������̼��Ӧ��
D��������þ���ܶȻ�С������������ʵ���˳�����ת����
��� �⣺A������Al�������ᷴӦ������Ӧ�����������ڼ�ʿ�������������Һ��ȥ�����е����ۣ���A��ȷ��
B���Ȼ�������Һ�л����Ȼ���������������ͭ�ۣ���Ӧ������ͭ���ӣ����������ʣ�Ӧ�������ۣ���B����
C�����ڹ�������������е�ˮ�֡�������̼��Ӧ�������ڿ��������գ�Ӧ�������������գ��ò�����������������C����
D���Ȼ�����Һ�л����Ȼ�þ������������þ���ܶȻ�С�������������ɼ�������������������������������ת����������þ����D����
��ѡA��
���� ���⿼�黯ѧ���ʵķ��롢�ᴿ������Ϊ�߿��������ͺ�Ƶ���㣬��Ŀ�Ѷ��еȣ����������ѧ���ķ���������ʵ�����������������Ŀ��飬ע��������ʵ����ʵ���ͬ�Լ�ʵ��ĺ����ԺͿ����Ե����ۣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �¶� | 250�� | 300�� | 350�� |
| K | 2.041 | 0.270 | 0.012 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
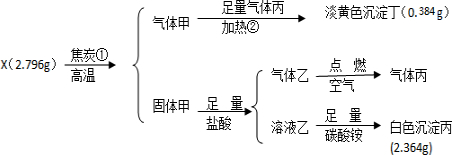
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | �÷�Ӧ��ƽ�ⳣ������ʽΪK=$\frac{{c}^{2}��CO��}{c��C{O}_{2}��•c��C��}$ | |
| B�� | 550��ʱ����Ӧ��ƽ���CO2��ת����ԼΪ5.7% | |
| C�� | 650��ʱ��ƽ����ٳ��������Ϊ3��2��CO2��CO�Ļ�����壬��ƽ�ⲻ�ƶ� | |
| D�� | T��ʱ���÷�Ӧ��ƽ�ⳣ������ֵΪ1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1��1 | B�� | 2��5 | C�� | 4��1 | D�� | 3��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ݢ٢ޢۢ� | B�� | �ݢڢޢۢ� | C�� | �ݢڢޢܢ� | D�� | �ݢ٢ޢܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ϡ���������������У���ַ�Ӧ��μ�KSCN��Һ�����������ɣ���Һδ��Ѫ��ɫ��˵��ϡ����ܽ�Fe����ΪFe3+ | |
| B�� | ��ȥFeCl3��Һ������Cu2+����������Cu2+��FeCl3��Һ�м����������ۣ���ַ�Ӧ����� | |
| C�� | �Ƚ�Fe��OH��3��Al��OH��3��Ksp����0.1mol•L-1��FeCl3��Һ�еμ�0.1mol•L-1��ˮ�����ٲ���������Ȼ���ٵ���0.1mol•L-1A1Cl3��Һ���۲����� | |
| D�� | ��֤������Fe3+��Br2��Cl2�����Թ������μ���1mL0.1mol•L-1FeBr2��Һ������KSCN��Һ��1mL����Ȼ����μ�����ˮ����������ֱ����ˮ�������۲������������л����ˮ���е����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com