
分析 2.24L该混合气体的物质的量为0.1mol,完全燃烧得到4.48L二氧化碳和3.6g水,生成二氧化碳的物质的量为0.2mol,水的物质的量为0.2mol,则说明混合气体平均分子式为C2H4,利用平均值法判断.
解答 解:2.24升该混合气体的物质的量=$\frac{2.24L}{22.4L/mol}$=0.1mol,完全燃烧得到4.48升二氧化碳和3.6克水,生成二氧化碳的物质的量=$\frac{4.48L}{22.4L/mol}$=0.2mol,水的物质的量=$\frac{3.6g}{18g/mol}$=0.2mol,则说明混合气体平均分子式为C2H4,可能为C2H2和C2H6混合,也可能为CH4和C3H4混合,
故答案为:C2H2、C2H6或CH4、C3H4.
点评 本题考查分子式的确定、混合物计算,题目难度中等,关键是利用平均分子组成判断烃的组成,常用方法有1、平均碳法 2、平均氢法 3、平均碳氢分子式法 4、平均式量法.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
 $\stackrel{△}{→}$
$\stackrel{△}{→}$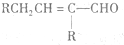 兔耳草醛是重要的合成香料,它具有独特的新鲜水果的清香.由枯茗酸
兔耳草醛是重要的合成香料,它具有独特的新鲜水果的清香.由枯茗酸 合成兔耳草醛的路线如下:
合成兔耳草醛的路线如下:
 、
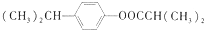
、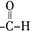 (写结构式);检验B中含氧官能团的实验方案是配制银氨溶液,取少量B加入新配制的银氨溶液中,然后水浴加热
(写结构式);检验B中含氧官能团的实验方案是配制银氨溶液,取少量B加入新配制的银氨溶液中,然后水浴加热 .
. 、
、 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 L 1 mol•L-1的醋酸溶液中含有的醋酸分子数为NA | |
| B. | 电解精炼铜时,当阳极上质量减少6.4 g时,电路中转移的电子数为2NA | |
| C. | 常温下,46 g NO2和N2O4的混合物中含有的氧原子数为2NA | |
| D. | 11.2 L CO2中含有的分子数为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  用图1装置除去HCl中少量的Cl2 | |
| B. |  用图2装置蒸干Al2(SO4)3饱和溶液制取无水Al2(SO4)3 | |
| C. |  图3制备并收集少量NO2 | |
| D. |  图4是原电池装置,Fe电极为阴极 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用溶解、过滤的方法提纯含有少量碳酸镁的氢氧化镁 | |
| B. | 向混有乙酸的乙酸乙酯中加入NaOH溶液再分液提纯乙酸乙酯 | |
| C. | 除去FeCl2中少量的FeBr2:加入适量氯水,在加四氯化碳萃取、分液 | |
| D. | 向AlCl3溶液中滴加氨水,产生白色沉淀,再加入NaHSO4溶液,沉淀消失 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com