
利用下图所示装置,选择适当试剂可完成实验A、B、C,并得出相应的实验结论。实验A、B、C所用试剂或所得结论列于下表中。
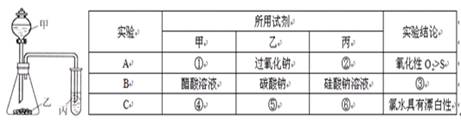
(1)请填写①-⑥的试剂名称或实验结论:
① ② ③
④ ⑤ ⑥
(2)请利用该装置自行设计一个有机实验D。回答下列问题:
实验所用试剂:甲 ,乙 ,丙 。
锥形烧瓶中反应的化学方程式为 ,大试管中的现象是 ;欲收集烧瓶中产生的气体,应采用 法,需补充的玻璃仪器至少有 。
(1)①蒸馏水 ②氢硫酸 ③酸性:醋酸>碳酸>硅酸 ④浓盐酸 ⑤高锰酸钾或氯酸钾 ⑥石蕊试液 (2)饱和食盐水;电石;高锰酸钾溶液或溴水;CaC2+2H2O→Ca(OH)2+CH≡CH↑;高锰酸钾溶液褪色;排水;集气瓶或水槽
由装置图可以知道是个固体(液体)+液体不加热的装置。
A: 若甲为H2O,乙为MnO2,丙中盛有氢硫酸(H2S饱和溶液),旋开活塞后,丙中的现象为溶液变浑浊,2H2S+O2=2S↓+2H2O;B:若甲为醋酸,乙为碳酸钠,丙中盛有硅酸钠,旋开活塞后,丙中的现象为有白色沉淀生成,则酸性:醋酸>碳酸>硅酸;C:若甲为浓盐酸,乙为KMnO4,丙中盛有石蕊试液,旋开活塞后,C中的现象是溶液褪色,说明有氯水具有漂白性;
③实验应该根据实验装置特点选择常温下固体与液体反应,生成气体与溶液丙反应。马上联想到实验室制备乙炔。甲为饱和食盐水,乙为电石,丙为高锰酸钾溶液(或溴水),CaC2+2H2O→Ca(OH)2+CH≡CH↑,乙炔氧化反应(或加成)高锰酸钾溶液褪色(其他的答案也可以)。


科目:高中化学 来源: 题型:阅读理解
| ||
| ||
| b-d |
| 16 |
| b-d |
| 16 |
| 16(d-a) |
| b-d |
| 16(d-a) |
| b-d |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 实验步骤 | 预期现象和结论 | 步骤1:取适量牙膏样品加水充分搅拌、过滤,得滤液A和沉淀B. | / | 步骤2:取适量滤液A于试管中, |
有 |
步骤3:取适量沉淀B于试管中,加入过量 |
/ | 步骤4:往所得滤液中通入过量二氧化碳. | 产生成白色沉淀, |
查看答案和解析>>
科目:高中化学 来源:2012届河北省三河一中高三上学期第二次月考化学试卷 题型:实验题
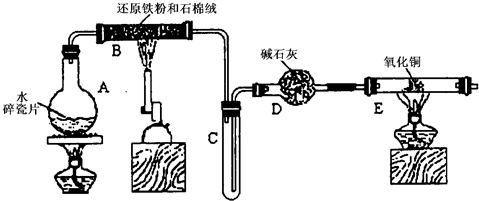
(12分)某学习小组利用下图所示装置进行“铁与水气反应”和其他实验(略去了夹持仪器)。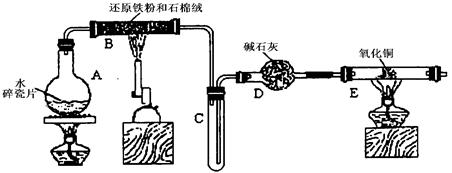
(1)为了安全,加热E以前必须进行的操作是____________________________。
(2) B中发生反应的化学方程式是 _______________。
(3)已知有反应:Cu2O+2H+ Cu+Cu2++H2O,则可用来检验反应后E中的红色固体中除Cu外是否含Cu2O,可用的试剂是________(填序号)
Cu+Cu2++H2O,则可用来检验反应后E中的红色固体中除Cu外是否含Cu2O,可用的试剂是________(填序号)
a.稀硝酸 b.稀硫酸 c.盐酸 d.浓硫酸
(4)在E后若再接二个盛碱石灰的干燥管(依次称为F和G),则还可用该装置测定水的组成。若反应后盛有药品的E的质量减轻了e g,F的质量增加了f g。水中元素的物质的量之比可表示为(不用化简)n(H):n(O)= ________:_______;若反应后E中除Cu外还含有另一种还原产物Cu2O,则该比值将___________ (选填“偏大”“偏小”或“无影响”)。
(5)某学生为了检验反应后固体的成分,反应前在E管中加入了氧化铜固体16g,反应后称量固体的质量变为13.6g,则13.6g的成分为:___________(若为混合物,需计算出各自的质量)
查看答案和解析>>
科目:高中化学 来源:2014届河北省高三调研考试理综化学试卷(解析版) 题型:填空题
工业上生产金属钛的方法很多。以钛铁矿(主要成分FeTiO3,钛酸亚铁)为主要原料冶炼金属钛,生产的工艺流程图如下,其中钛铁矿与浓硫酸发生反应的化学方程式为:
FeTiO3+2H2SO4=TiOSO4+FeSO4+2H2O

回答下列问题:
(1)钛铁矿和浓硫酸反应属于______________________ (选填“氧化还原反应”或“非氧化还原反应”)。
(2)上述生产流程中加入物质A的目的是防止Fe2+被氧化,物质A是________,上述制备TiO2的过程中,所得到的副产物和可回收利用的物质分别是__________、___________。
(3)反应TiCl4+2Mg=2MgCl2+Ti在Ar气氛中进行的理由是_______________。
(4)由二氧化钛制取四氯化钛所涉及的反应有:
TiO2 (s)+ 2Cl2 (g) +2C(s) =TiCl4(g) + 2CO(g) ΔH1 = -72 kJ•mol-1
TiO2(s) + 2Cl2 (g) =TiCl4(g) + O2 (g) ΔH2 =+38.8kJ•mol-1
C(s)+CO2(g)=2CO(g) ΔH3 =+282.8kJ•mol-1
①反应C(s)+CO2(g)=2CO(g)在高温下能够自发进行的原因是______________________。
②反应C(s)+O2(g)=CO2 (g)的ΔH=_______________。
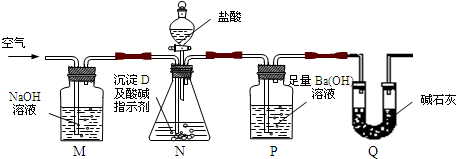
(5)研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2-CaO作电解质,利用下图所示装置获得金属钙,并以钙为还原剂,还原二氧化钛制备金属钛。①写出阳极所发生反应的电极反应式:________________________________。

②在制备金属钛前后,CaO的总量不变,其原因是(请结合化学用语解释) 。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年河北省高三上学期第二次月考化学试卷 题型:实验题
(12分)某学习小组利用下图所示装置进行“铁与水气反应”和其他实验(略去了夹持仪器)。
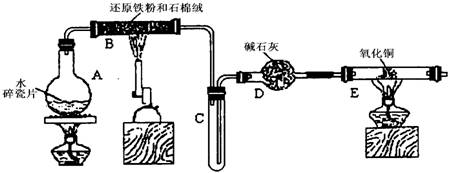
(1)为了安全,加热E以前必须进行的操作是____________________________。
(2) B中发生反应的化学方程式是 _______________。
(3)已知有反应:Cu2O+2H+ Cu+Cu2++H2O,则可用来检验反应后E中的红色固体中除Cu外是否含Cu2O,可用的试剂是________(填序号)
Cu+Cu2++H2O,则可用来检验反应后E中的红色固体中除Cu外是否含Cu2O,可用的试剂是________(填序号)
a.稀硝酸 b.稀硫酸 c.盐酸 d.浓硫酸
(4)在E后若再接二个盛碱石灰的干燥管(依次称为F和G),则还可用该装置测定水的组成。若反应后盛有药品的E的质量减轻了e g,F的质量增加了f g。水中元素的物质的量之比可表示为(不用化简)n(H):n(O)= ________:_______;若反应后E中除Cu外还含有另一种还原产物Cu2O,则该比值将___________ (选填“偏大”“偏小”或“无影响”)。
(5)某学生为了检验反应后固体的成分,反应前在E管中加入了氧化铜固体16g,反应后称量固体的质量变为13.6g,则13.6g的成分为:___________(若为混合物,需计算出各自的质量)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com