
 .
. .
.分析 (1)Ca是20号元素,钙原子核外电子数为20,有3个电子层,各层电子数为2、8、8、1,对于主族元素,电子层数=周期数,最外层电子数=族序数;
(2)先判断最活泼的非金属元素,再确定该化合物的化学式,根据电子式书写规则写出其的形成过程;根据晶体类型判断沸点高低;
(3)生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色,应为Fe(OH)2→Fe(OH)3的转化;
(4)钙与水反应生成氢氧化钙与氢气,根据n=$\frac{V}{Vm}$计算氢气的物质的量,根据电子转移守恒计算Ca的物质的量,根据氧化钙的质量分数计算氧化钙的质量,计算氧化钙的物质的量,氧化钙与水反应生成氢氧化钙,氢氧化钙与二氧化碳反应生成碳酸钙,根据钙元素守恒可知生成的n(CaCO3)=n(Ca)+n(CaO),再根据m=nM计算碳酸钙的质量.
解答 解:(1)Ca是20号元素,钙原子核外电子数为20,有3个电子层,各层电子数为2、8、8、1,原子结构示意图为 ,故答案为:
,故答案为:
(2)元素周期表中最活泼的非金属元素是F元素,与Ca形成化合物离子化合物D,所以D是CaF 2,氟化钙为离子化合物,阴阳离子需要标出所带电荷,用电子式表示其形成过程为: ;F与Si形成D的化合物E是SiF4,SiF4是共价化合物,所以D的沸点比E高.
;F与Si形成D的化合物E是SiF4,SiF4是共价化合物,所以D的沸点比E高.
故答案为:高; ;
;
(3)钙线试样溶于稀盐酸后,加入过量NaOH溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色M(OH)n,M为Fe元素,处于第四周期第VIII族,故答案为:第四周期,第Ⅷ族;
(4)224mlH2的物质的量为$\frac{0.224L}{22.4L/mol}$=0.01mol,钙与水反应生成氢氧化钙与氢气,根据电子转移守恒可知,Ca的物质的量为$\frac{0.01mol×2}{2}$=0.01mol,样品中CaO质量分数为3.5%,故氧化钙的质量为1.6g×3.5%=0.056g,故氧化钙的物质的量为$\frac{0.056g}{56g/mol}$=0.001mol,氧化钙与水反应生成氢氧化钙,氢氧化钙与二氧化碳反应生成碳酸钙,根据钙元素守恒可知生成的n(CaCO3)=n(Ca)+n(CaO)=0.01mol+0.001mol=0.011mol,碳酸钙的质量为0.011mol×100g/mol=1.1g,
故答案为:1.1.
点评 本题考查结构与位置关系、常用化学用语书写、氧化还原反应、化学计算等,题目综合性较大,难度中等,(4)中注意利用守恒进行计算.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应NH3(g)+HCl(g)═NH4Cl(s)在室温下可自发进行,则该反应的△H>0 | |
| B. | 电解法精炼铜时,以粗铜作阴极,纯铜作阳极 | |
| C. | CH3COOH 溶液加水稀释后,溶液中的$\frac{c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})}$值减小 | |
| D. | 增大反应物浓度可加快反应速率,因此用浓硫酸与铁反应能增大生成H2的速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 次氯酸的电子式  | B. | 钠离子的结构示意图 | ||
| C. | 硫原子的最外层电子排布式3s23p4 | D. | 二氧化硅的分子式 SiO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 8个中子的碳原子:12C | B. | HClO的结构式:H-Cl-O | ||
| C. | 镁离子的结构示意图: | D. | 15N的电子排布式:1s22s22p4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
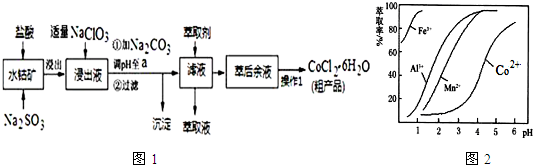
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com