
| A. | CH3CH═CH2和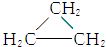 | B. | 乙炔和苯 | C. | 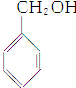 和 和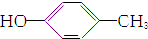 | D. | 乙酸和甲酸甲酯 |
分析 根据结构相似,组成相差n个CH2原子团的有机物,互为同系物;分子式相同,但结构不同的有机物,属于同分异构体,据此解答.
解答 解:A、CH3CH═CH2和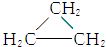 分子式相同均为C3H6,结构不同,属于同分异构体,故A不选;
分子式相同均为C3H6,结构不同,属于同分异构体,故A不选;
B、乙炔含有碳碳三键,属于炔烃,苯为芳香烃,两者分子式不同,结构不同,既不是同系物也不是同分异构体,故B选;
C、 和
和 分子式相同,均是C7H8O,结构不同,属于同分异构体,故C不选;
分子式相同,均是C7H8O,结构不同,属于同分异构体,故C不选;
D、乙酸和甲酸甲酯,分子式相同,均是C2H4O2,结构不同,属于同分异构体,故D不选,
故选B.
点评 本题考查有机物的官能团及同系物、同分异构体,注意能根据名称写出分子式或结构简式和概念的辨析,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | ①和③ | B. | ②和③ | C. | ①和② | D. | ②和④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在共价化合物中一定存在共价键 | |
| B. | 只存在共价键的物质一定是共价化合物 | |
| C. | 含有共价键的化合物一定是共价化合物 | |
| D. | 离子化合物中只含有离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验目的 | 实验操作 |
| A | 检验蔗糖水解产物中的葡萄糖 | 取1mL 20%蔗糖溶液,加入少量稀硫酸,水浴加热后取少量溶液于另一试管中,加入几滴新制Cu(OH)2,加热 |
| B | 除去乙烷中混有的少量乙烯 | 将混合气体通入足量酸性KMnO4溶液中 |
| C | 检验葡萄糖中含有醛基 | 向3mL 2%氨水溶液中加入几滴2%的硝酸银溶液,再加入1mL10%的葡萄糖溶液温水浴加热几分钟 |
| D | 验证蛋白质的盐析 | 向豆浆、鸡蛋清溶液中均滴加饱和硫酸铵溶液,振荡至出现沉淀,再向沉淀物中加入蒸馏水,不断振荡 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 反应过程中能量关系可用如图表示: | |
| B. | 若将该反应设计成原电池,锌为负极 | |
| C. | 若将该反应设计成原电池,正极可用石墨 | |
| D. | 若将其设计为原电池,当有32.5 g锌溶解时,正极放出的气体一定为11.2 L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲苯和乙苯 | B. | 乙烯和丁烯 | C. | 甲烷和丙烯 | D. | 乙炔和丁炔 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | v正(NH3)=3v逆(H2) | |
| B. | 1个N≡N键断裂的同时有6个N-H键断裂 | |
| C. | 反应体系压强不再变化 | |
| D. | 混合气体质量不再变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由长、短周期元素共同组成的元素族称为主族 (除零族外) | |
| B. | 同一元素不可能既表现金属性,又表现非金属性 | |
| C. | 短周期元素原子形成简单离子后,最外层电子都达到8电子稳定结构 | |
| D. | 互为同位素的不同核素,物理性质和化学性质都不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 浓度/mol.L-1 | NO | N2 | CO2 |
| 时间/min | |||
| 0 | 0.100 | 0 | 0 |
| 10 | 0.058 | 0.021 | 0.021 |
| 20 | 0.040 | 0.30 | 0.030 |
| 30 | 0.040 | 0.30 | 0.030 |
| 40 | 0.032 | 0.034 | 0.017 |
| 50 | 0.032 | 0.034 | 0.017 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com