
| A. | 若甲烧杯中溶液浓度为0.1 mol•L-1,则乙烧杯中溶液浓度大于0.01 mol•L-1 | |
| B. | 向甲烧杯中加入等体积pH=(14-a)的NaOH溶液后,溶液显碱性 | |
| C. | 两溶液中水电离出的OH-浓度:10C甲(OH-)<C乙(OH-) | |
| D. | 取等体积甲乙溶液分别与适量NaOH溶液完全中和,所得溶液的pH:甲>乙 |
分析 A、醋酸为弱电解质,浓度越小,电离度越小,pH=a的醋酸溶液中醋酸的电离度小于pH=(a+1)的醋酸溶液,据此判断;
B、由于氢氧化钠是强电解质,所以向甲烧杯中加入等体积pH=(14-a)的NaOH溶液后,醋酸过量,溶液呈酸性;
C、根据c(OH-)=$\frac{{k}_{w}}{c({H}^{+})}$判断;
D、醋酸为弱电解质,pH=a的醋酸溶液中醋酸的浓度大于pH=(a+1)的醋酸溶液的浓度的10倍,据此判断;
解答 解:A、醋酸为弱电解质,浓度越小,电离度越小,pH=a的醋酸溶液中醋酸的电离度小于pH=(a+1)的醋酸溶液,所以乙烧杯中溶液浓度小于0.01 mol•L-1,故A错误;
B、由于氢氧化钠是强电解质,所以向甲烧杯中加入等体积pH=(14-a)的NaOH溶液后,醋酸过量,溶液呈酸性,故B错误;
C、根据c(OH-)=$\frac{{k}_{w}}{c({H}^{+})}$可知,10C甲(OH-)=C乙(OH-),故C错误;
D、醋酸为弱电解质,pH=a的醋酸溶液中醋酸的浓度大于pH=(a+1)的醋酸溶液的浓度的10倍,所以取等体积甲乙溶液分别与适量NaOH溶液完全中和,所得溶液的pH:甲>乙,故D正确;
故选D.
点评 本题考查了弱电解质的电离,根据弱电解质的电离特点及影响弱电解质电离的因素来分析解答即可,注意等物质的量的一元酸中和氢氧化钠的能力与酸的强弱无关,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 1.12 | B. | 2.24 | C. | 3.36 | D. | 4.48 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业生产硫酸的过程中使用过量的氧气,以提高二氧化硫的转化率 | |
| B. | 合成氨工业中使用催化剂,以提高NH3的产量 | |
| C. | 红棕色的NO2加压后颜色先变深再变浅 | |
| D. | CO2(g)?CO2(aq)△H<0,降温增压可增大二氧化碳气体在水中的溶解度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在潮湿的环境中,铜容易发生析氢腐蚀形成铜绿 | |
| B. | 常温下,将pH=4的醋酸溶液稀释后,电离平衡右移,所有离子的浓度均降低 | |
| C. | 反应SiO2(s)3C(s)=SiC(s)+2CO(g)室温下不能自发进行,则该反应的△H<0 | |
| D. | 等体积、等物质的量浓度的NH3•H2O溶液与NH4Cl溶液混合后溶液呈碱性,说明NH3•H2O的电离程度大于NH${\;}_{4}^{+}$的水解程度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.3mol Na2O2与盐酸反应,转移的电子数为0.6NA | |
| B. | 2L 0.1mol/L Al2(SO4)3溶液中,Al3+的数目为0.4NA | |
| C. | 标准状况下,4.48L O2所含有的共用电子对数目为0.2NA | |
| D. | 在常温下,0.3mol NaHSO4固体中含有的离子数目为0.6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10 | B. | 20 | C. | 30 | D. | 40 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷与四氯化碳分子都是含有极性键的极性分子 | |
| B. | 甲烷与四氯化碳分子内的键角均为60° | |
| C. | 甲烷分子比四氯化碳稳定,因为C-H键键能比C-Cl键大 | |
| D. | 甲烷沸点低于四氯化碳,因为C-H键键长比C-Cl键短 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
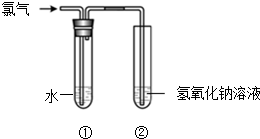 某同学用图所示装置制取氯水并进行相关实验.
某同学用图所示装置制取氯水并进行相关实验.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com