

 �Ƹ�С״Ԫ�������������ϵ�д�
�Ƹ�С״Ԫ�������������ϵ�д� ����һ������ܼƻ�ϵ�д�
����һ������ܼƻ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
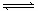 H++OH�� ��H��0������������ȷ���ǣ� ��
H++OH�� ��H��0������������ȷ���ǣ� ��| A����ˮ�м���ϡ��ˮ��ƽ�������ƶ���c(OH��)���� |
| B����ˮ�м������������������ƣ�c(H+)����Kw���� |
| C����ˮ�м�����������NaOH��ƽ�������ƶ���c(OH��)���� |
| D����ˮ���ȣ�Kw����c(H+)���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��Na+ | B��HCO3�� | C��Fe2+ | D��Cl�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������Һ��pH��10��pH(��)��11 |
| B������Һ��pH��7��pH(��)��11 |
| C������Һ�У�c(NH4+)+c(NH3��H2O)��c(Cl-) |
| D���ס�������Һ�зֱ����0.2 g NaOH��pH(��)��pH(��) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

| A��ԭ�����Һ�е�CO2-3��AlO��2�����ʵ���֮��Ϊ1:2 |
| B��V1��V2=l��5 |
| C��M��ʱ���ɵ�CO2Ϊ0.05mol |
| D��a���߱�ʾ�����ӷ���ʽΪ��AlO��2+H++H2O=Al(OH)3�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��404 KJ/mol | B��260 KJ/mol | C��230 KJ/mol | D��200 KJ/mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������ | B��С�� | C������ | D������ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����������PH=3�Ĵ�����Һ��PH=4�Ĵ�����Һ��ȫ�к�ʱ�����������Ƶ����ʵ�����ǰ���Ǻ��ߵ�10�� |
| B����0.1mol/L�İ�ˮ�����0.1mol/L��HCl��Һ����ӦPH=7ʱ������HCl��Һ�����С�ڰ�ˮ����� |
| C��pH��3.6��0.1mol/L HX��0.1mol/L NaX�Ļ����Һ�У�2c(Na+)=c(X��) |
| D��0.1mol��L��1��������Һ�У�c��OH����= c��H+��+ c��HS����+ c��H2S�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
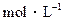 ��CH3COONa��Һ��0.1
��CH3COONa��Һ��0.1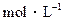 ��HCl��Һ�������Ϻ���Һ�������������ʵ���Ũ�ȵĹ�ϵ�У���ȷ����
��HCl��Һ�������Ϻ���Һ�������������ʵ���Ũ�ȵĹ�ϵ�У���ȷ����| A��[CH3COO��] = [Cl��] = [H+] > [CH3COOH] |
| B��[CH3COO��] = [[Cl��] > [CH3COO��] > [H+] |
| C��[CH3COO��] > [Cl��] > [H+] > [ CH3COOH] |
| D��[CH3COO��] > [Cl��] > [ CH3COOH] > [H+] |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com