
物质在水溶液中可能存在电离平衡、盐的水解平衡或沉淀溶解平衡,它们都可看作化学平衡的一种。请根据所学化学知识回答下列问题:
(1)A为0.1 mol·L-1的(NH4)2SO4溶液,在该溶液中离子浓度由大到小的顺序为
________________________________________________________________________。
(2)B为0.1 mol·L-1的NaHCO3溶液,NaHCO3在该溶液中存在的平衡有(用离子方程式表
示)________________________________________________________________________
________________________________________________________________________。
(3)C为0.1 mol·L-1的(NH4)2Fe(SO4)2溶液,与同浓度的(NH4)2SO4溶液中相比较______(填溶质的化学式)溶液中NH 的浓度更大,其原因是
的浓度更大,其原因是
________________________________________________________________________
________________________________________________________________________。
(4)D为含有足量AgCl固体的饱和溶液,AgCl在溶液中存在如下平衡:AgCl(s)
 Ag+(aq)+Cl-(aq)
Ag+(aq)+Cl-(aq)
在25 ℃时,AgCl的Ksp=1.8×10-10mol2·L-2。现将足量AgCl分别放入下列液体中:①100 mL蒸馏水 ②100 mL 0.3 mol·L-1 AgNO3溶液 ③100 mL 0.1 mol·L-1 MgCl2溶液充分搅拌后冷却到相同温度,Ag+浓度由大到小的顺序为______(填序号),此时溶液②中Cl-物质的量浓度为________。
答案 (1)c(NH )>c(SO
)>c(SO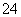 )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
(2)HCO

 H++CO
H++CO ;HCO
;HCO +H2O
+H2O
 H2CO3+OH-;H2O
H2CO3+OH-;H2O
 H+OH-
H+OH-
(3)(NH4)2Fe(SO4)2 Fe2+消解显酸性,对NH 的消解有抑制作用
的消解有抑制作用
(4)②①③ 6×10-10 mol·L-1
解析 (1)NH 消解显酸性且水解程度小,所以有:
消解显酸性且水解程度小,所以有:
c(NH )>c(SO
)>c(SO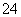 )>c(H+)>c(OH-)。
)>c(H+)>c(OH-)。
(2)NaHCO3溶液中存在三个平衡体系:
①HCO 的电离平衡:HCO
的电离平衡:HCO

 H++CO
H++CO ;②HCO
;②HCO 的消解平衡:HCO
的消解平衡:HCO +H2O
+H2O
 H2CO3+OH-;③H2O的电离平衡:H2O
H2CO3+OH-;③H2O的电离平衡:H2O
 H++OH-;
H++OH-;
(3)(NH4)2Fe(SO4)2溶液中,Fe2+消解产生的H+对NH 水解起抑制作用,NH
水解起抑制作用,NH 水解程度小,与同浓度的(NH4)2SO4溶液相比,前者NH
水解程度小,与同浓度的(NH4)2SO4溶液相比,前者NH 的浓度更大。
的浓度更大。
(4)①与③相比,③溶液中的Cl-使AgCl的溶解平衡逆向移动,c(Ag+)最小,②中溶液中的Ag+虽然使AgCl的溶解平衡逆向移动,但溶液中Ag+的浓度要比①、③中Ag+的浓度大的多。所以②中Ag+浓度最大。②中c(Cl-)=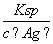 =
=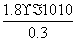 mol·L-1=6×10-10 mol·L-1。
mol·L-1=6×10-10 mol·L-1。


 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案科目:高中化学 来源: 题型:
X、Y、Z、M、W为五种短周期元素。X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15,X与Z可形成XZ2型分子;Y与M形成的气态化合物在标准状况下的密度为0.76 g/L; W的质子数是X、Y、Z、M四种元素质子数之和的1/2。下列说法正确的是
A.原子半径: W>Z>Y>X>M B.XZ2、X2M2、W2Z2均为直线形的共价化合物
C.由X元素形成的单质不一定是导体
D.由 X、Y、Z、M四种元素形成的化合物一定既含有离子键,又含有共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
1 mol某烃在氧气中充分燃烧,需要消耗氧气179.2 L(标准状况下)。它在光照的条件下与氯气反应能生成3种不同的一氯取代物。该烃的结构简式是( )

查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.95℃纯水的pH<7,说明加热可导致水呈酸性
B.pH=3的醋酸溶液,稀释至10倍后pH=4
C.0.2 mol·L-1的盐酸与等体积水混合后pH=1
D.pH=3的醋酸溶液与pH=11的氢氧化钠溶液等体积混合后pH=7
查看答案和解析>>
科目:高中化学 来源: 题型:
将0.2 mol·L-1 HA溶液与0.2 mol·L-1 NaOH溶液等体积混合,测得混合溶液中c(Na+)>c(A-),则(用“>”、“<”或“=”填写下列空白):
(1)混合溶液中c(HA)________c(A-);
(2)混合溶液中c(HA)+c(A-)________0.1 mol·L-1;
(3)混合溶液中由水电离出的c(OH-)______0.2 mol·L-1 HA溶液中由水电离出的c(H+);
(4)25℃时,如果取0.2 mol·L-1 HA溶液与0.1 mol·L-1 NaOH溶液等体积混合,测得混合溶液的pH<7,则HA的电离程度________NaA的水解程度。
查看答案和解析>>
科目:高中化学 来源: 题型:
偏二甲肼与N2O4 是常用的火箭推进剂,二者发生如下化学反应:
(CH3)2NNH2 (l )+2N2O4 (l )=2CO2 (g )+3N2 (g )+4H2O (l ) (Ⅰ)
(1)若将反应(Ⅰ)设计成原电池,则正极的电极反应式为
(酸性电解质)。
(2)火箭残骸中常现红棕色气体,原因为:N2O4 (g) 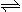 2NO2 (g) (Ⅱ)
2NO2 (g) (Ⅱ)
当温度升高时,气体颜色变深,则反应(Ⅱ)为 (填“吸热”或“放热”)反应。
(3)一定温度下,反应(Ⅱ)的焓变为ΔH。现将1 mol N2O4 充入一恒压密闭容器中,
下列示意图正确且能说明反应达到平衡状态的是________.
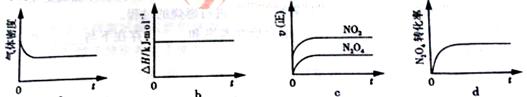
若在相同温度下,上述反应改在体积为1L的恒容密闭容器中进行,平衡常数________(填“增大”“不变”或“减小”),反应3s后NO2的物质的量为0.6mol,则0~3s内的平均反应速率v(N2O4)=________mol·L-1·s-1。
(4)NO2可用氨水吸收生成NH4NO3 。25℃时,将amol NH4NO3溶于水,溶液显酸性,原因是 (用离子方程式表示)。向该溶液滴加bL氨水后溶液呈中性,则滴加氨水的过程中的水的电离平衡将______(填“正向”“不”或
“逆向”)移动,所滴加氨水的浓度为_______mol·L-1。(NH3·H2O的电离平衡常数
Kb=2×10—5 mol·L-1)
查看答案和解析>>
科目:高中化学 来源: 题型:
.下列事实不能用平衡移动原理解释的是
|
|
|
| |||||||||||||
| A | B | C | D |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中不正确的是( )
A.组成蛋白质的氨基酸几乎都是α氨基酸
B.利用盐析可以分离和提纯蛋白质
C.DNA是生物体遗传信息的载体、蛋白质合成的模板
D.RNA主要存在于细胞核中,它根据DNA提供的信息控制体内蛋白质的合成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com