
| A. | 为防止铁生锈,在其表面涂一层防锈油漆 | |
| B. | 为防止火灾,在面粉厂、加油站等场所要严禁烟火 | |
| C. | 为加快H2O2的分解速率,把反应容器放到冷水中冷却 | |
| D. | 为加快KClO3的分解速率,加入MnO2 |
分析 A.防止铁生锈,在其表面涂一层防锈油漆,防止铁与潮湿的空气接触;
B.根据面粉厂、纺纱厂、加油站周围的空气中漂浮着可燃性的气体或粉尘,遇明火可能会发生爆炸进行解答;
C.温度越低反应速率越慢;
D.加入MnO2,对KClO3的分解起催化作用,所以加快化学反应速率.
解答 解:A.防止铁生锈,在其表面涂一层防锈油漆,阻止铁与潮湿的空气接触,故A正确;
B.面粉厂、纺纱厂、加油站周围的空气中漂浮着可燃性的气体或粉尘,遇明火可能会发生爆炸,所以面粉厂、纺纱厂、加油站均要严禁烟火,故B正确;
C.温度越低反应速率越慢,所以把反应容器放到冷水中冷却,反应速率减慢,故C错误;
D.加入MnO2,对KClO3的分解起催化作用,所以加快化学反应速率,故D正确;
故选C.
点评 本题考查了金属的防护、可燃物的性质、温度和催化剂对反应速率的影响,题目难度不大,侧重于基础知识的考查,注意把握影响反应速率的因素.


科目:高中化学 来源: 题型:选择题
| A. | KCl>NaCl>BaO>CaO | B. | NaCl>KCl>CaO>BaO | ||
| C. | CaO>BaO>NaCl>KCl | D. | CaO>BaO>KCl>NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铜与盐酸反应:H++OH-═H2O | |
| B. | 氯化钙溶液与碳酸钠溶液反应:Ca2++CO32-═CaCO3↓ | |
| C. | 硫酸溶液与碳酸钡反应:Ba2++SO42-═BaSO4↓ | |
| D. | 碳酸钙与稀盐酸反应:CO32-+2H+═H2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
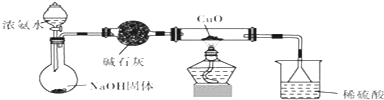
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
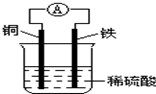
| A. | 铜棒逐渐溶解 | |
| B. | 该装置能将电能转化为化学能 | |
| C. | 负极反应式为Fe-2e-=Fe2+,发生还原反应 | |
| D. | 电子由铁棒通过导线流向铜棒 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 原子半径(10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 |
| 最高或最低化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
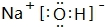 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
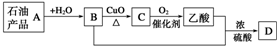
| A. | A能使酸性高锰酸钾溶液褪色 | B. | 可用B萃取碘水中的碘单质 | ||
| C. | B与乙酸发生了取代反应 | D. | D的结构简式为CH3COOCH2CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
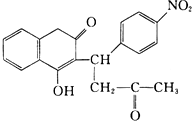
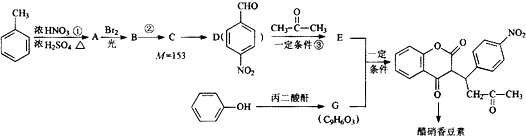
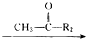 R1-CH═
R1-CH═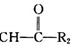 +H2O
+H2O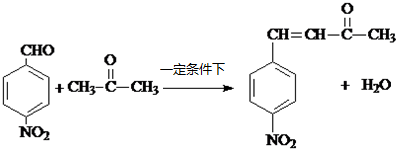 .
.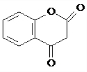 .
.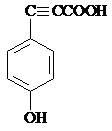 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由X、Y、Z三种元素形成的某种化合物,可能含有离子键 | |
| B. | 五种元素分别形成的单核离子中,M的离子半径最大 | |
| C. | W的氯化物是由一种10e-离子和一种18e-离子构成的 | |
| D. | X元素与Z所在主族的各元素形成的A2B型化合物中X2Z沸点最低 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com