
| A. | 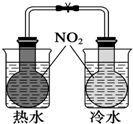 证明温度对平衡移动的影响 | B. | 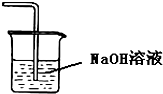 吸收HCl尾气 | ||
| C. | 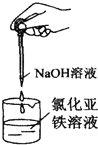 制备氢氧化亚铁 | D. | 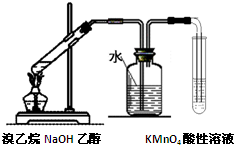 验证溴乙烷消去反应生成了乙烯 |
分析 A.2NO2?N2O4 △H<0,由颜色的变化可知平衡移动的方向;
B.HCl极易与NaOH溶液反应,可发生倒吸;
C.氢氧化亚铁易被氧化,制备时应隔绝空气;
D.溴乙烷与NaOH醇溶液发生消去反应生成乙烯,挥发的乙醇被水吸收,则试管中高锰酸钾可氧化乙烯.
解答 解:A.2NO2?N2O4 △H<0,由颜色的变化可知平衡移动的方向,则图中装置可证明温度对平衡移动的影响,故A正确;
B.HCl极易与NaOH溶液反应,可发生倒吸,则应加倒扣的漏斗吸收,故B错误;
C.氢氧化亚铁易被氧化,制备时应隔绝空气,则在液面下挤出NaOH溶液,故C错误;
D.溴乙烷与NaOH醇溶液发生消去反应生成乙烯,挥发的乙醇被水吸收,则试管中高锰酸钾可氧化乙烯,则高锰酸钾溶液褪色可验证溴乙烷消去反应生成了乙烯,故D正确;
故选AD.
点评 本题考查化学实验方案的评价,为高频考点,涉及化学平衡、物质制备、有机物的结构与性质等,把握物质的性质、反应原理及实验装置的作用等为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 碳酸钠可作胃酸的中和剂 | B. | SiO2可用于制造太阳能电池 | ||
| C. | 铁经常用作红色油漆和涂料 | D. | 生石灰用作食品抗氧化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 弱酸 | 醋酸 | 次氯酸 | 碳酸 | 亚硫酸 |
| 电离平衡常数 (25℃) | Ka=1.75ⅹ10-5 | Ka=2.98ⅹ10-8 | Ka1=4.3ⅹ10-7 Ka2=5.61ⅹ10-11 | Ka1=1.54ⅹ10-2 Ka2=1.02ⅹ10-7 |
| A. | 少量的CO2通入NaClO溶液中:CO2+H2O+2ClO-═CO32-+2HClO | |
| B. | 少量的SO2通入Na2CO3溶液中:SO2+H2O+2CO32-═SO32-+2HCO3- | |
| C. | 少量的SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-═CaSO3↓+2HClO | |
| D. | 相同浓度的NaHCO3溶液与NaHSO3溶液等体积混合:H++HCO3-═CO2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅥⅠA | 0 | |
| 2 | ⑥ | ⑦ | ⑪ | |||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤经过气化和液化等物理变化可以转化为清洁燃料 | |
| B. | “地沟油”禁止食用,但可以用来制肥皂 | |
| C. | 合成纤维、人造纤维及碳纤维都属于有机高分子材料 | |
| D. | 用聚氯乙烯代替聚乙烯作食品包装袋,有利于节约成本 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
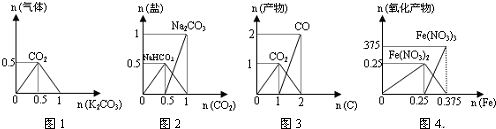
| A. | 图1:n (HCl)=1 mol,K2CO3逐步加入到HCl溶液中,在敞口容器中生成的气体 | |
| B. | 图2:n (NaOH)=1 mol,CO2逐步通入到NaOH溶液中反应生成的盐 | |
| C. | 图3:n (O2)=1 mol,高温下C和O2在密闭容器中的反应产物 | |
| D. | 图4:n (HNO3)=1 mol,Fe和稀HNO3反应生成的氧化产物(还原产物为NO) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com