
下列关于铜电极的叙述不正确的是( )
A.在镀件上镀铜时镀件作阴极
B.在镀件上镀铜时可用金属铜作阳极
C.用电解法精炼粗铜时粗铜作阳极
D.用电解法精炼粗铜时纯铜作阳极
 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:
在相同温度下,0.01 mol·L-1 NaOH溶液和0.01 mol·L-1的盐酸相比,下列说法正确的是( )
A.由水电离出的[H+]相等
B.由水电离出的[H+]都是1.0×10-12 mol·L-1
C.由水电离出的[OH-]都是0.01 mol·L-1
D.两者都促进了水的电离
查看答案和解析>>
科目:高中化学 来源: 题型:
现向含AgBr的饱和溶液中:
(1)加入固体AgNO3,则[Ag+]________(填“变大”、“变小”或“不变”,下同);
(2)加入更多的AgBr固体,则[Ag+]________;
(3)加入AgCl固体,则[Br-]________,[Ag+]________;
(4)加入Na2S固体,则[Br-]________,[Ag+]________。
查看答案和解析>>
科目:高中化学 来源: 题型:
用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,向所得的溶液中加入0.1 mol Cu(OH)2后恰好恢复到电解前的浓度和pH。则电解过程中转移的电子的物质的量为
( )
A.0.1 mol B.0.2 mol C.0.3 mol D.0.4 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
在50 mL 0.2 mol·L-1 CuSO4溶液中插入两个电极,通电电解(不考虑水分蒸发)。则:
(1)若两极均为铜片,试说明电解过程中CuSO4溶液的浓度________(填“增大”、“减小”或“不变”)。
(2)若阳极为纯锌,阴极为铜片,阳极反应式是________________________________________________________________________
________________________________________________________________________。
(3)若阳极为纯锌,阴极为铜片,如不考虑H+在阴极上放电,当电路中有0.04 mol e-通过时,阴极增重________g,阴极上的电极反应式是________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示,在一U形管中装入含有紫色石蕊的Na2SO4试液,通直流电,一段时间后U形管内会形成一个倒立的三色“彩虹”,从左到右颜色的顺序是( )
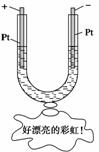
A.蓝、紫、红 B.红、蓝、紫 C.红、紫、蓝 D.紫、红、蓝
查看答案和解析>>
科目:高中化学 来源: 题型:
等物质的量浓度、等体积的氢氧化钠溶液和醋酸溶液完全反应后,溶液中有关离子浓度之间不存在的关系是( )
A.[H+][OH-]=KW
B.[Na+]>[CH3COO-]>[OH-]>[H+]
C.[Na+]=[CH3COO-]+[OH-]
D.[Na+]+[H+]=[CH3COO-]+[OH-]
查看答案和解析>>
科目:高中化学 来源: 题型:
某工厂采用电解法处理含铬废水,耐酸电解槽用铁板作阴、阳极,槽中盛放含铬废水,原理示意图如右图,下列说法不正确的是( )。
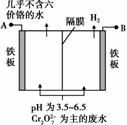
A.A接电源正极
B.阳极区溶液中发生的氧化还原反应为Cr2O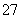 +6Fe2++14H+===2Cr3++6Fe3++7H2O
+6Fe2++14H+===2Cr3++6Fe3++7H2O
C.阴极区附近溶液pH降低
D.若不考虑气体的溶解,当收集到H2 13.44 L(标准状况)时,有0.1 mol Cr2O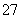 被还原
被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
美国海军海底战事中心与麻省理工大学共同研制成功了用于潜航器的镁-过氧化氢燃料电池系统。其工作原理如图所示。以下说法中 错误的是( )
错误的是( )

A.电池的负极反应为:Mg-2e-====Mg2+
B.电池工作时,H+向负极移动
C.电池工作一段时间后,溶液的pH增大
D.电池总反应式是:Mg+H2O2+2H+====Mg2++2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com