
【题目】R元素的一种原子可表示为:![]() ,则下列说法中正确的是
,则下列说法中正确的是
A.R元素的相对原子质量的近似整数值在数值上等于A
B.R元素的近似相对原子质量为A
C.R元素的近似相对原子质量为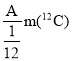 (其中m(
(其中m(![]() )表示一个碳-12原子的质量)
)表示一个碳-12原子的质量)
D.无法计算出R元素的近似相对原子质量
科目:高中化学 来源: 题型:
【题目】A~G都是有机化合物,它们的转化关系如图,请回答下列问题:
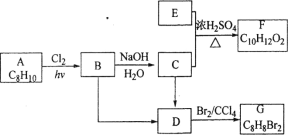
已知:RX+NaOH ![]() ROH+NaX
ROH+NaX
RCH2CH2X+NaOH ![]() RCH=CH2+NaX+H2O
RCH=CH2+NaX+H2O
(1)已知:6.0 g化合物E完全燃烧生成8.8 g CO2和3.6 g H2O;E的蒸气与氢气的相对密度为30,则E的分子式为___________。
(2)A为一取代芳烃,B中含有一个甲基。由B生成C的化学方程式为________________。
(3)由B生成D、由C生成D的反应条件分别是_________、__________。
(4)由A生成B、由D生成G的反应类型分别是__________、__________。
(5)F存在于栀子香油中,其结构简式为___________。
(6)在G的同分异构体中,苯环上一硝化的产物只有一种的共有 _____个,其中核磁共振氢谱有两组峰,且峰面积比为l:1的是______________(填结构简式)。
(7) 已知烯烃能发生如下的反应:
![]() RCHO+R’CHO
RCHO+R’CHO
请写出下列反应产物的结构简式:
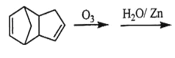 ________________________
________________________
(8) A是二聚环戊二烯(C10H12)的同分异构体,能使溴的四氯化碳溶液褪色,A经高锰酸钾酸性溶液加热氧化可以得到对苯二甲酸[提示:苯环的烷基(—CH3,—CH2R,—CHR2)或烯基侧链经酸性高锰酸钾溶液氧化得羧基,写出A所有可能的结构简式(不考虑立体异构):___________________________________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为甲烷晶体的晶胞结构,下列有关说法正确的是( )
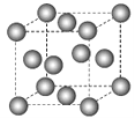
A.甲烷晶胞中的球体只代表一个碳原子
B.晶体中1个![]() 分子有12个紧邻的甲烷分子
分子有12个紧邻的甲烷分子
C.![]() 晶体熔化时需克服共价键
晶体熔化时需克服共价键
D.一个甲烷晶胞中含有8个![]() 分子
分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E五种元素,它们的核电荷数依次增大。已知:A失去一个电子后就成为一个质子;B有两个电子层,其最外层的电子数是次外层电子数的2倍;C的L层得2个电子后成为稳定结构;D是海水中含量第一位的金属元素;E的最外层电子比次外层电子少一个。请填写下列空格:
(1)A形成的单质的结构式为______; BC2的电子式_______________。
(2)D离子的结构示意图_________,D、E结合形成的化合物的电子式_____
(3)B、C、D三种元素可形成一种化合物,其化学式为_____,所含的化学键有____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用0.1mol·L-1的NaOH溶液分别滴定相同浓度的弱酸HX、HY的稀溶液,其滴定曲线如图所示。下列说法错误的是( )
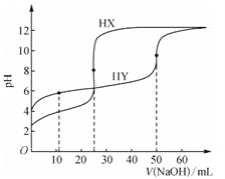
A.HX的酸性比HY的强B.滴定过程中,均可用酚酞作指示剂
C.室温下,Ka(HY)的数量级约为10-4 D.滴定前,HY的体积为HX的两倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)密度为1.10 g/mL、质量分数为20%的盐酸的物质的量浓度为__________ mol/L
(2)取此盐酸50 mL和足量的镁反应后,求:
①放出的H2在标准状况下的体积_______________。
②将生成的H2缓慢通过过量的灼热CuO,求理论上被还原出的铜的质量__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝、钛、钡(第2主族)等元素在能源、材料等领域应用广泛。回答下列问题:
⑴与钛同周期的所有副族元素的基态原子中,最外层电子数与基态钛原子相同的元素有________种。基态Ti2+的最外层电子排布式为________________。
⑵铝的逐级电离能数据为:I1=580 kJmol-1、I2=1820 kJmol-1、I3=2750 kJmol-1、I4=11600 kJmol-1。请分析数据规律,预测钡的逐级电离能的第一个数据“突跃”点出现在________之间(用I1、I2、I3等填空![]() 。
。
⑶已知第ⅡA族元素的碳酸盐MCO3热分解的主要过程是:M2+结合碳酸根离子中的氧离子。则CaCO3、BaCO3的分解温度较高的是________________(填化学式),理由是________________。
⑷催化剂M能催化乙烯、丙烯、苯乙烯等的聚合,其结构如图1所示。
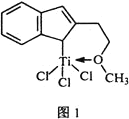
①M中,碳原子的杂化类型有________________。
②M中,不含________![]() 填标号
填标号![]() 。
。
A. π键 B. δ键 C. 配位键 D.氢键 E. 离子键
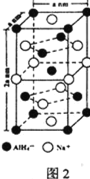
⑸氢化铝钠(NaAlH4)是一种新型轻质储氢材料,其晶胞结构如图2所示,为长方体。写出与AlH4-空间构型相同的一种分子_______________(填化学式)。NaAlH4晶体中,与AlH4-紧邻且等距的Na+有________个;NaAlH4晶体的密度为________ gcm-3(用含a、NA的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的类别和核心元素的化合价是研究物质性质的两个基本视角。请根据如图所示,回答下列问题:

(1)Y是形成酸雨的主要物质之一,它溶于水反应的化学方程式为_____;另一类硝酸型酸雨主要由人类活动产生的NOx造成的,写出NO2与水反应的化学方程式为______;酸雨的pH______(填范围)。
(2)Y能使品红溶液褪色,它与一种黄绿色气体等体积通入水中得到的溶液却几乎没有漂白性,反应的离子方程式为_______;Y也能使酸性高锰酸钾溶液褪色,写出该反应的离子方程式______,并用单线桥法标明电子转移的方向和数目,体现了Y的_____性。
(3)W的浓溶液与铜单质在加热条件下可以发生化学反应,反应的化学方程式为_____。
(4)现用98%的浓硫酸(ρ=1.84g/cm3)配制成浓度为0.5mol/L的稀硫酸500mL,回答下列问题:
①所需浓硫酸的体积为______mL。
②将浓硫酸沿烧杯内壁缓缓注入盛水的烧杯中,不断搅拌的目的是_____,若搅拌过程中有液体溅出,会导致最终所配溶液浓度_____(填“偏大”、“偏小”或“无影响”,下同)。
③在转入容量瓶前,烧杯中的液体应先_____,否则会使浓度_____。
(5)已知S的氧化性较弱,则硫粉与铜加热反应的化学方程式为_____。
(6)欲制备Na2S2O3(硫代硫酸钠),从氧化还原反应角度分析,合理的是_____(填序号)。
A.Na2S+S B.Na2SO3+S C.Na2SO3+Na2SO4 D.SO2+Na2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】毒重石的主要成分为BaCO3(含Ca2+、Mg2+、Fe3+等杂质)。实验室利用毒重石制备BaCl2·2H2O的流程如图:
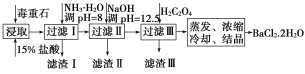
(1)毒重石用盐酸浸取前需充分研磨,目的是__。
(2)加入NH3·H2O调pH=8可除去__(填离子符号),滤渣Ⅱ中含__(填化学式)。加入H2C2O4时应避免过量,原因是__。
已知:Ksp(BaC2O4)=1.6×10-7,Ksp(CaC2O4)=2.3×10-9
Ca2+ | Mg2+ | Fe3+ | |
开始沉淀时的pH | 11.9 | 9.1 | 1.9 |
完全沉淀时的pH | 13.9 | 11.1 | 3.2 |
(3)利用间接酸碱滴定法可测定Ba2+的含量,实验分两步进行。
已知:2CrO42-+2H+=Cr2O72-+H2O
Ba2++CrO42-=BaCrO4↓
步骤Ⅰ:移取xmL一定浓度的Na2CrO4溶液于锥形瓶中,加入酸碱指示剂,用bmol·L-1盐酸标准液滴定至终点,测得滴加盐酸的体积为V0mL。
步骤Ⅱ:移取ymLBaCl2溶液于锥形瓶中,加入xmL与步骤Ⅰ相同浓度的Na2CrO4溶液,待Ba2+完全沉淀后,再加入酸碱指示剂,用bmol·L-1盐酸标准液滴定至终点,测得滴加盐酸的体积为V1mL。
滴加盐酸标准液时应使用酸式滴定管,“0”刻度位于滴定管的__(填“上方”或“下方”)。BaCl2溶液的浓度为__mol·L-1。若步骤Ⅱ中滴加盐酸时有少量待测液溅出,Ba2+浓度测量值将__(填“偏大”或“偏小”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com