

 .
. ,无机试剂任选,格式参照图.
,无机试剂任选,格式参照图. .
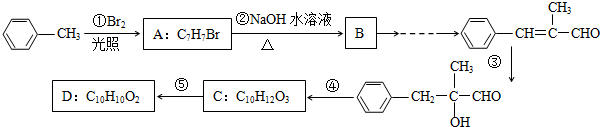
. 分析 根据题中各物质的转化关系,甲苯与溴在光照条件下发生取代反应生成A为 ,A碱性水解生成B为
,A碱性水解生成B为 ,B经过氧化生成苯甲醛,成苯甲醛与丙醛发生信息b中的反应可得
,B经过氧化生成苯甲醛,成苯甲醛与丙醛发生信息b中的反应可得 ,
, 与水加成得
与水加成得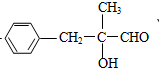 ,
, 发生氧化反应得C为
发生氧化反应得C为 ,C发生消去反应D
,C发生消去反应D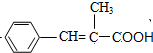 ,D能与碳酸氢钠反应生成二氧化碳,符合中物质的转化关系,据此答题.
,D能与碳酸氢钠反应生成二氧化碳,符合中物质的转化关系,据此答题.
解答 解:根据题中各物质的转化关系,甲苯与溴在光照条件下发生取代反应生成A为 ,A碱性水解生成B为
,A碱性水解生成B为 ,B经过氧化生成苯甲醛,成苯甲醛与丙醛发生信息b中的反应可得
,B经过氧化生成苯甲醛,成苯甲醛与丙醛发生信息b中的反应可得 ,
, 与水加成得
与水加成得 ,
, 发生氧化反应得C为
发生氧化反应得C为 ,C发生消去反应D
,C发生消去反应D ,D能与碳酸氢钠反应生成二氧化碳,符合中物质的转化关系,
,D能与碳酸氢钠反应生成二氧化碳,符合中物质的转化关系,
(1)C为 ,C中官能团的名称为 羟基、羧基,③的反应类型为加成反应,
,C中官能团的名称为 羟基、羧基,③的反应类型为加成反应,
故答案为:羟基、羧基;加成反应;
(2)反应⑤为醇的消去,所以⑤的反应条件为浓硫酸,加热,
故答案为:浓硫酸,加热;
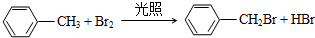
(3)反应①为甲苯与溴在光照条件下发生取代反应生成 ,反应的化学方程式为
,反应的化学方程式为  ,
,
故答案为: ;
;
(4)B经过氧化生成苯甲醛,成苯甲醛与丙醛发生信息b中的反应可得 ,合成路线为
,合成路线为 ,
,
故答案为: .
.
点评 本题考查有机物的推断与合成,熟记有机物性质和反应条件并能灵活运用是解答本题的关键,再结合转化关系进行推断,需要学生熟悉掌握官能团的性质与演变,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 原子半径:r(W)>r(Z)>r(Y)>r(X) | |
| B. | 元素Y分别与元素Z、W形成的化合物中化学键类型相同 | |
| C. | 元素Z和元素Y、W均能形成离子化合物 | |
| D. | 四种元素形成的氢化物中,沸点最高的是元素Y的氢化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
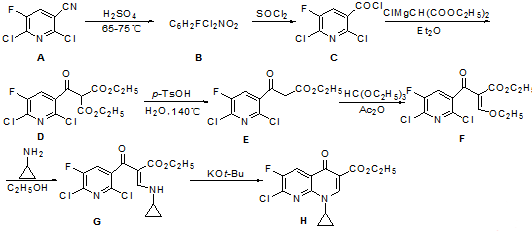
 .由C→D的反应类型是取代反应.
.由C→D的反应类型是取代反应. (其中一种).
(其中一种). 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:查看答案和解析>>
科目:高中化学 来源: 题型:推断题
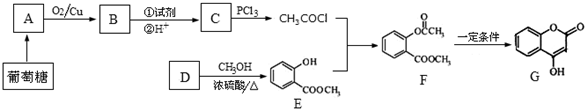
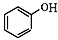 +NaOH→
+NaOH→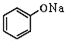 +H2O
+H2O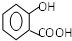 .
.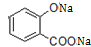 、CH3COONa、CH3OH.
、CH3COONa、CH3OH.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 产品标准 | GB5461 |
| 产品等级 | 一级 |
| 配 料 | 食盐、碘酸钾、抗结剂 |
| 碘含量(以I计) | 20~50mg/kg |
| 分装时期 | |
| 分装企业 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
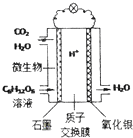 最近科学家研制的一种新型“微生物电池”可以将污水中的有机物转化为H2O和CO2,同时产生电能,其原理示意如图.下列有关该电池的说法正确的是( )
最近科学家研制的一种新型“微生物电池”可以将污水中的有机物转化为H2O和CO2,同时产生电能,其原理示意如图.下列有关该电池的说法正确的是( )| A. | 氧化银电极上反应为:Ag2O+2e-═2Ag+O2- | |
| B. | 石墨电极上反应为:C6H12O6+6H2O+24e-═6CO2↑+24H+ | |
| C. | 每转移4mol电子,氧化银电极产生22.4LCO2气体(标准状况) | |
| D. | 每30g C6H12O6参与反应,有4mo1 H+经质子交换膜进入正极区 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 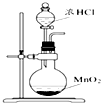 可用装置甲制取氯气 | |
| B. | 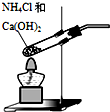 可用装置乙制取氨气 | |
| C. | 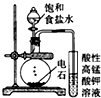 可用装置丙制取并检验乙炔(乙炔中含有H2S、PH3) | |
| D. | 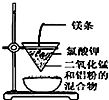 可用装置丁制得金属锰 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
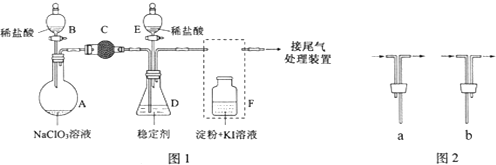
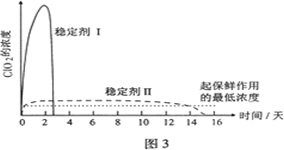
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 CH3COOCH2CH3+H2O,酯化(或取代)反应.
CH3COOCH2CH3+H2O,酯化(或取代)反应.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com