
 ČēĶ¼ŹĒÓĆøÉŌļ“æ¾»µÄCl2ÓėCu·Ū·“Ó¦Ą“ÖĘČ”ĪŽĖ®ĀČ»ÆĶµÄŹµŃé×°ÖĆĶ¼£¬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
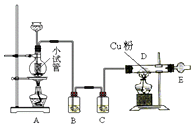
ČēĶ¼ŹĒÓĆøÉŌļ“æ¾»µÄCl2ÓėCu·Ū·“Ó¦Ą“ÖĘČ”ĪŽĖ®ĀČ»ÆĶµÄŹµŃé×°ÖĆĶ¼£¬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ·ÖĪö £Ø1£©Š”ŹŌ¹ÜÄŚŅŗĢåĘšŅŗ·ā×÷ÓĆ£»ÉÕĘæÄŚ¶žŃõ»ÆĆĢŗĶÅØŃĪĖį¼ÓČČ·“Ӧɜ³ÉĀČ»ÆĆĢ”¢ĀČĘųŗĶĖ®£»
£Ø2£©ÅØŃĪĖį¾ßÓŠ»Ó·¢ŠŌ£¬ÖʱøµÄĀČĘųÖŠŗ¬ÓŠĀČ»ÆĒāŗĶĖ®ÕōĘų£¬ŅĄ¾ŻĀČ»ÆĒāŅ×ČÜÓŚĖ®£¬ĀČĘųŌŚ±„ŗĶŹ³ŃĪĖ®ÖŠČܽā¶Č²»“óµÄŠŌÖŹŃ”Ōń³żŌÓŹŌ¼Į£¬ÅØĮņĖį¾ßÓŠĪüĖ®ŠŌ£¬æÉŅŌøÉŌļĀČĘų£»
£Ø3£©ĶÓėĀČĘųŌŚ¼ÓČČĢõ¼žĻĀ·“Ӧɜ³ÉĀČ»ÆĶ£»
£Ø4£©¼īŹÆ»ŅÓŠøÉŌļĘųĢåŗĶĪüŹÕCl2µÄ×÷ÓĆ£®
½ā“š ½ā£ŗ£Ø1£©³¤¾±Ā©¶·Ć»ÓŠ»īČū£¬ĒŅĀČĘųÓŠ¶¾£¬ĪŖ·ĄÖ¹ĀČĘų“Ó³¤¾±Ā©¶·ŅŻ³ö£¬²ÉÓĆŅŗ·āµÄ·½·Ø£¬ĖłŅŌŠ”ŹŌ¹ÜÓŠŅŗ·āµÄ×÷ÓĆ£»¼ÓČČĢõ¼žĻĀ£¬¶žŃõ»ÆĆĢŗĶÅØŃĪĖį·“Ӧɜ³ÉĀČ»ÆĆĢ”¢ĀČĘųŗĶĖ®£¬Ąė×Ó·“Ó¦·½³ĢŹ½ĪŖ£ŗMnO2+4H++2Cl-$\frac{\underline{\;\;”÷\;\;}}{\;}$Mn2++Cl2”ü+2H2O£¬
¹Ź“š°øĪŖ£ŗŅŗ·ā£Ø·ĄÖ¹Cl2“Ó³¤¾±Ā©¶·ÖŠŅŻ³ö£©£»MnO2+4H++2Cl-$\frac{\underline{\;\;”÷\;\;}}{\;}$Mn2++Cl2”ü+2H2O£»
£Ø2£©ÅØŃĪĖįÓŠ»Ó·¢ŠŌ£¬ĖłŅŌÖĘČ”µÄĀČĘųÖŠŗ¬ÓŠĀČ»ÆĒāĘųĢ壬ĀČ»ÆĒā¼«Ņ×ČÜÓŚĖ®£¬±„ŗĶŹ³ŃĪĖ®ÖŠŗ¬ÓŠĀČĄė×Ó£¬ÄÜŅÖÖĘĀČĘųµÄČܽā£¬ĖłŅŌ×°ÖĆBÓ¦øĆŃ”ÓƱ„ŗĶŹ³ŃĪĖ®£» ĀČĘųÄÜŗĶ¼ī·“Ó¦£¬ĒŅÅØĮņĖįÓŠĪüĖ®ŠŌ£¬ĖłŅŌŃ”ÓĆÅØH2SO4×÷øÉŌļ¼Į£¬
¹Ź“š°øĪŖ£ŗ±„ŗĶŹ³ŃĪĖ®£»³żČ„ĀČĘųÖŠµÄĀČ»ÆĒā£»ÅØĮņĖį£»øÉŌļĀČĘų£»
£Ø3£©²£Į§¹ÜDÖŠ·¢Éś·“Ó¦ĪŖĶÓėĀČĘųŌŚ¼ÓČČĢõ¼žĻĀ·“Ӧɜ³ÉĀČ»ÆĶ£¬·½³ĢŹ½£ŗCu+Cl2$\frac{\underline{\;¼ÓČČ\;}}{\;}$CuCl2£¬
¹Ź“š°øĪŖ£ŗCu+Cl2$\frac{\underline{\;¼ÓČČ\;}}{\;}$CuCl2£»
£Ø4£©ĀČĘųÓŠ¶¾£¬ĖłŅŌĪ²Ęų²»ÄÜÖ±½ÓÅÅæÕ£¬Ó¦øĆŃ”ÓĆ¼īŠŌĪļÖŹĪüŹÕ£»æÕĘųÖŠŗ¬ÓŠĖ®ÕōĘų£¬ĪŖµĆµ½½ĻøÉŌļµÄĀČ»ÆĶ£¬Ó¦øĆŌŚĀČĘųŗĶĶµÄ·“Ó¦“¦¼ÓŅ»øöøÉŌļ×°ÖĆ£¬¶žÕß×÷ÓĆ¼ę±ø£¬ĖłŅŌ¼īŹÆ»ŅµÄ×÷ÓĆŹĒĪüŹÕĪ“·“Ó¦ĶźµÄCl2£¬·ĄÖ¹æÕĘųÖŠµÄĖ®ÕōĘų½ųČė·“ӦװÖĆ£¬
¹Ź“š°øĪŖ£ŗĪüŹÕĪ“·“Ó¦ĶźµÄCl2£¬·ĄÖ¹æÕĘųÖŠµÄĖ®ÕōĘų½ųČė·“ӦװÖĆ£®
µćĘĄ ±¾Ģāæ¼²éĮĖĀČ»ÆĶµÄÖʱøŹµŃ飬ŅŖøł¾ŻŹµŃéÄæµÄєȔŹµŃé×°ÖĆ”¢ŹµŃéŅ©Ę·£¬ŹĒѧĻ°µÄÄŃµć£¬Ņ²ŹĒøßæ¼µÄČČµć£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
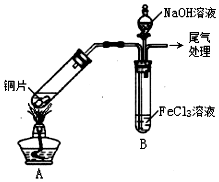 ij»ÆѧŠĖȤŠ”×éĢ½¾æSO2ÓėFeCl3ČÜŅŗµÄ·“Ó¦£¬ĖłÓĆ×°ÖĆČēĶ¼ĖłŹ¾£Ø¼Š³ÖŅĒĘ÷ŅŃĀŌČ„£©
ij»ÆѧŠĖȤŠ”×éĢ½¾æSO2ÓėFeCl3ČÜŅŗµÄ·“Ó¦£¬ĖłÓĆ×°ÖĆČēĶ¼ĖłŹ¾£Ø¼Š³ÖŅĒĘ÷ŅŃĀŌČ„£©²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓÉ”°C£Øs£¬ŹÆÄ«£©-”śC£Øs£¬½šøÕŹÆ£©”÷H=+119 kJ•mol-1”±æÉÖŖ½šøÕŹÆ±ČŹÆÄ«ĪČ¶Ø | |
| B£® | ŌŚ101 kPaŹ±£¬2 g H2ĶźČ«Č¼ÉÕÉś³ÉŅŗĢ¬Ė®£¬·Å³ö285.8 kJČČĮ棬ŌņĒāĘųČ¼ÉÕµÄČČ»Æѧ·½³ĢŹ½±ķŹ¾ĪŖ£ŗ2H2£Øg£©+O2£Øg£©ØT2H2O£Øl£©”÷H=+285.8 kJ•mol-1 | |
| C£® | ŌŚ101 kPaŹ±£¬1 molĢ¼Č¼ÉÕĖł·Å³öµÄČČĮæĪŖĢ¼µÄČ¼ÉÕČČ | |
| D£® | µČĮæµÄĮņÕōĘųŗĶĮņ¹ĢĢå·Ö±šĶźČ«Č¼ÉÕ£¬Ē°Õ߷ųöµÄČČĮæ¶ą |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | H2£Øg£©µÄČ¼ÉÕČČĪŖ571.6 kJ•mol-1 | |
| B£® | Ķ¬ÖŹĮæµÄH2£Øg£©ŗĶCH3OH£Øl£©ĶźČ«Č¼ÉÕ£¬H2£Øg£©Č¼ÉշųöµÄČČĮæ¶ą | |
| C£® | H2SO4£Øaq£©+Ba£ØOH£©2£Øaq£©ØTBaSO4£Øs£©+H2O£Øl£©”÷H=-57.3 kJ•mol-1 | |
| D£® | 3H2£Øg£©+CO2£Øg£©ØTCH3OH£Øl£©+H2O£Øl£©”÷H=+135.9 kJ•mol-1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
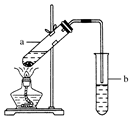 ŹµŃéŹŅ³£ÓĆČēĶ¼ĖłŹ¾×°ÖĆÖĘȔɣĮæŅŅĖįŅŅõ„£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
ŹµŃéŹŅ³£ÓĆČēĶ¼ĖłŹ¾×°ÖĆÖĘȔɣĮæŅŅĖįŅŅõ„£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 20% | B£® | 25% | C£® | 30% | D£® | 75% |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³£ĪĀĻĀ£¬°±Ė®ÓėĀČ»Æļ§µÄpH=7µÄ»ģŗĻČÜŅŗÖŠ£ŗc£ØCl-£©£¾c£ØNH4+£© | |
| B£® | ³£ĪĀĻĀ£¬ŌŚpH=11µÄČÜŅŗÖŠ£¬Ė®µēĄė³öµÄc£ØOH-£©Ņ»¶ØµČÓŚ10-3mol/L | |
| C£® | ČōĒæĖį”¢Ēæ¼īÖŠŗĶŗóČÜŅŗµÄpH=7£¬ŌņÖŠŗĶÖ®Ē°Ėį”¢¼īµÄpHÖ®ŗĶŅ»¶ØµČÓŚ14 | |
| D£® | ½«ĪļÖŹµÄĮæÅضČŗĶĢå»ż¶¼ĻąĶ¬µÄŅ»ŌŖĖįHAÓėŅ»ŌŖ¼īBOH»ģŗĻŗó£¬ČÜŅŗ³ŹÖŠŠŌ£¬Ōņ·“Ó¦ŗóČÜŅŗÖŠc£ØH+£©=$\sqrt{Kw}$ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NH3 | B£® | NH4NO3 | C£® | SiO2 | D£® | HNO3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | æÉÓĆäåµÄĖÄĀČ»ÆĢ¼ČÜŅŗĒų·ÖÖ±ĮóĘūÓĶŗĶĮŃ»ÆĘūÓĶ | |
| B£® | µ°°×ÖŹČÜŅŗÖŠ¼ÓČėÅصÄĮņĖįļ§ČÜŅŗ»įÓŠµ°°×ÖŹĪö³ö | |
| C£® | ¼×Ķ锢±½”¢ŅŅ“¼”¢ŅŅĖįŗĶõ„Ąą¶¼æÉŅŌ·¢ÉśČ”“ś·“Ó¦ | |
| D£® | Ļą¶Ō·Ö×ÓÖŹĮæĻą½üµÄ“¼ŗĶĶéĢž£¬ĶéĢžµÄ·ŠµćŌ¶Ō¶øßÓŚ“¼ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com