
某无色透明酸性溶液,可能含有K+、Mg2+、Al3+、Cu2+、NH4+、Cl﹣、SO42﹣、NO3﹣中的几种,取该溶液三等份分别进行实验①加入少量Zn产生H2,②逐滴加人NaOH溶液,其加入量和沉淀生成量关系如图所示,③加入0.1mol/LBaCl2溶液至5ml时不再产生白色沉淀,取上层清液加入足量AgNO3溶液,得到0.287g沉淀,由此推知原溶液中( )
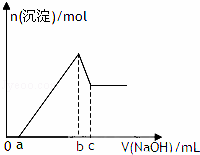
|
| A. | 一定没有Cu2+、NO3﹣、Cl﹣ | B. | 可能有K+、NH4+、NO3﹣、SO42﹣ |
|
| C. | 不能确定是否含有K+、NO3﹣ | D. | 一定有Mg2+、Al3+、Cl﹣、SO42﹣ |
| 常见阳离子的检验;常见阴离子的检验. | |
| 专题: | 物质检验鉴别题. |
| 分析: | 某无色透明酸性溶液,一定不含Cu2+,①加入少量Zn产生H2,证明含H+,②逐滴加人NaOH溶液,其加入量和沉淀生成量关系如图所示,则沉淀显示先是增大,后接着减小,则一定含有Mg2+、Al3+,一定不含有NH4+,③加入0.1mol/LBaCl2溶液至5ml时不再产生白色沉淀,一定含有SO42﹣,硫酸根离子和钡离子的物质的量是相等的,即为0.1mol/×0.005L=0.0005mol,氯化钡中氯离子的物质的量是0.001mol,取上层清液加入足量AgNO3溶液,得到0.287g沉淀,则AgCl的物质的量是0.002mol,所以原溶液含有氯离子是0.001mol,根据电荷守恒可以确定硝酸根离子是否存在. |
| 解答: | 解;解:某无色透明酸性溶液,一定不含Cu2+,①加入少量Zn产生H2,证明含H+,②逐滴加人NaOH溶液,其加入量和沉淀生成量关系如图所示,则沉淀显示先是增大,后接着减小,则一定含有Mg2+、Al3+,一定不含有NH4+,③加入0.1mol/LBaCl2溶液至5ml时不再产生白色沉淀,一定含有SO42﹣,硫酸根离子和钡离子的物质的量是相等的,即为0.1mol/×0.005L=0.0005mol,氯化钡中氯离子的物质的量是0.001mol,取上层清液加入足量AgNO3溶液,得到0.287g沉淀,则AgCl的物质的量是0.002mol,所以原溶液含有氯离子是0.001mol,不能确定硝酸根离子是否存在. 综上知道:溶液中一定存在的离子有:Mg2+、Al3+、Cl﹣、SO42﹣,一定不存在的是Cu2+、NH4+,其余的离子无法判断. 故选D. |
| 点评: | 本题考查了常见阴阳离子的检验,题目难度中等,注意掌握常见的离子之间的反应现象及检验方法,能够根据反应现象判断溶液中存在的离子和不能存在的离子. |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
在一定条件下RO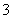 与R-发生如下反应:RO
与R-发生如下反应:RO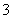 +5R-+6H+===3R2+3H2O,下列关于R的叙述中正确的是( )
+5R-+6H+===3R2+3H2O,下列关于R的叙述中正确的是( )
A.R的最外层电子数为5
B.R的氢化物的水溶液属于强酸
C.RO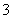 中的R只能被还原
中的R只能被还原
D.R2在常温常压下一定是气体
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关说法体现了化学与生产、生活、社会的密切关系。其中不正确的是
A.绚丽缤纷的烟花中添加了含钾、钠、钙、铜等金属元素的化合物
B.为防止中秋月饼等富脂食品氧化变质,常在包装袋中放入生石灰
C.停车场安装催化光反应设施,可使汽车尾气中的CO和NOX反应生成无毒气体
D.氮化硅陶瓷、氧化铝陶瓷、光导纤维等属于新型无机非金属材料
查看答案和解析>>
科目:高中化学 来源: 题型:
某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl。下列说法正确的是
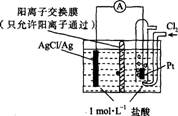
A.正极反应为AgCl+e-═Ag+Cl-
B.放电时,交换膜右侧溶液中有大量白色沉淀生成
C.若用NaCl溶液代替盐酸,则电池总反应随之改变
D.当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.02 mol离子
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子在给定的条件下能大量共存的是( )
|
| A. | 饱和氯水中:Cl﹣、NO3﹣、Na+、SO32﹣ |
|
| B. | 常温下, |
|
| C. | 0.1 mol/L的NaOH溶液中:K+、AlO2﹣、SO42﹣、CO32﹣ |
|
| D. | 在PH=7的溶液中:Fe3+、Na+、Br﹣、Cl﹣ |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于氯水的说法正确的是( )
|
| A. | 向氯水中通入少量二氧化硫,氯水的漂白性增强 |
|
| B. | 氯水中加入NaCl固体,对溶液的pH无影响 |
|
| C. | 常温下,pH=2的氯水中:c(Cl﹣)+c(ClO﹣)+c(OH﹣)=0.01mol/L |
|
| D. | 向氯水中滴加少量NaHCO3溶液的离子反应方程式为:Cl2+2HCO3﹣═2CO2↑+Cl﹣+ClO﹣+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
有一稀硫酸和稀硝酸的混合酸,其中H2SO4和HNO3的物质的量浓度分别是4mol/L和2mol/L,取10mL此混合酸,向其中加入过量的铁粉,待反应结束后,可产生标准状况下的混合气体体积为(设反应中HNO3被还原成NO)( )
|
| A. | 0.448L | B. | 0.672L | C. | 0.896L | D. | 0.224L |
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上制备纯硅反应的热化学方程式如下:SiCl4(g)+2H2(g)=Si(s)+4HCl(g);△H=+QkJ/mol(Q>0)某温度、压强下,将一定量反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述正确的是( )
|
| A. | 反应过程中,若增大压强能提高SiCl4的转化率 |
|
| B. | 若反应开始时SiCl4为1 mol,则达平衡时,吸收热量为Q kJ |
|
| C. | 反应至4 min时,若HCl浓度为0.12 mol/L,则H2的反应速率为0.03 mol/(L•min) |
|
| D. | 当反应吸收热量为0.025Q kJ时,生成的HCl通入100 mL 1 mol/L的NaOH溶液恰好反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质。以下叙述正确的是( )
A.植物油不能使溴水褪色 B.淀粉水解的最终产物是葡萄糖
C.葡萄糖、蔗糖都能水解 D.蛋白质溶液中滴加硝酸汞溶液后可发生盐析
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com