
| A. | 1:6 | B. | 6:1 | C. | 1:5 | D. | 5:1 |
分析 KClO3+6HCl=KCl+3Cl2↑+3H2O中,Cl元素的化合价由+5价降低为0,Cl元素的化合价由-1价升高为0,失去电子被氧化,得到电子被还原,以此计算.
解答 解:KClO3+6HCl=KCl+3Cl2↑+3H2O中,Cl元素的化合价由+5价降低为0,Cl元素的化合价由-1价升高为0,失去电子被氧化,得到电子被还原,由反应可知,5molHCl被氧化与1molKClO3被还原时,转移电子相同均为5mol,该反应中只有Cl原子被氧化、被还原,则该反应中被氧化与被还原的原子数之比为5:1,
故选D.
点评 本题考查氧化还原反应及计算,为高频考点,把握反应中元素的化合价变化、电子及原子守恒为解答的关键,侧重分析与计算能力的考查,注意化合价变化的判断及应用,题目难度不大.


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6种 | B. | 10种 | C. | 11种 | D. | 12种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
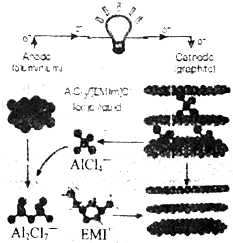 2015年4月,由中美科学家共同完成的“快速充放电铝离子电池”,具有高效耐用、可超快充电、可燃性低、成本低等特点.该电池以金属铝作为负极,三维结构的泡沫石墨材料为正极,AlCl4-可在其中或在脱嵌,由有机离子 (EMI+不参与反应)Al2Cl7-和AlCl4-组成的离子液体做电解质溶液,该电池放电时的原理如图所示,下列说法正确的是( )
2015年4月,由中美科学家共同完成的“快速充放电铝离子电池”,具有高效耐用、可超快充电、可燃性低、成本低等特点.该电池以金属铝作为负极,三维结构的泡沫石墨材料为正极,AlCl4-可在其中或在脱嵌,由有机离子 (EMI+不参与反应)Al2Cl7-和AlCl4-组成的离子液体做电解质溶液,该电池放电时的原理如图所示,下列说法正确的是( )| A. | 放电时,负极的电极反应式:Al-3e-+7AlCl4-═Al2C17- | |
| B. | 充电过程中,AlCl4-脱嵌并从阴极向阳极迁移 | |
| C. | 充电过程中阳极的电极反应式为:Cn+AlCl4--e-═Cn,其中C的化合价升高 | |
| D. | 该离子液体也可用于钢制品上电镀铝,但阴极材料要换成镀件 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 因为SO2有漂白性,所以它能使品红溶液、溴水褪色 | |
| B. | SO2和Cl2都有漂白作用,将两种气体同时作用于湿润的有色布条,漂白效果更好 | |
| C. | 在有些反应中显示氧化性,在有些反应中显示还原性 | |
| D. | 将SO2气体通入装有FeCl3溶液的试管里,黄色逐渐褪去 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 油脂水解可得到氨基酸和甘油 | |
| B. | 淀粉和纤维素水解最终产物都是葡萄糖 | |
| C. | 蛋白质水解的最终产物是氨基酸,某些蛋白质可用硝酸来检验 | |
| D. | 葡萄糖可用新制的氢氧化铜来检验 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 淀粉、纤维素、油脂都属于高分子化合物 | |
| B. | 能发生酯化反应的酸不一定都是羧酸 | |
| C. | 天然蛋白蛋水解的最终产物是一种氨基酸,这种氨基酸有两性 | |
| D. | 油脂水解得到的醇是丙三醇 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com