
 甲酸乙酯,
甲酸乙酯, .
.
分析 (1)①酯类物质名称为形成酯的酸和醇命名为某酸某酯;
②二烯烃的命名中选取含有2个碳碳双键的碳链为主链,距离碳碳双键最近的一端命名为1号碳,据此解答即可;
(2)麻黄素的结构简式判断其分子中含有的官能团名称.
解答 解:(1)① 是甲酸和乙醇反应生成的酯,名称为甲酸乙酯,
是甲酸和乙醇反应生成的酯,名称为甲酸乙酯,
故答案为:甲酸乙酯;
②2,5-二甲基-2,4-己二烯,主链为2,4-己二烯,在2号C、5号C上都含有一个甲基,编号从距离碳碳双键最近的一端开始,该有机物结构简式为: ,
,
故答案为: ;
;
(2)麻黄素 中含氧官能团为羟基,可看成醇类物质,
中含氧官能团为羟基,可看成醇类物质,
故答案为:羟基;醇.
点评 本题考查了命名方法的应用、有机物结构简式的书写、有机物的官能团,该题注重了基础性试题的考查,侧重对学生基础知识的检验和训练,有利于培养学生的规范答题能力,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 合成纤维、人造纤维及碳纤维都属于有机高分子材料 | |
| B. | 煤经过气化和液化等物理变化可转化为清洁燃料 | |
| C. | 利用粮食酿酒经过了淀粉→葡萄糖→乙醇的化学变化过程 | |
| D. | 偏二甲基肼[NH2N(CH3)2]是火箭动力液体燃料,它是一种氨基酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钠固体 | B. | 水 | ||
| C. | 硫酸钾固体 | D. | 滴加少量CuSO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素符号 | 元素性质与原子(或分子)结构 |
| T | 最外层电子数是次外层电子数的3倍 |
| X | 常温下单质为双原子分子,分子中含有3对共用电子对 |
| Y | M层比K层少1个电子 |
| Z | 第3周期元素的简单离子中半径最小 |

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
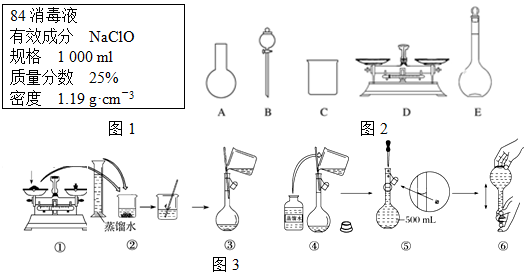
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 能源与材料、信息被称为现代社会发展的三大支柱,化学与能源有着密切联系.
能源与材料、信息被称为现代社会发展的三大支柱,化学与能源有着密切联系.| 化学键 | H-H | Cl-Cl | H-Cl |
| 键能 | 436 | 243 | 431 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com