
| A. | 电解质与非电解质本质区别是在水溶液或熔化状态下能否电离 | |
| B. | 纯碱、烧碱均属于碱 | |
| C. | 电离时能产生H+的化合物,一定是酸 | |
| D. | 非金属氧化物一定是酸性氧化物 |
分析 A.电解质能导电的原因是在水溶液或熔融状态下自身能电离出自由移动的离子;
B.纯碱是碳酸钠属于盐;
C.水溶液中电离出的阳离子全部是氢离子的化合物为酸;
D.酸性氧化物是能与碱生成盐和水的反应,一般是非金属氧化物.
解答 解:A.依据化合物在水溶液或熔融状态下能否导电对化合物分类,能够导电的化合物为电解质,都不导电的化合物为非电解质,导电的原因为有自由移动的离子,本质区别是在水溶液或熔化状态下能否电离出自由移动的离子,故A正确;
B.纯碱是碳酸钠属于盐、烧碱事氢氧化钠均属于碱,故B错误;
C.电离时能产生H+的化合物,不一定是酸,如NaHSO4能电离出氢离子,属于盐,故C错误;
D.酸性氧化物是能与碱生成盐和水的反应,一般是非金属金属氧化物,但有些非金属氧化物不一定是酸性氧化物,如一氧化碳等,故D错误;
故选A.
点评 本题考查了电解质非电解质概念和实质的理解应用,注意物质名称、组成的分析判断,掌握基础是解题关键,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 离子方程式 | 单质氧化性 |
| 向NaBr溶液中滴入氯水,一段时间后再加入CCl4 | 静置后,液体分层,上层接近无色,下层橙红色 | 2Br-+Cl2=2 Cl-+Br2 | Cl2>Br2 |
| 向KI溶液中滴入氯水,一段时间后再加入CCl4 | 静置后,液体分层,上层接近无色,下层紫色 | 2I-+Cl2=2 Cl-+I2 | Cl2>I2 |
| 向KI溶液中滴入溴水,一段时间后再加入CCl4 | 静置后,液体分层,上层接近无色,下层紫色 | 2I-+Br2=2 Br-+I2 | Br2>I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Al3+、HCO3-、NO3- | B. | AlO2-、Cl-、Mg2+、K+ | ||
| C. | NH4+、Na+、CH3COO-、NO3- | D. | Na+、NO3-、Fe3+、I- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠着火后,可用泡沫灭火器来灭火 | |
| B. | 氧化钠和过氧化钠都属于碱性氧化物 | |
| C. | 氧化钠和过氧化钠的组成元素相同,都可以与CO2反应且产物相同 | |
| D. | 用洁净的玻璃管向包有Na2O2的脱脂棉吹气,脱脂棉燃烧,说明CO2、H2O与Na2O2的反应是放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba2+、Na+、CO32-、OH- | B. | Na+、Cu2+、SO42-、NO3- | ||
| C. | Mg2+、K+、OH-、Cl- | D. | H+、CO32-、NO3-、K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
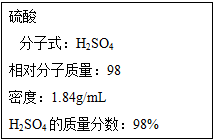 如图为实验室某浓硫酸试剂瓶的标签,试根据标签上的有关数据回答下列问题:
如图为实验室某浓硫酸试剂瓶的标签,试根据标签上的有关数据回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 吗啡、海洛因等虽然有麻醉、止痛、镇静作用,但易上瘾且有害,这类物质属于毒品 | |
| B. | 大量使用纯碱可使钙离子沉淀完全,预防胆结石产生 | |
| C. | 为使火腿肠颜色更鲜红,可多加一些亚硝酸钠 | |
| D. | 碳酸氢钠可作为抗酸药,阿司匹林是重要的抗生素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com