
|
含1 mol Ba(OH)2的稀溶液与足量稀盐酸反应,放出热量114.6 kJ.下列热化学方程式中,正确的是 | |
A. |
Ba(OH)2(aq)+2HCl(aq) |
B. |
Ba(OH)2(aq)+2HCl(aq) |
C. |
|
D. |
|
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:辽宁省葫芦岛一高2010-2011学年高二下学期第一次月考化学试题 题型:013
|
下列叙述正确的是 | |
| [ ] | |
A. |
合成氨生产过程中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率 |
B. |
含1 mol Ba(OH)2的稀溶液和含1 mol H2SO4的稀溶液反应释放热量a KJ,则表示该反应中和热的热化学反应方程式为:OH-(aq)+H+(aq)=H2O(l);ΔH=________a KJ/mol |
C. |
电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的Cl2进入阳极室 |
D. |
电解精炼铜时,同一时间内阳极溶解铜的质量比阴极析出铜的质量小 |
查看答案和解析>>
科目:高中化学 来源:辽宁省沈阳二中2011届高三第四次阶段测试化学试题 题型:013
|
下列叙述正确的是 | |
| [ ] | |
A. |
合成氨生产过程中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率 |
B. |
含1 mol Ba(OH)2的稀溶液和含1 mol H2SO4的稀溶液反应释放热量a KJ,则表示该反应中和热的热化学反应方程式为:OH-(aq)+H+(aq)=H2O(l);ΔH=-a KJ/mol |
C. |
电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的Cl2进入阳极室 |
D. |
电解精炼铜时,同一时间内阳极溶解铜的质量比阴极析出铜的质量小 |
查看答案和解析>>
科目:高中化学 来源:江西省白鹭洲中学2012届高三第一次月考化学试题 题型:013
|
向含 1 mol HCl和1 mol MgSO4的混合溶液中加入1 mol·L-1的Ba(OH)2溶液,产生沉淀的物质的量(n)与加入Ba(OH) 2溶液体积(V)间的关系图正确的是 | |
| [ ] | |
A. |
|
B. |
|
C. |
|
D. |
|
查看答案和解析>>
科目:高中化学 来源:山西省太原五中2012届高三10月月考化学试题 题型:022
有A、B、C、D、E五种常见化合物,都是由下表中的离子形成的:
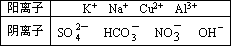
为了鉴别上述化合物.分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴人到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,只有B、C为紫色(透过蓝色钻玻璃);
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中都能产生白色沉淀;
⑤将B、D两溶液混合,未见沉淀或气体生成.若将D的溶液酸化,并加入铜片,则能生成一种气体,该气体遇空气变为红棕色
根据上述实验填空:
(1)写出B、D的化学式:B________ D________
(2)将含1 mol A的溶液与含1 mol E的溶液反应后蒸干,仅得到一种化合物,该化合物的化学式为________.
(3)在A溶液中加入少量澄清石灰水,其离子方程式为________.
(4)C常用作净水剂,用离子方程式和适当文字说明其净水原理________.
(5)若向含溶质1 mol的C溶液中逐滴加入Ba(OH)2溶液,生成沉淀质量最大为________克.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com