
【题目】(1)标准状况下,用一定量的水吸收氨气后制得浓度为12.0mol·L-1、密度为0.915g·cm-3的氨水。试计算1体积水吸收____________体积的氨气可制得上述氨水。(水的密度以1.00g·cm-3计)
(2) 硫铁矿高温下空气氧化产生二氧化硫:4FeS2+11O2 = 8SO2+2Fe2O3设空气中N2、O2的含量分别为0.800和0.200(体积分数),试完成下列各题:
①1.00mol FeS2完全氧化,需要空气的体积(标准状况)为________L
②55L空气和足量FeS2完全反应后,气体体积(同温同压)变为________L
③设FeS2氧化产生的气体混合物为100L,其中O2为aL,SO2为bL。写出a和b的关系式:________________________________
【答案】378 308 52 13b=200-10a
【解析】
(1)假设溶液体积为1.00L,根据n(NH3)=c(NH3)×V,求出1L溶液中所含氨气的物质的量,求出标准状况下氨气的体积;根据水的质量=氨水的质量-氨气的质量,求出水的质量,进而求出水的体积;由V(NH3/V(H2O)求出1体积水所吸收氨气的体积。
(2)①根据方程式计算需要氧气的物质的量,再根据V=nVm氧气的体积,根据空气中氧气的体积分数计算需要空气的体积;
②计算空气中氧气的体积,利用差量法计算反应后气体体积变化,据此解答;
③根据二氧化硫的体积计算参加反应氧气体积,表示出氮气的体积,利用氮气体积不变列关系式解答;
(1)假设溶液体积为1.00L,1.00L该氨水含氨的物质的量为1.00L×12.0mol/L=12.0mol,V(NH3)=12.0mol×22.4L/mol=268.8L;1.00L该氨水中含水的质量m(H2O)=1![]() 12
12![]() =711g,V(H2O)=
=711g,V(H2O)=![]() L=0.711L;标准状况下,1体积水吸收氨气的体积为V(H2)=(268L/0.711L)
L=0.711L;标准状况下,1体积水吸收氨气的体积为V(H2)=(268L/0.711L)![]() 1L=378L,本题答案为:378
1L=378L,本题答案为:378
(2)①根据方程式4FeS2+11O2=8SO2+2Fe2O3可以知道,1.00molFeS2完全氧化需要氧气物质的量=11/4mol,故需要空气的体积=![]() =308L,因此,本题答案为:308;
=308L,因此,本题答案为:308;
②55L空气中氧气的体积=55L×0.2=11L,则:4FeS2+11O2=8SO2+2Fe2O3
11 8 △V = 11-8=3
故反应后气体的体积为55L-3L=52L,因此,本题正确答案是:52;
③4FeS2+11O2=8SO2+2Fe2O3
11 8
( 11/8 )b b
反应前后氮气的体积不变,则:(aL+![]() bL)
bL)![]() 4=100L-aL-bL,整理可得:13b=200-10a,因此,本题答案是:13b=200-10a。
4=100L-aL-bL,整理可得:13b=200-10a,因此,本题答案是:13b=200-10a。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】有硫酸镁溶液500mL,它的密度是1.20g/cm3,其中镁离子的质量分数是4.8%,则有关该溶液的说法不正确的是
A. 溶质的质量分数是24.0%
B. 硫酸根离子的质量分数是19.2%
C. 溶液的物质的量浓度是2.4mol/L
D. 溶质和溶剂的物质的量之比是1:40
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物甲和G都在生活中有很多用途,其合成路线如下:
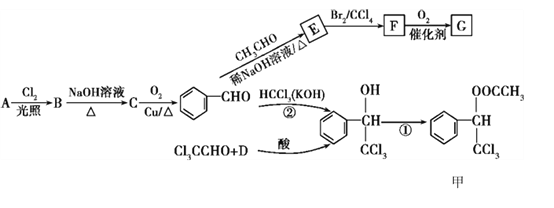
已知:①R1—CHO+R2—CH2—CHO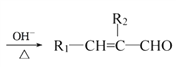 (R1、R2代表烃基或氢原子)
(R1、R2代表烃基或氢原子)
②D与A互为同系物;在相同条件下,D蒸气相对于氢气的密度为39。
(1)A的分子式是____,G中含氧官能团的名称是____。
(2)②的反应类型是____, F的结构简式为______。
(3)B的核磁共振氢谱有____组峰,峰面积之比为_____________。
(4)C有多种同分异构体,其中属于芳香族化合物的有____种。
(5)写出反应①的化学方程式:_____________。
(6)设计实验检验E中的官能团(说明实验操作步骤、现象及结论)____________
(7)G的同分异构体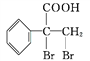 是一种重要的药物中间体,其合成路线与G相似,请以
是一种重要的药物中间体,其合成路线与G相似,请以![]() 为原料设计它的合成路线(其他所需原料自选,注明反应条件)________。
为原料设计它的合成路线(其他所需原料自选,注明反应条件)________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】你认为减少酸雨的产生可采取的措施是( )
①用煤作燃料 ②把工厂烟囱造高 ③化石燃料脱硫 ④在已酸化的土壤中加石灰 ⑤开发新能源.
A.①②③
B.②③④⑤
C.③⑤
D.①③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K时,将n(HA)+n(Aˉ)=0.lmol的HA、NaA混合物溶于水形成1L溶液,溶液中c(HA)、c(Aˉ)与pH的关系如图所示。下列叙述中正确的是
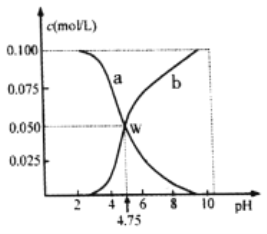
A. a线表示的是c(Aˉ)的变化
B. pH=6 时,c(Na+)+c(HA)>0. 1mol/L
C. 298K时,Aˉ的水解平衡常数(K)的数量级为10-10
D. 若将等物质的量的HA、NaA溶于水中,所得溶液pH恰好为4.75
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上冶炼钛的有关反应如下所示:
① C(s) + O2(g) ![]() CO2(g) ΔH1
CO2(g) ΔH1
② 2CO(g) + O2(g) ![]() 2CO2(g) ΔH2
2CO2(g) ΔH2
③ TiO2(s) + 2Cl2(g) ![]() TiCl4(g) + O2(g) ΔH3
TiCl4(g) + O2(g) ΔH3
④ TiCl4(s) + 2Mg(s) ![]() 2MgCl2(s) + Ti(s) ΔH4
2MgCl2(s) + Ti(s) ΔH4
⑤ TiO2(s) + 2Cl2(g) + 2C(s) ![]() TiCl4(g) + 2CO(g) ΔH5
TiCl4(g) + 2CO(g) ΔH5
下列有关推断正确的是( )
A. 2ΔH1=ΔH2 B. ΔH1<0,ΔH2>0
C. ΔH5=ΔH3+2ΔH1-ΔH2 D. 2ΔH1-ΔH2>0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com