
| A. | 常温下 pH为5的盐酸溶液稀释 1000倍后,pH 等于8 | |
| B. | 在滴有酚酞溶液的氨水里,加入盐酸至恰好呈无色,则此时溶液的 pH=7 | |
| C. | 浓度均为0.1 mol/L的氨水和氯化铵溶液,水电离出的 c(H+)前者大于后者 | |
| D. | 等浓度的 CH3COOH与 KOH任意比混合:c(K+)+c(H+)=c(OH-)+c(CH3COO-) |
分析 A.酸溶液无论稀释多少倍,都不可能呈碱性;
B.酚酞的不是范围为8-10,滴有酚酞的溶液呈无色,溶液可能为酸性;
C.弱碱抑制水的电离,盐类水解促进水的电离;
D.任何溶液都遵循电荷守恒,根据电荷守恒判断.
解答 解:A.常温下pH为5的盐酸溶液稀释1000倍后,pH接近7,但小于7,溶液不可能呈碱性,故A错误;
B.在滴有酚酞溶液的氨水里,加入盐酸至恰好呈无色,该溶液可能为酸性,此时溶液的pH不一定为7,故B错误;
C.氨水中存在:NH3•H20?NH4++OH-,抑制水的电离,氯化铵溶液存在:NH4++H20?NH3•H20+H+,促进水的电离,水电离出的 c(H+)前者小于后者,故C错误;
D.任何溶液都遵循电荷守恒,则等物质的量浓度的CH3COOH溶液与KOH溶液任意比混合:c(K+)+c(H+)=c(OH-)+c(CH3COO-),故D正确;
故选D.
点评 本题考查离子浓度的比较、酸的稀释以及盐类水解等知识,题目难度中等,本题注意把握守恒方法的应用,B为易错点,注意酚酞的不是范围.


科目:高中化学 来源: 题型:选择题
| A. | 甲酸 | B. | 乙酸 | C. | 丙酸 | D. | 乙二酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯与溴水在铁做催化剂的作用下可以发生取代反应 | |
| B. | 甲烷和苯都既能发生取代反应,又能使酸性KMnO4溶液褪色 | |
| C. | 乙醇和乙酸分子中都含羟基,都既能与Na反应,又能与NaOH溶液反应 | |
| D. | 甲苯可与浓硝酸在一定条件下发生取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol H2的质量只有在标准状况下才为2 g | |
| B. | 标准状况下,1 mol水蒸气的体积大约为22.4 L | |
| C. | 273℃,1.01×105 Pa状态下,1 mol气体体积大于22.4 L | |
| D. | 0.5 mol O2和0.5 mol N2组成的混合气体体积约为22.4 L |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油的分馏、煤的气化属物理变化;石油的裂解、煤的干馏属化学变化 | |
| B. | 铝及合金是日常生活广泛使用的材料,通常用电解氯化铝的方法制取铝 | |
| C. | 绿色化学期望从源头消除污染,生产过程中充分利用原料,实现零排放 | |
| D. | 在江河入海口的钢铁闸门上安装铜块或锌块,均可防止钢铁闸门被腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA | |
| B. | 28g乙烯(C2H4)和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA | |
| C. | 常温常压下,92g的NO2和N2O4混合气体含有的原子数为6NA | |
| D. | 0.5molO3与11.2LO2所含的分子数一定相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
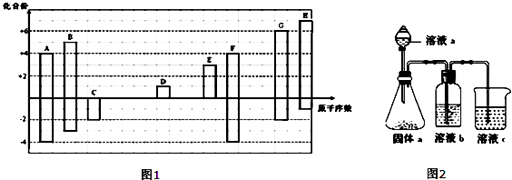
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com