

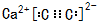 ,A的结构式H-C≡C-H,B分子中碳原子的杂化方式是sp2
,A的结构式H-C≡C-H,B分子中碳原子的杂化方式是sp2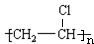 .
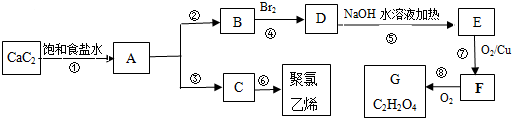
. 分析 碳化钙与饱和食盐水反应得到有机物A,则A为CH≡CH,B是一种植物生长的调节剂,为乙烯,则乙炔与氢气发生加成反应生成B,B为CH2=CH2,B与溴发生加成反应生成D,D为BrCH2CH2Br,D发生水解反应生成E,E为HOCH2CH2OH;
氯乙烯发生加聚反应生成聚氯乙烯,则C为CH2=CHCl,A与HCl发生加成反应生成C,据此分析解答.
解答 解:碳化钙与饱和食盐水反应得到有机物A,则A为CH≡CH,B是一种植物生长的调节剂,为乙烯,则乙炔与氢气发生加成反应生成B,B为CH2=CH2,B与溴发生加成反应生成D,D为BrCH2CH2Br,D发生水解反应生成E,E为HOCH2CH2OH;
氯乙烯发生加聚反应生成聚氯乙烯,则C为CH2=CHCl,A与HCl发生加成反应生成C,
(1)CaC2的电子式为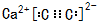 ,A的结构式H-C≡C-H,B为乙烯,每个C原子价层电子对个数是3,为sp2杂化,
,A的结构式H-C≡C-H,B为乙烯,每个C原子价层电子对个数是3,为sp2杂化,
故答案为: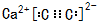 ;H-C≡C-H;sp2;
;H-C≡C-H;sp2;
(2)上述反应中,反应②③④属于加成反应,反应⑤属于取代反应,反应⑥属于加聚反应,反应⑦⑧属于氧化反应,
故答案为:加成反应;取代反应;加聚反应;
(3)反应①的化学反应方程式为:CaC2+2H2O→Ca(OH)2+C2H2↑;
③的反应方程式为:HC≡CH+HCl $\stackrel{一定条件下}{→}$CH2=CHCl;
⑤的反应方程式为:BrCH2CH2Br+2NaOH$→_{△}^{H_{2}O}$HOCH2CH2OH+2NaBr;
反应⑥的化学反应方程式为:nCH2=CHCl$\stackrel{一定条件下}{→}$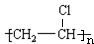 ;
;
故答案为:CaC2+2H2O→Ca(OH)2+C2H2↑;
HC≡CH+HCl $\stackrel{一定条件下}{→}$CH2=CHCl;
BrCH2CH2Br+2NaOH$→_{△}^{H_{2}O}$HOCH2CH2OH+2NaBr;
nCH2=CHCl$\stackrel{一定条件下}{→}$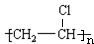 .
.
点评 本题考查有机物推断,为高频考点,涉及烃、卤代烃、醇、高分子化合物之间的转化,明确常见有机物官能团及其性质、反应条件、反应类型即可解答,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 锥形瓶里溶液在滴定过程中溅出 | |
| B. | 滴定管装液后尖嘴部位有气泡,滴定后气泡消失 | |
| C. | 指示剂变色15s后又恢复为原来的颜色便停止滴定 | |
| D. | 锥形瓶用蒸馏水冲洗后未用待测液润洗 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 30% | B. | 40% | C. | 50% | D. | 60% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 图为一个原电池,完成下列问题:
图为一个原电池,完成下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 任何可逆反应都有一定的限度 | |
| B. | 化学反应的限度是不可改变的 | |
| C. | 相同条件下,不同的可逆反应,其反应的限度不同 | |
| D. | 化学反应达到限度时,正逆反应速率相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀有气体元素最外层电子数均为8个 | |
| B. | 原子最外层少于4个电子的元素均是金属元素 | |
| C. | 相同条件下,H2O的沸点比H2S高是因为水分子间含有氢键 | |
| D. | 目前人们已发现了5000多种核素,说明发现了5000多种元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通入酸性KMnO4溶液 | B. | 通入澄清石灰水 | ||
| C. | 通入足量的溴水 | D. | 通入浓硫酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com