

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��14�֣��ϳɰ��Թ���ũҵ��������������Ҫ���塣
��֪��N2��g��+3H2��g��![]() 2NH3��g������H=-92��4 kJ��mol-1����ش�
2NH3��g������H=-92��4 kJ��mol-1����ش�
��1���ϳɰ���ҵ�в�ȡ�����д�ʩ��������������ԭ�����͵��ǣߣߣߣߣߣ�����ĸ����
a��������ý���������ӿ컯ѧ��Ӧ����
b�����ýϸ�ѹǿ��20 MPa~50 MPa��
c����ԭ�����е�����CO�����徻����ȥ
d�������ɵİ�Һ������ʱ����ϵ�з������
��2��һ���¶��£����ܱ������г���1 mol N2��3 mol H2��������Ӧ��
���������ݻ�V�㶨���ﵽƽ��ʱ�������ѹǿΪԭ����![]() ����N2��ת���ʧ�1=�ߣߣߣߣߣ���ʱ����Ӧ���ȣߣߣߣߣ�kJ�����¶��ºϳɰ���Ӧ��ƽ�ⳣ��K=�ߣߣߣߣߣ�ֻ���г����ֱ���ʽ����
����N2��ת���ʧ�1=�ߣߣߣߣߣ���ʱ����Ӧ���ȣߣߣߣߣ�kJ�����¶��ºϳɰ���Ӧ��ƽ�ⳣ��K=�ߣߣߣߣߣ�ֻ���г����ֱ���ʽ����
��������ѹǿ�㶨����ﵽƽ��ʱ��������N2��ת���ʧ�2�ߣߧ�1���������������
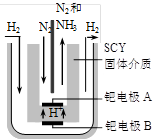
��3�����ŶԺϳɰ��о��ķ�չ��ϣ����ѧ�Ҳ��ø����ӵ����Ե�SCY�մɣ��ܴ���H+��Ϊ���ʣ�������������������ϵĽ����ٶྦྷ��Ĥ���缫��ʵ���˳�ѹ��570�������¸�ת���ʵĵ�ⷨ�ϳɰ���װ������ͼ�����ٵ缫A�ǵ��صģߣߣߣ���������� �����������ü��ϵĵ缫��Ӧʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010������ʡ��У������һ��ģ�⿼�����ۻ�ѧ���� ���ͣ������
��14�֣��ϳɰ��Թ���ũҵ��������������Ҫ���塣
��֪��N2��g��+3H2��g��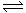 2NH3��g������H= -92��4 kJ��mol-1����ش�
2NH3��g������H= -92��4 kJ��mol-1����ش�
��1���ϳɰ���ҵ�в�ȡ�����д�ʩ��������������ԭ�����͵��ǣߣߣߣߣߣ�����ĸ����
a��������ý���������ӿ컯ѧ��Ӧ����
b�����ýϸ�ѹǿ��20 MPa~50 MPa��
c����ԭ�����е�����CO�����徻����ȥ
d�������ɵİ�Һ������ʱ����ϵ�з������
��2��һ���¶��£����ܱ������г���1 mol N2��3 mol H2��������Ӧ��
���������ݻ�V�㶨���ﵽƽ��ʱ�������ѹǿΪԭ���� ����N2��ת���ʧ�1=�ߣߣߣߣߣ���ʱ����Ӧ���ȣߣߣߣߣ�kJ�����¶��ºϳɰ���Ӧ��ƽ�ⳣ��K=�ߣߣߣߣߣ�ֻ���г����ֱ���ʽ����
����N2��ת���ʧ�1=�ߣߣߣߣߣ���ʱ����Ӧ���ȣߣߣߣߣ�kJ�����¶��ºϳɰ���Ӧ��ƽ�ⳣ��K=�ߣߣߣߣߣ�ֻ���г����ֱ���ʽ����
��������ѹǿ�㶨����ﵽƽ��ʱ��������N2��ת���ʧ�2�ߣߧ�1���������������
��3�����ŶԺϳɰ��о��ķ�չ��ϣ����ѧ�Ҳ��ø����ӵ����Ե�SCY�մɣ��ܴ���H+��Ϊ���ʣ�������������������ϵĽ����ٶྦྷ��Ĥ���缫��ʵ���˳�ѹ��570�������¸�ת���ʵĵ�ⷨ�ϳɰ���װ������ͼ�����ٵ缫A�ǵ��صģߣߣߣ���������� �����������ü��ϵĵ缫��Ӧʽ�� ��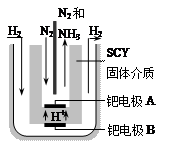
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010������ʡ��У������һ��ģ�⿼�����ۻ�ѧ���� ���ͣ��ۺ���
��14�֣��ϳɰ��Թ���ũҵ��������������Ҫ���塣
��֪��N2��g��+3H2��g�� 2NH3��g������H=
-92��4 kJ��mol-1����ش�
2NH3��g������H=
-92��4 kJ��mol-1����ش�
��1���ϳɰ���ҵ�в�ȡ�����д�ʩ��������������ԭ�����͵��ǣߣߣߣߣߣ�����ĸ����
a��������ý���������ӿ컯ѧ��Ӧ����
b�����ýϸ�ѹǿ��20 MPa~50 MPa��
c����ԭ�����е�����CO�����徻����ȥ
d�������ɵİ�Һ������ʱ����ϵ�з������
��2��һ���¶��£����ܱ������г���1 mol N2��3 mol H2��������Ӧ��
���������ݻ�V�㶨���ﵽƽ��ʱ�������ѹǿΪԭ���� ����N2��ת���ʧ�1=�ߣߣߣߣߣ���ʱ����Ӧ���ȣߣߣߣߣ�kJ�����¶��ºϳɰ���Ӧ��ƽ�ⳣ��K=�ߣߣߣߣߣ�ֻ���г����ֱ���ʽ����
����N2��ת���ʧ�1=�ߣߣߣߣߣ���ʱ����Ӧ���ȣߣߣߣߣ�kJ�����¶��ºϳɰ���Ӧ��ƽ�ⳣ��K=�ߣߣߣߣߣ�ֻ���г����ֱ���ʽ����
��������ѹǿ�㶨����ﵽƽ��ʱ��������N2��ת���ʧ�2�ߣߧ�1���������������
��3�����ŶԺϳɰ��о��ķ�չ��ϣ����ѧ�Ҳ��ø����ӵ����Ե�SCY�մɣ��ܴ���H+��Ϊ���ʣ�������������������ϵĽ����ٶྦྷ��Ĥ���缫��ʵ���˳�ѹ��570�������¸�ת���ʵĵ�ⷨ�ϳɰ���װ������ͼ�����ٵ缫A�ǵ��صģߣߣߣ���������� �����������ü��ϵĵ缫��Ӧʽ�� ��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ���Ĵ�ʡģ���� ���ͣ������
 2NH3(g)����H= -92.4 kJ/mol��
2NH3(g)����H= -92.4 kJ/mol��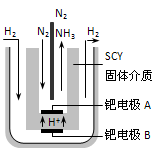
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com