
【题目】既能通过化学反应使溴水褪色,又能使酸性高锰酸钾溶液褪色的是
A. 苯 B. 乙烷 C. 聚乙烯 D. 丙烯
 步步高达标卷系列答案
步步高达标卷系列答案科目:高中化学 来源: 题型:
【题目】在2A(g)+B(s)![]() 3C(g)+4D(g)反应中,表示该反应速率最快的是( )
3C(g)+4D(g)反应中,表示该反应速率最快的是( )
A.υ(A)= 0.5 mol/(L·s) B.υ(B)= 0.3 mol/(L·s)
C.υ(C)= 12 mol/(L·min) D.υ(D)= 6 mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某一元弱酸(用HA表示)在水中的电离方程式是:HA![]() H++A-,回答下列问题:
H++A-,回答下列问题:
(1)若向溶液中加入少量Na,以上平衡将向________(填“正”、“逆”)反应方向移动,溶液中c(OH-)将________(填“增大”、“减小”或“不变”)。
(2)在一定温度下,HA加水稀释过程中溶液的导电能力如右图所示,请回答:

①a、b、c三点溶液中,c(H+)由小到大的顺序是: 。
②a、b、c三点溶液中,HA的电离程度最大的是: 。
(3)在25℃下,将c mol/L的HA与0.01mol/L的NaOH溶液等体积混合,反应平衡时溶液中c(Na+)=c(A-)。请用含c的代数式表示HA的电离常数Ka=________(注明单位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浮选凝聚法处理酸性污水的工作原理如图所示,下列说法不正确的是

A. Fe电极的电极反应式为:Fe-2e-═Fe2+
B. 通入空气的石墨电极的电极反应式为O2+2CO2+4e-═2CO32-
C. 通入甲烷的石墨电极的电极反应式为:CH4+100H--8e-═CO32-+7H2O
D. 为增强污水的导电能力,可向污水中加入适量工业用食盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A的结构简式如右图: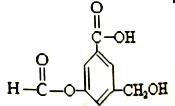
下列有关A的性质叙述中,正确的是
A. A 与金属钠完全反应时,两者反应的物质的量之比为1∶3
B. 1molA最多能与5mol氢气发生反应,反应类型是加成反应
C. 1molA与足量碳酸氢钠溶液反应,生成CO2的物质的量为2mol
D. A既能与羧基反应,又能与醇反应,还能发生水解反应和缩聚反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种短周期元素A、B、C、D、E的原子序数依次增大,A和C同族,B和D 同族,C的简单离子和B的简单离子具有相同的电子层结构。A和B、D、E均能形成共价型化合物。A和B形成的化合物在水中呈碱性,C和E形成的化合物中阴阳离子的个数比为1:1。回答下列问题:
(1)五种元素中,原子半径最大的是____________(填元素名称),非金属性最强元素的是___________。
(2)由元素A分别和元素B、D、E所形成的共价型化合物中,热稳定性最差的是
______________(用化学式表示)。
(3)元素A和E形成的化合物与元素A和B形成的化合物反应,产物的电子式为_________________,其中存在的化学键类型为_________________________。
(4)E离子的结构示意图是____________________;
元素D最高价氧化物的水化物的化学式为_________________。
(5)单质E与水反应的离子方程式为 ____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请根据题目要求回答以下问题:
(1)CuSO4·5H2O的摩尔质量是________; 0.1mol CH4含有的氢原子数为____; 0.2 mol·L-1的 AlCl3溶液中Cl—的物质的量浓度是________。
(2)现有以下物质:①NaCl ②氯水③醋酸 ④HCl ⑤酒精(C2H5OH)⑥CaCO3⑦Ba(OH)2属于强电解质的是__________,属于弱电解质的是_______。(填序号)
写出Ba(OH)2的电离方程式_________________________,
写出④与⑥反应的离子方程式____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向浓度为 0.1 mol/L、体积为 V L 的氨水中逐滴加入 0.1 mol/L 的盐酸,下列 各选项中数值变大的有
![]()
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[物质结构与性质]
原子序数小于36的X、Y、Z、W、R五种元素,原子序数依次增大。五种元素中,仅R为金属元素,其原子序数为27。X价电子排布式为nsnnpn,元素Z基态原子s电子总数与p电子总数相等,W与其它四种元素能层数不同,且未成对电子数目为1个。
根据判断出的元素回答下列问题:
(1)基态R原子核外电子排布式为 ,X、Y、Z三种原子第一电离能由大到小的顺序为 (用具体元素符号表示)。
(2)1mol配合物[R(XY)6]4-中含有σ键的数目为 。
(3)XZW2是一种高毒类物质,结构与甲醛相似,X原子杂化方式为 ,其沸点高于甲醛的主要原因是 。
(4)YW3为黄色、油状、具有刺激性气味的液体,该分子的立体构型为 (用文字描述)。
(5)某晶体的晶胞结构如下图所示,则该化合物的化学式为 (R、Z用具体元素符号表示)。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com