
£Ø13·Ö£©¹¤ŅµÉĻæÉĄūÓĆĆŗµÄĘų»Æ²śĪļ£ØCOŗĶH2£©ŗĻ³É¶ž¼×ĆŃ£ØCH3OCH3£©Ķ¬Ź±Éś³É¶žŃõ»ÆĢ¼£¬ĘäČż²½·“Ó¦ČēĻĀ£ŗ
¢Ł 2H2 (g)£«CO(g)  CH3OH (g) ¦¤H£½ £90.8 kJ”¤mol-1
CH3OH (g) ¦¤H£½ £90.8 kJ”¤mol-1
¢Ś 2CH3OH(g)  CH3OCH3(g)£«H2O(g) ¦¤H£½ £23.5 kJ”¤mol-1
CH3OCH3(g)£«H2O(g) ¦¤H£½ £23.5 kJ”¤mol-1
¢Ū CO(g)£«H2O(g)  CO2 (g)£«H2(g) ¦¤H£½ £41.3 kJ”¤mol-1
CO2 (g)£«H2(g) ¦¤H£½ £41.3 kJ”¤mol-1
£Ø1£©×ÜŗĻ³É·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ĪŖ ”£
£Ø2£©Ņ»¶ØĢõ¼žĻĀµÄĆܱÕČŻĘ÷ÖŠ£¬ÉĻŹö×Ü·“Ó¦“ļµ½Ę½ŗāŹ±£¬ŅŖĢįøßCOµÄ×Ŗ»ÆĀŹ£¬æÉŅŌ²ÉČ”µÄ“ėŹ©ŹĒ_____£ØĢī×ÖÄø“śŗÅ£©”£
A øßĪĀøßŃ¹ B ¼ÓČė“߻ƼĮ C ¼õÉŁCO2µÄÅضČ
D Ōö¼ÓCOµÄÅØ¶Č E ·ÖĄė³ö¶ž¼×ĆŃ
£Ø3£©·“Ó¦¢Ś2CH3OH(g) CH3OCH3(g)£«H2O(g)ŌŚĖÄÖÖ²»Ķ¬Ģõ¼žĻĀ½ųŠŠ£Ø·“Ó¦Ę÷¾łĪŖĻąĶ¬µÄŗćČŻĆܱÕČŻĘ÷£¬CH3OCH3”¢H2OĘšŹ¼ÅضČĪŖ0£©£¬CH3OH(g)µÄÅØ¶Č£Ømol/L£©Ėę·“Ó¦Ź±¼ä£Ømin£©µÄ±ä»ÆĒéæöČēĻĀ±ķ£ŗ
CH3OCH3(g)£«H2O(g)ŌŚĖÄÖÖ²»Ķ¬Ģõ¼žĻĀ½ųŠŠ£Ø·“Ó¦Ę÷¾łĪŖĻąĶ¬µÄŗćČŻĆܱÕČŻĘ÷£¬CH3OCH3”¢H2OĘšŹ¼ÅضČĪŖ0£©£¬CH3OH(g)µÄÅØ¶Č£Ømol/L£©Ėę·“Ó¦Ź±¼ä£Ømin£©µÄ±ä»ÆĒéæöČēĻĀ±ķ£ŗ
ŹµŃé ŠņŗÅ | ĪĀ¶Č ÅØ¶Č Ź±¼ä | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
1 | 800”ę | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
2 | 800”ę | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
3 | 800”ę | c3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
4 | 820”ę | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
øł¾ŻÉĻŹöŹż¾Ż£¬Ķź³ÉĻĀĮŠĢīæÕ£ŗ
¢ŁŹµŃé1£¬·“Ó¦ŌŚ10ÖĮ20·ÖÖÓŹ±¼äÄŚÓĆCH3OH(g)±ķŹ¾µÄĘ½¾łĖŁĀŹĪŖ ”£
¢ŚŹµŃé2£¬CH3OH(g)µÄ³õŹ¼ÅضČc2£½ mol/L£¬·“Ó¦¾20·ÖÖÓ¾Ķ“ļµ½Ę½ŗā£¬æÉĶĘ²āŹµŃé2ÖŠ»¹Ņžŗ¬µÄĢõ¼žŹĒ ”£
¢ŪÉ菵Ńé3µÄ·“Ó¦ĖŁĀŹĪŖv3£¬ŹµŃé1µÄ·“Ó¦ĖŁĀŹĪŖv1£¬Ōņv3 v1£ØĢī£¾”¢£½”¢£¼£©£¬ĒŅc3£½ mol/L”£
£Ø13·Ö£©
£Ø1£©3H2(g)£«3CO(g) CH3OCH3(g)£«CO2 (g) ¦¤H£½£246.4 kJ”¤mol-1£Ø2·Ö£©
CH3OCH3(g)£«CO2 (g) ¦¤H£½£246.4 kJ”¤mol-1£Ø2·Ö£©
£Ø2£© C E £Ø2·Ö£©
£Ø3£©¢Ł0.013mol/(L”¤min) £Ø2·Ö£©
¢Ś1.0£Ø2·Ö£©£¬“߻ƼĮ£Ø1·Ö£©
¢Ū£¾£Ø2·Ö£©£¬1.2 mol/L£Ø2·Ö£©
”¾½āĪö”æ
ŹŌĢā·ÖĪö£ŗ£Ø1£©×ÜŗĻ³É·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ3H2(g)£«3CO(g) CH3OCH3(g)£«CO2 (g)£¬øł¾ŻøĒĖ¹¶ØĀɵĆ×Ü·“Ó¦=¢Ł”Į2+¢Ś+¢Ū£¬ĖłŅŌ×Ü·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ĪŖ3H2(g)£«3CO(g)
CH3OCH3(g)£«CO2 (g)£¬øł¾ŻøĒĖ¹¶ØĀɵĆ×Ü·“Ó¦=¢Ł”Į2+¢Ś+¢Ū£¬ĖłŅŌ×Ü·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ĪŖ3H2(g)£«3CO(g) CH3OCH3(g)£«CO2 (g) ¦¤H£½£246.4 kJ”¤mol-1£»
CH3OCH3(g)£«CO2 (g) ¦¤H£½£246.4 kJ”¤mol-1£»
£Ø2£©A”¢ĪĀ¶ČÉżøߣ¬Ę½ŗāÄęĻņŅĘ¶Æ£¬COµÄ×Ŗ»ÆĀŹ½µµĶ£¬“ķĪó£»B”¢¼ÓČė“߻ƼĮ¶ŌĘ½ŗāĪŽÓ°Ļģ£¬COµÄ×Ŗ»ÆĀŹ²»±ä£¬“ķĪó£»C”¢¼õÉŁ¶žŃõ»ÆĢ¼µÄÅØ¶Č£¬Ę½ŗāÕżĻņŅĘ¶Æ£¬COµÄ×Ŗ»ÆĀŹŌö“ó£¬ÕżČ·£»D”¢Ōö¼ÓCOµÄÅØ¶Č£¬ĖäČ»Ę½ŗāÕżĻņŅĘ¶Æ£¬µ«ŹĒCOµÄ×Ŗ»ÆĀŹ½µµĶ£¬“ķĪó£»E”¢·ÖĄė³ö¶ž¼×ĆŃ£¬Éś³ÉĪļÅØ¶Č¼õŠ”£¬Ę½ŗāÕżĻņŅĘ¶Æ£¬COµÄ×Ŗ»ÆĀŹÉżøߣ¬ÕżČ·£¬“š°øŃ”CE£»
£Ø3£©¢ŁŹµŃé1£¬·“Ó¦ŌŚ10ÖĮ20·ÖÖÓŹ±¼äÄŚÓĆCH3OH(g)µÄÅØ¶Č¼õÉŁ0.80-0.67=0.13mol/L£¬ĖłŅŌÓĆ¼×“¼±ķŹ¾µÄĘ½¾łĖŁĀŹĪŖ0.13mol/L/10min=0.013 mol/(L”¤min)£»
¢ŚŹµŃé2ÓėŹµŃé1µÄĪĀ¶ČĻąĶ¬£¬“ļµ½µÄĘ½ŗāדĢ¬ĻąĶ¬£¬µ«²»Ķ¬µÄŹĒ“ļµ½Ę½ŗāµÄŹ±¼ä¶Ģ£¬ĖłŅŌŹµŃé2ÖŠµÄ¼Ó³ÉµÄĘšŹ¼ÅضČÓėŹµŃé1ĻąĶ¬£¬¶¼ŹĒ1.0mol/L£¬ŹµŃé2µÄ·“Ó¦ĖŁĀŹæģ£¬µ«Ę½ŗāĪ“øı䣬ĖłŅŌŅžŗ¬µÄĢõ¼žŹĒŹµŃé2Ź¹ÓĆĮĖ“߻ƼĮ£»
¢Ūøł¾Ż±ķÖŠŹż¾ŻæÉÖŖŹµŃé3Ę½ŗāŹ±CH3OH(g)ÅØ¶Č“óÓŚŹµŃé1£¬ŌņŹµŃé3µÄ¼×“¼µÄĘšŹ¼ÅØ¶Č“óÓŚŹµŃé1£¬·“Ó¦ĪļÅضČŌö“󣬷“Ó¦ĖŁĀŹ¼Óæģ£¬ĖłŅŌv3>v1£»2CH3OH(g) CH3OCH3(g)£«H2O(g)ŹĒ·“Ó¦Ē°ŗóĘųĢåĪļÖŹµÄĮæ²»±äµÄæÉÄę·“Ó¦£¬ĖłŅŌŗćĪĀŗćČŻĢõ¼žĻĀ“ļµ½µÄĘ½ŗāŹĒµČŠ§Ę½ŗā£¬ŹµŃé3ÖŠ¼×“¼Ę½ŗāÅØ¶ČŹĒŹµŃé1µÄ0.6/0.5=1.2±¶£¬ŌņĘšŹ¼ÅضČŅ²ŹĒŹµŃé1µÄ1.2±¶£¬ĖłŅŌc3£½1.2mol/L”£
CH3OCH3(g)£«H2O(g)ŹĒ·“Ó¦Ē°ŗóĘųĢåĪļÖŹµÄĮæ²»±äµÄæÉÄę·“Ó¦£¬ĖłŅŌŗćĪĀŗćČŻĢõ¼žĻĀ“ļµ½µÄĘ½ŗāŹĒµČŠ§Ę½ŗā£¬ŹµŃé3ÖŠ¼×“¼Ę½ŗāÅØ¶ČŹĒŹµŃé1µÄ0.6/0.5=1.2±¶£¬ŌņĘšŹ¼ÅضČŅ²ŹĒŹµŃé1µÄ1.2±¶£¬ĖłŅŌc3£½1.2mol/L”£
æ¼µć£ŗæ¼²é»ÆŃ§Ę½ŗāĄķĀŪµÄÓ¦ÓĆ£¬Ę½ŗāµÄ¼ĘĖć£¬µČŠ§Ę½ŗāµÄÅŠ¶Ļ£¬øĒĖ¹¶ØĀɵÄÓ¦ÓĆ


 A¼Ó½šĢā ĻµĮŠ“š°ø
A¼Ó½šĢā ĻµĮŠ“š°ø Č«ÓŲāŹŌ¾ķĻµĮŠ“š°ø
Č«ÓŲāŹŌ¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğÕć½Ź”¶«ŃōĶā¹śÓļѧŠ£ø߶žÉĻѧʌʌ֊»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ČĖĢåŃŖŅŗÄŚµÄŃŖŗģµ°°×(Hb)Ņ×ÓėO2½įŗĻÉś³ÉHbO2£¬Ņņ“Ė¾ßÓŠŹäŃõÄÜĮ¦£®COĪüČė·ĪÖŠ·¢Éś·“Ó¦£ŗCO£«HbO2 O2£«HbCO,37”ꏱ£¬øĆ·“Ó¦µÄĘ½ŗā³£ŹżK£½220.HbCOµÄÅØ¶Č“ļµ½HbO2ÅØ¶ČµÄ0.02±¶£¬»įŹ¹ČĖÖĒĮ¦ŹÜĖš£®¾Ż“Ė£¬ĻĀĮŠ½įĀŪ“ķĪóµÄŹĒ
O2£«HbCO,37”ꏱ£¬øĆ·“Ó¦µÄĘ½ŗā³£ŹżK£½220.HbCOµÄÅØ¶Č“ļµ½HbO2ÅØ¶ČµÄ0.02±¶£¬»įŹ¹ČĖÖĒĮ¦ŹÜĖš£®¾Ż“Ė£¬ĻĀĮŠ½įĀŪ“ķĪóµÄŹĒ
A£®COÓėHbO2·“Ó¦µÄĘ½ŗā³£Źż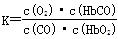
B£®ČĖĢåĪüČėµÄCOŌ½¶ą£¬ÓėŃŖŗģµ°°×½įŗĻµÄO2Ō½ÉŁ
C£®µ±ĪüČėµÄCOÓėO2ÅضČÖ®±Č“óÓŚ»ņµČÓŚ0.02Ź±£¬ČĖµÄÖĒĮ¦²Å»įŹÜĖš
D£®°ŃCOÖŠ¶¾µÄ²”ČĖ·ÅČėøßŃ¹Ńõ²ÖÖŠ½ā¶¾£¬ĘäŌĄķŹĒŹ¹ÉĻŹöĘ½ŗāĻņ×óŅʶÆ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğÕć½ĢØ֯֊ѧø߶žÉĻѧʌµŚŅ»“ĪĶ³Į·»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A£®ČČ»Æѧ·½³ĢŹ½ÖŠ£¬ČēĆ»ÓŠ×¢Ć÷ĪĀ¶ČŗĶŃ¹Ē棬±ķŹ¾·“Ó¦ČČŹĒŌŚ±ź×¼×“æöĻĀ²āµĆµÄŹż¾Ż
B£®ÉżøßĪĀ¶ČŗĶŌö¼Ó·“Ó¦ĪļµÄÅØ¶Č£¬¶¼Ź¹·“Ó¦Īļ»ī»Æ·Ö×ÓŹżŗĶ»ī»Æ·Ö×Ó°Ł·ÖŹżĶ¬Ź±Ōö¼Ó
C£®»Æѧ·“Ó¦ĖŁĀŹæÉĶعżŹµŃé²ā¶Ø£¬±ČČēæÉŅŌ²āĮæŌŚŅ»¶ØĪĀ¶ČŗĶŃ¹ĒæĻĀŹĶ·Å³öĄ“µÄĘųĢåµÄĢå»ż£¬»ņÕßæÉŅŌÓƱČÉ«µÄ·½·Ø²ā¶ØČÜŅŗŃÕÉ«µÄÉīĒ³½ųŠŠ»»Ėć
D£®ĪļÖŹ·¢Éś»Æѧ±ä»Æ²»Ņ»¶Ø°éĖę×ÅÄÜĮæ±ä»Æ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğŗÓÄĻŪ³ĮźĻŲµŚŅ»øßÖŠø߶žÉĻµŚŅ»“Īæ¼ŹŌ»Æѧ£ØB£©ŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
X”¢Y”¢ZČżÖÖĘųĢ壬°Ńa mol XÓėb mol Y³äČėŅ»ĆܱÕČŻĘ÷ÖŠ£¬·¢Éś·“Ó¦£ŗ
X£«2Y 2Z”£“ļµ½Ę½ŗāŹ±£¬ČōĖüĆĒµÄĪļÖŹµÄĮæĀś×ć£ŗn(X)£«n(Y)£½n(Z)£¬ŌņYµÄ×Ŗ
2Z”£“ļµ½Ę½ŗāŹ±£¬ČōĖüĆĒµÄĪļÖŹµÄĮæĀś×ć£ŗn(X)£«n(Y)£½n(Z)£¬ŌņYµÄ×Ŗ
»ÆĀŹĪŖ
A£® ”Į100% B£®
”Į100% B£®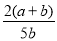 ”Į100%
”Į100%
C£®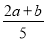 ”Į100% D£®
”Į100% D£®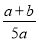 ”Į100%
”Į100%
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğŗÓÄĻŪ³ĮźĻŲµŚŅ»øßÖŠø߶žÉĻµŚŅ»“Īæ¼ŹŌ»Æѧ£ØB£©ŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
pHĻąĶ¬µÄ°±Ė®ŗĶNaOHČÜŅŗ£¬·Ö±šÓĆÕōĮóĖ®Ļ”ŹĶÖĮŌĢå»żµÄm±¶ŗĶn±¶£¬Ļ”ŹĶŗóĮ½ČÜŅŗµÄpHČŌČ»ĻąĶ¬£¬ŌņmŗĶnµÄ¹ŲĻµŹĒ
A£®m£¼n B£®m£½n C£®m£¾n D£®²»ÄÜČ·¶Ø
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğŗÓÄĻŪ³ĮźĻŲµŚŅ»øßÖŠø߶žÉĻµŚŅ»“Īæ¼ŹŌ»Æѧ£ØA£©ŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŌŚŅ»¶ØĪĀ¶ČĻĀ£¬½«ĘųĢåXŗĶĘųĢåYø÷0.16mol³äČė10LŗćČŻĆܱÕČŻĘ÷ÖŠ£¬·¢Éś·“Ó¦
X(g)£«Y(g) 2Z(g) ¦¤H£¼0£¬Ņ»¶ĪŹ±¼äŗó“ļµ½Ę½ŗā£¬·“Ó¦¹ż³ĢÖŠ²ā¶ØµÄŹż¾ŻČēĻĀ
2Z(g) ¦¤H£¼0£¬Ņ»¶ĪŹ±¼äŗó“ļµ½Ę½ŗā£¬·“Ó¦¹ż³ĢÖŠ²ā¶ØµÄŹż¾ŻČēĻĀ
±ķ£ŗ
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®øĆĪĀ¶ČĻĀ“Ė·“Ó¦µÄĘ½ŗā³£ŹżK£½1.44
B£®ĘäĖūĢõ¼ž²»±ä£¬½µµĶĪĀ¶Č£¬·“Ó¦“ļµ½ŠĀĘ½ŗāĒ°¦Ķ(Äę)£¾¦Ķ(Õż)
C£®·“Ó¦Ē°2minµÄĘ½¾łĖŁĀŹ¦Ķ(Z)£½2.0”Į10£3mol”¤L£1”¤min-1
D£®ĘäĖūĢõ¼ž²»±ä£¬ŌŁ³äČė0.2mol Z£¬Ę½ŗāŹ±XµÄĢå»ż·ÖŹżŌö“ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğŗÓÄĻŪ³ĮźĻŲµŚŅ»øßÖŠø߶žÉĻµŚŅ»“Īæ¼ŹŌ»Æѧ£ØA£©ŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĶ¼±ķŹ¾ČÜŅŗÖŠc(OH£)ŗĶc(H£«)µÄ¹ŲĻµ£¬ĻĀĮŠÅŠ¶Ļ“ķĪóµÄŹĒ£Ø £©
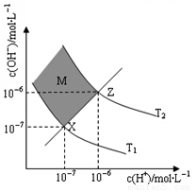
A£®Į½ĢõĒśĻß¼äČĪŅāµć¾łÓŠc(H£«)”¤c(OH£)£½Kw
B£®MĒųÓņÄŚČĪŅāµć¾łÓŠc(H£«)£¼c(OH£)
C£®Ķ¼ÖŠT1£¼T2
D£®XZĻßÉĻČĪŅāµć¾łÓŠpH£½7
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğŗÓÄĻŪ³ĮźĻŲµŚŅ»øßÖŠøßŅ»ÉĻµŚŅ»“Īæ¼ŹŌ»Æѧ£ØB£©ŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
Óė50 mL 0.1 mol/L Na2CO3 ČÜŅŗÖŠ Na+ µÄĪļÖŹµÄĮæÅضČĻąĶ¬µÄČÜŅŗŹĒ£Ø £©
A£®50mL 0.2mol/LµÄNaClČÜŅŗ B£®100mL 0.1mol/LµÄNaClČÜŅŗ
C£®25mL 0.2mol/LµÄNa2SO4ČÜŅŗ D£®10mL 0.5mol/LµÄNa2CO3ČÜŅŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğŗÓÄĻÖ£ÖŻŹŠøßŅ»ÉĻ10ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
æóČŖĖ®ŹĒČĖĆĒ¾Ó¼ŅĀĆÓĪ³£ÓƵÄŅūĮĻ£¬ŹŠ³”ÉĻÓŠŠ©²»·ØÉĢ··ĪŖÄ²Č”±©Ąū£¬ÓĆ×ŌĄ“Ė®£ØÓĆĀČĘųĻū¶¾£©Ć°³äæóČŖĖ®³öŹŪ”£ĪŖ±ę±šÕęĪ±£¬æÉÓĆĻĀĮŠµÄŅ»ÖÖ»ÆѧŹŌ¼ĮĄ“¼ų±š£¬øĆŹŌ¼ĮŹĒ£Ø £©
A£®·ÓĢŖŹŌŅŗ B£®ĀČ»Æ±µČÜŅŗ
C£®ĒāŃõ»ÆÄĘČÜŅŗ D£®ĻõĖįŅųČÜŅŗ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com