
环己酮是一种重要的有机化工原料。实验室合成环己酮的反应如下: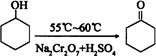
环己醇和环己酮的部分物理性质见下表:
| 物质 | 相对分子质量 | 沸点(℃) | 密度(g·cm—3、20 ℃) | 溶解性 | |
| 环己醇 | 100 | 161.1 | 0.9624 | 能溶于水和醚 | |
| 环己酮 | 98 | 155.6 | 0.9478 | 微溶于水,能溶于醚 | |

(1)D B E C A
(2)使水层中少量的有机物进一步被提取,提高产品的产量
(3)A B C
(4)降低环己酮的溶解度;增加水层的密度,有利于分层 水浴加热
(5)停止加热,冷却后通自来水
(6)60%(60.3%)
解析试题分析:(1)在上述方法中制取的物质环己酮中含有未反应的环己醇。由于环己醇能溶于水和醚,而环己酮微溶于水,能溶于醚,所以提纯步骤的正确步骤首先是往液体中加入NaCl固体至饱和,静置,分液。然后水层用乙醚(乙醚沸点34.6℃,易燃烧)萃取,萃取液并入有机层;再加入无水MgSO4固体,除去有机物中少量水。接着进行过滤,除去MgSO4晶体。最后蒸馏、除去乙醚后,收集151℃~156℃馏分即得到纯净的环己酮。(2)在B中水层用乙醚萃取的目的是使水层中少量的有机物进一步被提取,提高产品的产量。(3)混合振荡:用左手握住分液漏斗活塞,右手压住分液漏斗口部,把分液漏斗倒转过来振荡,使两种液体充分接触,振荡后打开活塞,将漏斗内气体放出. 分液时,为了使液体能够顺利流出,需先将上口玻璃塞打开或玻璃塞上的凹槽对准漏斗上的小孔,下层液体从下口流出,上层的液体从上口倒出。因此,错误的操作为A B C 。(4)在上述操作D中,加入NaCl固体的作用是降低环己酮的溶解度;增加水层的密度,有利于分层。在蒸馏除乙醚的操作中为了减少环己酮的挥发造成的消耗。通常采用的加热方式为水浴加热。(5)蒸馏操作时,一段时间后若发现未通冷凝水,应采取的正确方法是停止加热,冷却后通自来水,否则会导致冷凝管炸裂。(6)实际产量:m(环己酮)=" 0.9478g/ml×12mL=" 11.3736g.n(环己酮)=m÷M=11.3736g÷98g/mol="0.116mol." m(环己醇)= 0.9624g/ml×20ml=19.248g.n(环己醇)=19.248g ÷100g/mol="0.19248mol" .所以环己酮的产率为:(0.116mol÷0.19248mol)×100% ="60%" 。
考点:考查化学实验的步骤、及操作方法、错误的纠正方法、试剂的选择、产品产率的计算等知识。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:实验题
(14分)锰锌软磁铁氧体具有高磁导率、低矫顽力和低功率损耗等性能,已广泛应用于电子工业。碳酸锰主要用于制备锰锌软磁铁氧体,而制碳酸锰的原料之一是二氧化锰。某化学研究性学习小组拟从废旧干电池中回收二氧化锰制取碳酸锰。
①将干电池剖切、分选得到黑色混合物(主要成分为MnO2)洗涤、过滤、烘干。
②将上述固体按固液体积比2:9加入浓盐酸、加热,反应完全后过滤、浓缩。
③向上述溶液中加入Na2CO3溶液,边加边搅拌,再过滤即可得到碳酸锰。
(l)在第②步中,将上述固体与浓盐酸混合的目的是
(2)有人认为,将第③步中的Na2CO3溶液换成NH4HCO3溶液,也能达到上述目的,但同时有气体生成。请写出加入NH4HCO3溶液时发生的离子反应方程式 。
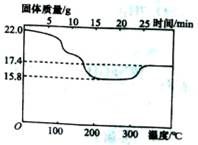
(3)查阅文献,发现第③步中,除生成MnCO3外还有可能生成Mn(OH)2,已知Mn(OH)2暴露在空气中时间稍长,易被氧化成褐色的MnO(OH)2, MnCO3和MnO(OH)2受热最终均分解成MnO2,该小组对上述沉淀的成分提出以下假设,请帮助完成假设:
假设一:全部为MnCO3; 假设二:全部为Mn(OH)2; 假设三:
为验证假设二是否正确,该小组进行了以下研究:
①定性研究:请你完成下表中的内容.
| 实验步骤(不要求写出具体步骤) | 预期的实验现象和结论 |
| 将所得沉淀过滤、洗涤, | |
| | |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
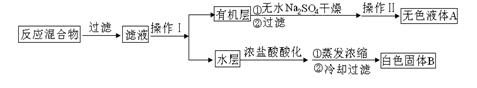
海水是巨大的资源宝库,工业上从海水中提取食盐和溴的过程如下:
(1)可以用淀粉-KI试纸检验操作I中是否有溴生成,其操作方法是___________________。
(2)操作Ⅱ发生反应的离子方程式为_____________;可以用碳酸钠溶液代替操作Ⅱ中的二氧化硫水溶液,生成物中溴的化合价分别为+5和-1价,操作Ⅲ中如果用稀硫酸代替氯气,则操作Ⅲ中发生反应的离子方程式为______。
(3)溴苯是一种化工原料,可以用溴和苯反应合成。实验室合成溴苯的装置示意图如下:

下表为苯、溴和溴苯的相关数据:
| | 苯 | 溴 | 溴苯 |
| 密度/g·cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
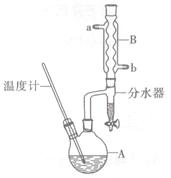
正丁醚常用作有机反应的溶剂。实验室制备正丁醚的反应和主要实验装置如下:
2CH3CH2CH2CH2OH (CH3CH2CH2CH2)2O+H2O
(CH3CH2CH2CH2)2O+H2O
反应物和产物的相关数据如下
| | 相对分子质量 | 沸点/℃ | 密度/(g/cm3) | 水中溶解性 |
| 正丁醇 | 74 | 117.2 | 0.8109 | 微溶 |
| 正丁醚 | 130 | 142.0 | 0.7704 | 几乎不溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
发酵粉是一种化学膨松剂,可由小苏打、臭粉(碳酸氢铵)、明矾中的两种物质组成。某小组为探究不同品牌的发酵粉的化学成分,进行如下实验。
【提出假设】
(1)假设1:由小苏打和臭粉组成
假设2:由小苏打和明矾组成
假设3:由 组成
【方案与流程】
为探究甲品牌的发酵粉的成分,某同学设计如下实验,得到如下现象: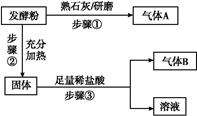
(2)结合步骤①~③分析,气体A为 ,该发酵粉的成分为 (填化学式)。
(3)若步骤①和②操作不变(现象也相同),将步骤③中足量稀盐酸改为足量氯化钡溶液,观察到有白色沉淀生成,能否确定发酵粉的成分并说明理由: 。
(4)乙品牌的发酵粉的化学组成可能为假设2情况,请你设计实验验证。
实验仪器和用品任选,限选试剂:稀盐酸、0.1 mol/L NaOH溶液
写出实验步骤、预期现象和结论。
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量样品溶于足量的盐酸后,将溶液分成两份,分别装入A、B试管中 | |
| 步骤2: | ,证明有Na+,发酵粉中有NaHCO3 |
| 步骤3: | ,结合步骤2中的结论,假设2成立 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
芳香族羧酸通常用芳香烃的氧化来制备。芳香烃的苯环比较稳定,难于氧化,而环上的支链不论长短,在强烈氧化时,最终都氧化成羧基。某同学用甲苯的氧化反应制备苯甲酸。反应原理:
反应试剂、产物的物理常数:
| 名称 | 相对分子质量 | 性状 | 熔点 | 沸点 | 密度 | 溶解度 | ||
| 水 | 乙醇 | 乙醚 | ||||||
| 甲苯 | 92 | 无色液体易燃易挥发 | -95 | 110.6 | 0.8669 | 不溶 | ∞ | ∞ |
| 苯甲酸 | 122 | 白色片状或针状晶体 | 122.4 | 248 | 1.2659 | 微溶 | 易溶 | 易溶 |

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
硫化碱法是工业上制备Na2S2O3的方法之一,反应原理为:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2 (该反应△H>0)
某研究小组在实验室用硫化碱法制备Na2S2O3·5H2O流程如下。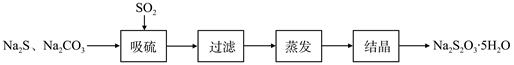
(1)吸硫装置如图所示。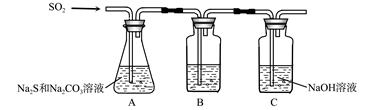
①装置B的作用是检验装置A中SO2的吸收效率,B中试剂是 ,表明SO2吸收效率低的实验现象是B中溶液 。
②为了使SO2尽可能吸收完全,在不改变A中溶液浓度、体积的条件下,除了及时搅拌反应物外,还可采取的合理措施是 、 。(写出两条)
(2)假设本实验所用的Na2CO3含少量NaCl、NaOH,设计实验方案进行检验。(室温时CaCO3饱和溶液的pH=10.2)
限选试剂及仪器:稀硝酸、AgNO3溶液、CaCl2溶液、Ca(NO3)2溶液、酚酞溶液、蒸馏水、pH计、烧杯、试管、滴管
| 序号 | 实验操作 | 预期现象 | 结论 |
| ① | 取少量样品于试管中,加入适量蒸馏水,充分振荡溶解,___________________。 | _______________ | 样品含NaCl |
| ② | 另取少量样品于烧杯中,加入适量蒸馏水,充分搅拌溶解,___________________。 | _______________ | 样品含NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
苯甲酸广泛应用于制药和化工行业。某同学尝试用甲苯的氧化反应制备苯甲酸。反应原理: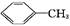 +2KMnO4
+2KMnO4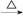
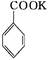 +KOH+
+KOH+
2MnO2↓+H2O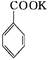 +HCl
+HCl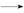
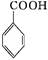 +KCl
+KCl
实验方法:一定量的甲苯和KMnO4溶液在100 ℃反应一段时间后停止反应,按如下流程分离出苯甲酸和回收未反应的甲苯。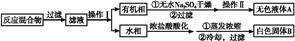
已知:苯甲酸分子量122,熔点122.4 ℃,在25 ℃和95 ℃时溶解度分别为0.3 g和6.9 g;纯净固体有机物一般都有固定熔点。
(1)操作Ⅰ为 ,操作Ⅱ为 。
(2)无色液体A是 ,定性检验A的试剂是 ,现象是 。
(3)测定白色固体B的熔点,发现其在115 ℃开始熔化,达到130 ℃时仍有少量不熔。该同学推测白色固体B是苯甲酸与KCl的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确。请完成表中内容。
| 序号 | 实验方案 | 实验现象 | 结论 |
| ① | 将白色固体B加入水中,加热溶解, | 得到白色晶体和无色滤液 | |
| ② | 取少量滤液于试管中, | 生成白色沉淀 | 滤液含Cl- |
| ③ | 干燥白色晶体, | | 白色晶体 是苯甲酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
海带成分中碘的检验实验方案设计。
(1)干海带灼烧后,将海带灰放至小烧杯中加入适量蒸馏水,搅拌、煮沸冷却、过滤。将滤液分成四份放入四支试管中,并标为1、2、3、4号。
(2)在1号试管中滴入6滴稀硫酸后,再加入约3 mL H2O2溶液,滴入1%淀粉液1~2滴,观察到溶液立刻由褐色变成蓝色,离子方程式为 。
(3)在2号试管中加入2 mL新制的饱和氯水,振荡溶液,观察现象,离子反应方程式为 。2 min后把加入氯水的溶液分成两份。其中甲中再滴入1%淀粉液1~2滴,观察现象为 ,乙溶液中加入2 mL CCl4,振荡萃取,静置2 min后观察现象为 。
(4)在3号试管中加入食用碘盐3 g,振荡使之充分溶解后滴入6滴稀硫酸。在滴入1%淀粉液1~2滴,观察到溶液立刻由无色变成蓝色,相关的离子方程式为 。
(5)在4号试管中加入硝酸银溶液,振荡,再加入稀硝酸溶液。原想利用反应生成黄色沉淀来检验碘离子。通过实验发现生成白色沉淀。用此方法检验碘元素失败。导致此步失败的可能原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com