
【题目】在一定温度下的定容容器中,当下列物理量不再发生变化时,表明反应![]() 已达到化学平衡状态的是( )
已达到化学平衡状态的是( )
①混合气体的压强②混合气体的密度③![]() 的物质的量的浓度④混合气体总物质的量⑤混合气体的平均相对分子质量⑥
的物质的量的浓度④混合气体总物质的量⑤混合气体的平均相对分子质量⑥![]() 与
与![]() 的比值⑦混合气体总质量.
的比值⑦混合气体总质量.
A. ②③⑤⑦B. ③④⑤⑥C. ①③④⑤D. ①②④⑦
【答案】A
【解析】
①该反应的反应前后气体体积不变,所以无论该反应是否达到平衡状态,混合气体的压强始终不变,所以不能根据混合气体的压强判断反应是否达到平衡状态,故①不选;
②该反应是一个反应前后气体的密度改变的反应,当混合气体的密度的密度不变时,该反应达到平衡状态,所以能判断是否达到平衡状态,故②选;
③当该反应达到平衡状态时,B的物质的量的浓度不变,所以能判断是否达到平衡状态,故③选;
④该反应是一个反应前后气体体积不变的化学反应,混合气体的物质的量始终不变,所以不能根据混合气体总物质的量判断反应是否达到平衡状态,故④不选;
⑤该反应是一个反应前后混合气体的平均相对分子质量改变的反应,当混合气体的平均相对分子质量不变时,该反应达到平衡状态,所以能判断是否达到平衡状态,故⑤选;
⑥无论反应是否达到平衡状态,v(C)与v(D)的比值始终不变,所以不能判断是否达到平衡状态,故⑥不选;
⑦该反应是一个反应前后气体质量改变的化学反应,当混合气体总质量不变时,该反应达到平衡状态,所以能判断反应是否达到平衡状态,故⑦选;
故答案为A。


科目:高中化学 来源: 题型:
【题目】甲和乙两位同学探究乙烯与溴的加成反应。
甲同学设计并进行的实验:
①先用乙醇和浓硫酸制取乙烯:CH3CH2OH![]() CH2=CH2↑+H2O;
CH2=CH2↑+H2O;
②将生成的气体直接通入溴水中,发现溶液褪色,即证明乙烯与溴水发生了加成反应;
③乙同学发现在甲同学的实验中,产生的气体有刺激性气味,推测在制得的乙烯中还可能含有少量还原性的杂质气体,由此提出必须先除去杂质,再与溴水反应。
请回答下列问题。
(1)甲同学设计的实验___ (填“能”或“不能”)验证乙烯与溴水发生了加成反应,其理由是_____。
A.使溴水褪色的反应,未必是加成反应
B.使溴水褪色的反应,就是加成反应
C.使溴水褪色的物质,未必是乙烯
D.使溴水褪色的物质,就是乙烯
(2)乙同学推测此乙烯中必定含有一种杂质气体是___,它与溴水反应的化学方程式是______。
(3)乙同学为了先除去杂质气体,再进行推测验证,设计了如下图所示的实验装置。
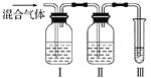
图中各装置盛放的试剂(填序号)是Ⅰ________,Ⅱ________,Ⅲ________。
A.品红溶液 B.氢氧化钠溶液 C.溴水 D.酸性高锰酸钾溶液
(4)为验证这一反应是加成反应而不是取代反应,丙同学提出可用pH试纸来测定反应溶液的酸性,理由是_______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜-锌原电池如图所示,电解质溶液为硫酸铜溶液,电池工作一段时间后,下列说法不正确的是
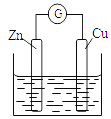
A. 锌电极上的反应为Zn-2e-=Zn2+
B. 电子从锌电极经过硫酸铜溶液流向铜电极
C. 溶液中的SO42-向锌电极移动
D. 铜电极质量增加
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用绿矾(FeSO4·7H2O)为原料制备补血剂甘氨酸亚铁[(H2NCH2COO)2Fe],有关物质性质如下:
甘氨酸(H2NCH2COOH) | 柠檬酸 | 甘氨酸亚铁 |
易溶于水,微溶于乙醇,两性化合物 | 易溶于水和乙醇,有酸性和还原性 | 易溶于水,难溶于乙醇 |
实验过程:
I.配制含0.10molFeSO4的绿矾溶液。
II.制备FeCO3:向配制好的绿矾溶液中,缓慢加入200mL1.1mol/LNH4HCO3溶液,边加边搅拌,反应结束后过滤并洗涤沉淀。
III.制备(H2NCH2COO)2Fe:实验装置如下图(夹持和加热仪器已省略),将实验II得到的沉淀和含0.20mol甘氨酸的水溶液混合后加入C中,然后利用A中反应产生的气体将C中空气排净,接着滴入柠檬酸溶液并加热。反应结束后过滤,滤液经蒸发结晶、过滤、洗涤、干燥得到产品。
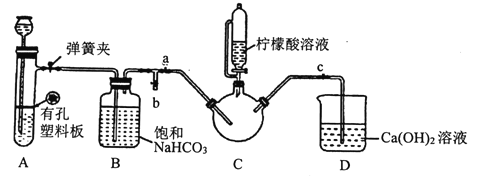
回答下列问题:
(1)实验I中:实验室配制绿矾溶液时,为防止FeSO4被氧化变质,应加入的试剂为____(写化学式)。
(2)实验II中:生成沉淀的离子方程式为________________。
(3)实验III中:
①检查装置A的气密性的方法是_________。
②装置A中所盛放的药品是_______ (填序号)。
a.Na2CO3和稀H2SO4 b.CaCO3和稀H2SO4 c.CaCO3和稀盐酸
③确认c中空气排尽的实验现象是______________。
④加入柠檬酸溶液一方面可调节溶液的pH促进FeCO3溶解,另一个作用是_______。
⑤洗涤实验III中得到的沉淀,所选用的最佳洗涤试剂是___(填序号)。
a.热水 b.乙醇溶液 c.柠檬酸溶液
⑥若产品的质量为17.34g,则产率为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是实验室硫酸试剂标签上的部分内容,据此下列说法正确的是( )

A. 配制稀硫酸定容时俯视刻度线会造成所配溶液浓度偏高
B. 取该硫酸1ml与1ml水混合后,物质的量浓度为9.2mol/L
C. 将该硫酸配成1mol/L的稀硫酸480ml所需的玻璃仪器只有:烧杯、500ml容量瓶、玻璃棒
D. 1molFe与足量的该硫酸反应产生1mol氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1,2二溴乙烷可作汽油抗爆剂的添加剂,常温下是无色液体,密度是2.18克/厘米3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂。在实验中可以用下图所示装置制备1,2二溴乙烷。其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水)。请填写下列空白:
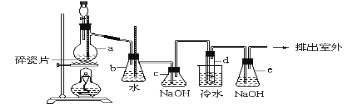
(1)烧瓶a中发生的是乙醇的脱水反应,即消去反应,反应温度是170℃,并且该反应要求温度迅速升高到170℃,否则容易产生副反应。请你写出乙醇的这个消去反应方程式:_______。
(2)写出制备1,2二溴乙烷的化学方程式:_________________________________。
(3)安全瓶b可以以上倒吸,并可以检查实验进行时试管d是否发生堵塞。请写出发生堵塞时瓶b中的现象:_______________________________________。
(4)容器c中NaOH溶液的作用是:_________________________________。
(5)某学生做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超出许多,如果装置的气密性没有问题,试分析其可能的原因__________。
(6)e装置内NaOH溶液的作用是___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、从古至今,铁及其化合物在人类生产生活中的作用发生了巨大变化。
(1)已知:Fe3O4(s) + CO(g)=3FeO(s) + CO2(g)ΔH1= +19.3 kJ·mol-1
3FeO(s) + H2O(g)=Fe3O4(s) + H2(g)ΔH2= -57.2 kJ·mol-1
C(s) + CO2(g)=2 CO(g)ΔH3= +172.4 kJ·mol-1
写出以铁氧化物为催化剂裂解水制氢气总反应的热化学方程式___________。
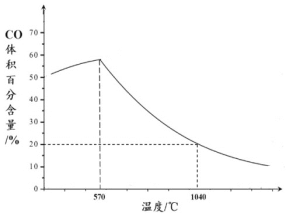
(2)下图表示其它条件一定时,Fe3O4(s)和CO(g)反应达平衡时CO(g)的体积百分含量随温度的变化关系。
①当温度低于570℃时,温度降低,CO的转化率__________(填“增大”、“减小”或“不变”),理由是_______________。
②当温度高于570℃时,随温度升高,反应Fe3O4(s) + CO(g)![]() 3FeO(s) + CO2(g)平衡常数的变化趋势是_________;(填“增大”、“减小”或“不变”);1040℃时,该反应的化学平衡常数的数值是____________。
3FeO(s) + CO2(g)平衡常数的变化趋势是_________;(填“增大”、“减小”或“不变”);1040℃时,该反应的化学平衡常数的数值是____________。
II、汽车尾气中CO、NOx以及燃煤废气中的SO2都是大气污染物,对它们的治理具有重要意义。
(1)吸收SO2和NO,获得Na2S2O4和NH4NO3产品的流程图如图所示(Ce为铈元素)。
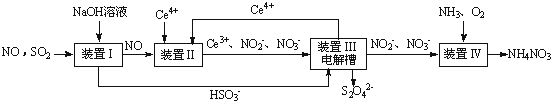
装置Ⅱ中,酸性条件下NO被Ce4+氧化的产物主要是NO3-和NO2-,请写出生成NO3-和NO2-物质的量之比为2:1时的离子方程式:________________________。
(2)装置Ⅲ的作用之一是用质子交换膜电解槽电解使得Ce4+再生,再生时生成的Ce4+在电解槽的____(填“阳极”或“阴极”),同时在另一极生成S2O42-的电极反应式为_________。
(3)已知进入装置Ⅳ的溶液中NO2-的浓度为a g·L-1,要使1.5 m3该溶液中的NO2-完全转化为NH4NO3,至少需向装置Ⅳ中通入标准状况下的氧气___L(用含a代数式表示,结果保留整数,否则不给分)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据金属活动性顺序分析,下列描述或判断错误的是
A.铜活动性不强,故铜不能与硝酸银溶液反应得到金属银
B.在氧气中灼烧时,铁丝比铜丝反应剧烈
C.与同种盐酸反应时,锌片比铁片反应剧烈
D.常温下,在空气中金属镁比铁容易氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】德国化学家凯库勒认为,苯分子的结构中碳碳间以单、双键交替排列结合成环状。为了验证凯库勒的观点,某学生设计了以下实验方案:
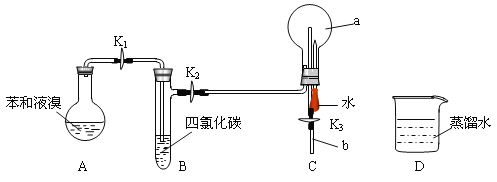
①按如图所示的装置连接好仪器;
②检测装置的气密性;
③在A中加入适量的苯和液溴的混合液体,再加入少量铁粉,塞上橡皮塞,打开K1、K2、K3止水夹;
④待烧瓶C中气体收集满后,将导管b的下端插入烧杯里的水中,挤压预先盛有水的胶头滴管,观察实验现象。
(1)A中所发生反应的反应类型为__________________,能证明凯库勒观点错误的实验现象是_______________________________________。
(2)装置B的作用是______________________________________________。
(3)烧瓶C的容积为500mL,收集气体时,由于空气未排尽,最终水未能充满烧瓶,假设烧瓶中混合气体对氢气的相对密度为37.9,则实验结束后,进入烧杯中的水的体积___ml(空气的相对分子质量以29计算)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com