
 CO(g) +H2(g) ��H= +131.3kJ��mol��1
CO(g) +H2(g) ��H= +131.3kJ��mol��1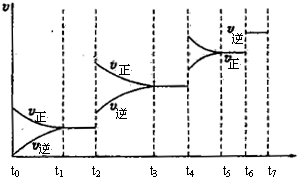


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 pC(g)���ܱ������н��У���ͼ��ʾ�ڲ�ͬ��Ӧʱ��t ʱ���¶�T��ѹǿP��������C�ڻ�����е�����ٷֺ����Ĺ�ϵ���ߡ�
pC(g)���ܱ������н��У���ͼ��ʾ�ڲ�ͬ��Ӧʱ��t ʱ���¶�T��ѹǿP��������C�ڻ�����е�����ٷֺ����Ĺ�ϵ���ߡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
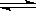 x Q(g) +3R(g)���÷�Ӧ��ƽ��ʱ������2.4mol R�������Q��Ũ��Ϊ0.4 mol/L�������й�������ȷ����
x Q(g) +3R(g)���÷�Ӧ��ƽ��ʱ������2.4mol R�������Q��Ũ��Ϊ0.4 mol/L�������й�������ȷ����| A��xֵΪ2 | B�����������ܶ����� |
| C��ƽ��ʱN��Ũ��Ϊ0.2 mol/L | D��N��ת����Ϊ80% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 z C
z C 2Z(g)+W(g)����H��0���ﵽƽ��ʱ��V��A��=" 1.2a" L��
2Z(g)+W(g)����H��0���ﵽƽ��ʱ��V��A��=" 1.2a" L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2 Z��g�����ﵽƽ��ʱ�������ǵ����ʵ������㣺n��X��+n��Y��= n��Z������Y��ת����Ϊ
2 Z��g�����ﵽƽ��ʱ�������ǵ����ʵ������㣺n��X��+n��Y��= n��Z������Y��ת����Ϊ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
 2SO3(g) ��֪c(SO2)ʼ=0.4mol/L��c(O2)ʼ=1mol/L���ⶨ�÷�Ӧ�ڸ��¶��µ�ƽ�ⳣ��K��19�����жϣ�
2SO3(g) ��֪c(SO2)ʼ=0.4mol/L��c(O2)ʼ=1mol/L���ⶨ�÷�Ӧ�ڸ��¶��µ�ƽ�ⳣ��K��19�����жϣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
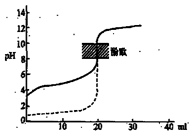
| A����H��0�ķ�Ӧ��������һ�������Է����� |
| B����0.1mol/LNaOH��Һ�ֱ�ζ���ͬ���ʵ���Ũ�Ⱥ���ͬ���������ʹ��ᣬ����ʵ�߱�ʾ���ǵζ���������� |
| C�������£���0.1mol/L��ˮ�У���������NH4Cl���壬��Һ��pH��С |
D�������ܱ������н��еķ�Ӧ3A(g) 2B(g)+C(s)���������������������£��ٳ���һ������A���壬A��ת���ʲ��� 2B(g)+C(s)���������������������£��ٳ���һ������A���壬A��ת���ʲ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
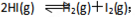 ��
�� ����t1ʱ��ʱ�ﵽƽ�⣬t2ʱ�������²����֣���t3ʱ��ʱ�ִﵽ�µ�ƽ�⣬������һ�仯��ͼ���ǣ�
����t1ʱ��ʱ�ﵽƽ�⣬t2ʱ�������²����֣���t3ʱ��ʱ�ִﵽ�µ�ƽ�⣬������һ�仯��ͼ���ǣ�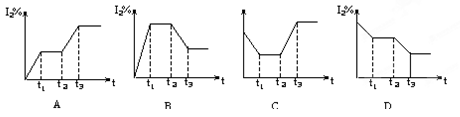
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2NH3����t1ʱ�̴ﵽƽ�⡣�����¶Ⱥ�ѹǿ���䣬��t2ʱ�̣���ͨ��һ����NH3����Ӧ������ʱ��Ĺ�ϵ������ȷ����
2NH3����t1ʱ�̴ﵽƽ�⡣�����¶Ⱥ�ѹǿ���䣬��t2ʱ�̣���ͨ��һ����NH3����Ӧ������ʱ��Ĺ�ϵ������ȷ���� 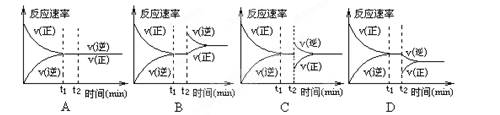
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com