
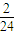 =
=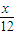 g,则△m=xg-
g,则△m=xg-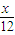 g=
g=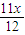 g
g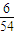 =
=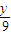 g,则△m=yg-
g,则△m=yg-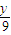 g=
g=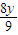 g
g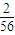 =
=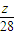 g,则△m=zg-
g,则△m=zg-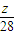 g=
g=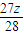 g
g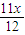 g=
g=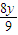 g=
g=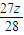 g,故z<x<y,即m(Fe)<m(Mg)<m(Al)
g,故z<x<y,即m(Fe)<m(Mg)<m(Al)

科目:高中化学 来源: 题型:
(2012?天津模拟)下表是25°C时某些弱酸的电离平衡常数,下列说法正确的是( )
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| 溶质 | Na2CO3 | NaHCO3 | Na2SiO3 | Na2SO3 | NaHSO3 | NaClO |
| pH | 11.6 | 9.7 | 12.3 | 10.0 | 4.0 | 10.3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com