
某离子反应涉及H2O、ClO-、NH4+、H+、N2、Cl-六种微粒。其中c(NH4+)随反应进行逐渐减小。下列判断错误的是
A.反应的氧化剂是ClO-
B.消耗l mol还原剂,转移电子3 mol
C.氧化剂与还原剂的物质的量之比为2:3
D.反应后溶液的酸性明显增强
C
【解析】
试题分析:本题考查氧化还原反应的基本概念、氧化还原方程式的配平及电子转移。根据题意知,c(NH4+)随反应进行逐渐减小,则NH4+为反应物,根据原子守恒知,N2为生成物,氮元素的化合价由—3价升高到0价;根据氧化还原反应元素化合价有升高的,必然有元素化合价降低判断,ClO-为反应物,Cl-为生成物,氯元素化合价由+1价降低到—1价;利用化合价升降法及原子守恒和电荷守恒配平的离子方程式为3ClO-+2NH4+=3H2O+2H++N2↑+3Cl-。A、ClO-中氯元素化合价由+1价降低到—1价;反应的氧化剂是ClO-,正确;B、NH4+中氮元素的化合价由—3价升高到0价,作还原剂,消耗l mol还原剂,转移电子3 mol,正确;C、氧化剂与还原剂的物质的量之比为3:2,错误;D、根据反应的离子方程式判断,反应后溶液的酸性明显增强,正确。
考点:考查氧化还原反应


 巧学巧练系列答案
巧学巧练系列答案 课课练江苏系列答案
课课练江苏系列答案科目:高中化学 来源: 题型:阅读理解

| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

| ||
| ||
查看答案和解析>>
科目:高中化学 来源:2013-2014学年山西省高三下学期第一次月考化学试卷(解析版) 题型:选择题
某离子反应中涉及H2O、ClO—、NH4+、H+、N2、Cl—六种微粒。其中N2的物质的量随时间变化的曲线如图所示。下列判断正确的是:
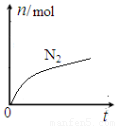
A.该反应的还原剂是Cl—
B.消耗1 mol还原剂,转移6 mol电子
C.氧化剂与还原剂的物质的量之比为2:3
D.反应后溶液的酸性明显增强
查看答案和解析>>
科目:高中化学 来源:2013-2014学年北京市朝阳区高三上学期期末考试化学试卷(解析版) 题型:选择题
某离子反应中涉及H2O、ClO—、NH4+、H+、N2、Cl—六种微粒。其中N2的物质的量随时间变化的曲线如图所示。下列判断正确的是
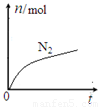
A.该反应的还原剂是Cl—
B.消耗1 mol还原剂,转移6 mol电子
C.氧化剂与还原剂的物质的量之比为2:3
D.反应后溶液的酸性明显增强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com