
| A. | 1 L 0.2 mol•L-1硫酸铁溶液中含有的SO42-数为0.6NA | |
| B. | 60 g SiO2晶体中含有2NA个Si-O键 | |
| C. | 1L浓度为1mol•L-1的Na2CO3溶液中含有NA个CO32- | |
| D. | 25℃时,pH=13的Ba(OH)2溶液中含有的OH-数目为0.1NA |
分析 A.1mol硫酸铁完全电离生成3mol硫酸根离子;
B.1molSiO2晶体存在4molSi-O键;
C.碳酸根离子为弱酸根离子,水溶液中部分发生水解;
D.溶液体积未知.
解答 解:A.硫酸铁为强电解质,完全电离,1 L 0.2 mol•L-1硫酸铁溶液中含有硫酸铁为0.2mol,电离产生的SO42-数为0.6NA,故A正确;
B.1molSiO2晶体存在4molSi-O键,所以60gSiO2晶体即1mol含有4molSi-O键,故B错误;
C.碳酸根离子为弱酸根离子,水溶液中部分发生水解,所以1L浓度为1mol•L-1的Na2CO3溶液中含有小于NA个CO32-,故C错误;
D.溶液体积未知,无法计算溶液中氢氧根离子个数,故D错误;
故选:A.
点评 本题考查了阿伏伽德罗常数的有关计算,明确电解质电离方式、二氧化硅结构特点、盐类水解规律是解题关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | NH4+、CO32-、K+、Na+ | B. | Na+、Ba2+、Cl-、HCO3- | ||
| C. | NO3-、Cu2+、K+、SO42- | D. | K+,Na+,Cl-,NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
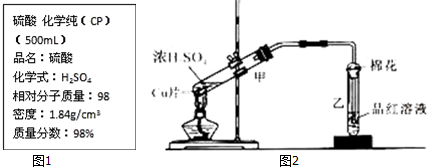
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
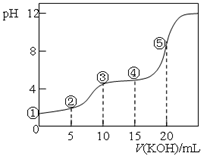 常温下,用0.10mol•L-1 KOH溶液滴定 10.00mL 0.10mol•L-1H2C2O4(二元弱酸)溶液 所得滴定曲线如图(混合溶液的体积可看成混合前溶液的体积之和).下列说法正确的是( )
常温下,用0.10mol•L-1 KOH溶液滴定 10.00mL 0.10mol•L-1H2C2O4(二元弱酸)溶液 所得滴定曲线如图(混合溶液的体积可看成混合前溶液的体积之和).下列说法正确的是( )| A. | 点①所示溶液中:c(H+)/c(OH-)=1012 | |
| B. | 点②所示溶液中:c(K+)+c(H+)=c(HC2O4-)+c(C2O42-)+c(OH-) | |
| C. | 点③所示溶液中:c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.05mol•L-1 | |
| D. | 点⑤所示溶液中:c(K+)>c(HC2O4-)>c(C2O42-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 原子半径大小:Na>S>O | B. | 还原性强弱:F->Cl->Br->I- | ||
| C. | 碱性强弱:KOH>NaOH>LiOH | D. | 气态氢化物稳定性:HBr>HCl>HF |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

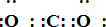 ;写出物质E的电子式:
;写出物质E的电子式: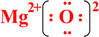 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 检验某有机物中是否含有醛基:取少量水溶液于试管中,加入过量氢氧化钠溶液和新制Cu(OH)2悬浊液,加热至沸腾,看是否有砖红色沉淀生成 | |
| B. | 提纯混有少量CaCl2的NaCl固体:将固体配成溶液,加入稍过量Na2CO3溶液至沉淀完全,过滤,再向滤液中加入稍过量盐酸,蒸发结晶 | |
| C. | 验证某无色溶液中存在SO42-:向试管中加入少量待测溶液,然后加入少量BaCl2溶液,后加入足量稀硝酸,观察到最后仍有白色沉淀生成即可 | |
| D. | 验证炭与浓硫酸反应产生的CO2:将炭与浓硫酸反应生成的气体通入盛有澄清石灰水的试管中,观察是否有白色沉淀生成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com