
| A. | 水由液态变为玻璃态,体积缩小 | |
| B. | 水由液态变为玻璃态,体积膨胀 | |
| C. | 玻璃态是水的一种特殊状态晶体 | |
| D. | 玻璃态水是水分子在空间有规则排列形成的 |
分析 A、由玻璃态的水密度与普通液态水的密度相同,质量不变;
B、根据玻璃态水与液态水密度的关系考虑;
C、根据水的状态来分析;
D、根据玻璃态的水无固定形状.
解答 解:A、由玻璃态的水密度与普通液态水的密度相同,质量不变,所以体积不变,故A错误;
B、由玻璃态的水密度与普通液态水的密度相同,质量不变,所以体积不变,故B错误;
C、由水的状态除了气、液和固态外,还有玻璃态,可知玻璃态是水的一种特殊状态,故C正确;
D、玻璃态的水无固定形状,所以在空间无规则排列,故D错误.
故选C.
点评 本题属于信息给予题,解答本题的关键是抓住题干中重要信息:玻璃态的水与普通液态水的密度相同,玻璃态的水无固定形状、不存在晶体结构.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
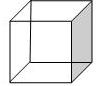 “立方烷”是一祌新合成的烃,其分子为正立方体结构,其碳架结构如图所示
“立方烷”是一祌新合成的烃,其分子为正立方体结构,其碳架结构如图所示 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 实验装置 | 现象 |
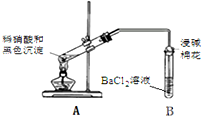 | 1.A试管中黑色沉淀逐渐溶解 2.A试管内上方出现红棕色气体 3.B试管中出现白色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
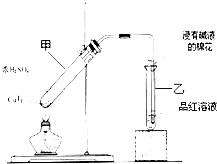 某教师在课堂上用右图所示的装置来验证浓硫酸与铜是否发生反应,并探讨反应所产生气体的性质.请回答下列问题:
某教师在课堂上用右图所示的装置来验证浓硫酸与铜是否发生反应,并探讨反应所产生气体的性质.请回答下列问题: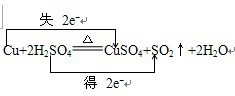 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C的质量分数降低 | B. | 平衡向右移动 | C. | B的转化率升高 | D. | x+y<z |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丙烷的分子式是C3H6 | |
| B. | 丙烷分子中的碳原子在一条直线上 | |
| C. | 丙烷在光照条件下能够和氯气发生加成反应 | |
| D. | 丙烷的熔点比乙烷高 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com