
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
分析 先根据烷烃的条件,确定烷烃的分子式,然后再根据官能团位置异构确定烯烃的同分异构体.
解答 解:第一步:确定该烷烃碳原子个数
①主链为4个碳原子的烷烃,其支链只能是甲基(不可能是乙基,否则主链超过4个碳原子).
②主链为4个碳原子的烷烃,支链数最多4个(下面的0,是指该物质只有一种,没有同分异构体)
甲基的个数 同分异构体
1个 0
2个 2
3个 0
4个 0
③结论:该烷烃总共有6个碳原子,
第二步:分析烯烃的同分异构体数目
①双键在1号位,有以下3种
C=C-C-C
1 2 3 4
2-乙基丁烯、2,3-二甲基丁烯、3,3-二甲基丁烯
②双键在2号位,有1种
C-C=C-C
1 2 3 4
2,3-二甲基-2-丁烯
结论:共有4种.
故选C.
点评 本题主要考查了同分异构体的写法,能熟练书写1-6个碳的碳链异构;常规的书写方法:碳链异构→位置异构→类别异构.


科目:高中化学 来源: 题型:选择题
| A. | CH4>SiH4>GeH4>SnH4 | B. | KCl>NaCl>MgCl2>MgO | ||
| C. | Rb>K>Na>Li | D. | 金刚石>SiC>Si>S |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 编号 | 实验目的 | 碳粉/g | 铁粉/g | 醋酸/% |
| ① | 为以下实验作参照 | 0.5 | 2.0 | 90.0 |
| ② | 醋酸浓度的影响 | 0.5 | 36.0 | |
| ③ | 0.2 | 2.0 | 90.0 |
| 编号 | 实验操作 | 预期现象和结论 |
| ① | 在试管中加入少量该FeCl3溶液和过量(填少量、过量)的KI溶液. | 深红色如期出现 |
| ② | 将试管中的混合溶液转移至分液漏斗(填仪器)中,倒入一定量的CCl4,塞住活塞,充分振荡(萃取),静置. | 液体分层,上层接近无色,下层紫红色 |
| ③ | 打开活塞,先放出下层液体,再从分液漏斗的上口中倒出水层于试管中,加入KSCN溶液 | 出现血红色,则反应后的混合物中含Fe3+,进而证明这的确是一个可逆反应;反之则不含Fe3+,进而证明不是一个可逆反应 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 131I与127I互为同位素 | |
| B. | 相同物质的量的131I与127I的质子数不同 | |
| C. | 131I与127I 是两种不同核素 | |
| D. | 日用碘盐对预防碘辐射起不到有效作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分液、萃取、蒸馏 | B. | 萃取、蒸馏、分液 | C. | 分液、蒸馏、萃取 | D. | 蒸馏、萃取、分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
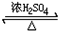 CH3COOC2H5+H2O反应类型取代反应;
CH3COOC2H5+H2O反应类型取代反应; 反应类型加聚反应.
反应类型加聚反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Zn为正极,Ag2O为负极 | |
| B. | Zn为负极,Ag2O为正极 | |
| C. | 原电池工作时,正极区溶液pH值减小 | |
| D. | 原电池工作时,负极区溶液pH值增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com