
| A. | 甲苯分子中所有原子可能共平面 | |
| B. | 只有水就能区别苯、酒精、四氯化碳这三种无色液体 | |
| C. | 在化学反应过程中,发生物质变化的同时一定发生能量变化 | |
| D. | 埋在潮湿土壤里的铁管比埋在干燥土壤里的铁管更难被腐蚀 |
分析 A.根据甲烷为正四面体结构分析甲苯中所有氢原子能否共平面;
B.水与苯混合分层后有机层在上层,四氯化碳与水混合后有机层在下层,乙醇与水混合不分层;
C.化学反应中反应物断键要吸热,生成物成键要放热;
D.金属的腐蚀分为电化学腐蚀和普通化学腐蚀,电化学腐蚀速率快与普通的化学腐蚀.
解答 解:A.由于甲烷为正四面体结构,甲苯可以看作甲烷中1个H被苯基取代,所以甲苯中所有原子不可能共平面,故A错误;
B.水与苯混合分层后有机层在上层,四氯化碳与水混合后有机层在下层,乙醇与水混合不分层,现象不同,可鉴别,故B正确;
C.化学反应中反应物断键要吸热,生成物成键要放热,所以化学反应过程中,不仅有物质的变化,同时还伴随有能量的变化,故C正确;
D.铁管在潮湿的环境下容易形成原电池,加快铁的腐蚀,与电化学腐蚀有关,故D错误.
故选BC.
点评 本题主要考查的是常见有机物的结构、有机物的鉴别、化学反应实质以及化学腐蚀与电化学腐蚀等,综合性较强,难度不大,需要认真整理.


科目:高中化学 来源: 题型:解答题
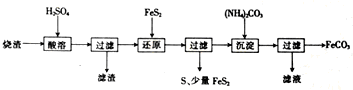
| 离子 | 离子浓度(mol?L-1) | |
| 还原前 | 还原后 | |
| Fe2+ | 0.10 | 2.50 |
| SO42- | 3.50 | 3.70 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
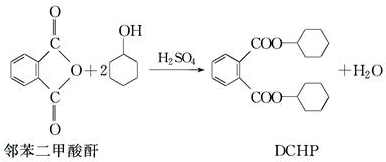
| A. | 邻苯二甲酸酐属于酸性氧化物 | |
| B. | 环己醇分子中所有的原子可能共平面 | |
| C. | DCHP能发生加成、取代、消去反应 | |
| D. | 1molDCHP最多可与含2molNaOH的烧碱溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
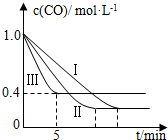 利用甲烷与水反应制备氢气,因原料廉价产氢率高,具有实用推广价值.
利用甲烷与水反应制备氢气,因原料廉价产氢率高,具有实用推广价值.| 编号 | 温度 | 压强 | c始(CO) | c始(H2O) |
| Ⅰ | 530℃ | 3MPa | 1.0mol•L-1 | 3.0mol•L-1 |
| Ⅱ | X | Y | 1.0mol•L-1 | 3.0mol•L-1 |
| Ⅲ | 630℃ | 5MPa | 1.0mol•L-1 | 3.0mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子式为C5H12的有机物化学性质相似 | |
| B. | 相同条件下,等质量的甲烷按a、b两种途径完全转化,途径a比b放出更多热量 | |
| C. | 需加热才能发生的反应都是吸热反应 | |
| D. | 电镀时待镀金属作阳极,镀层金属作阴极 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 的链节为
的链节为 .其单体的结构简式分别为
.其单体的结构简式分别为 、
、 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生石灰-Ca(OH)2 | B. | 重晶石-BaCO3 | C. | 绿矾-CuSO4•5H2O | D. | 小苏打-NaHCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将人群向低处疏散 | B. | 将人群逆风向疏散 | ||
| C. | 用浸有水的毛巾捂住口鼻 | D. | 向泄露地点撒一些石灰 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
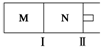 M、N两个容器中均发生反应:A(g)+3B(g)?2C(g)△H=-192kJ•mol-1.隔板Ⅰ固定不动,活塞Ⅱ可自由移动.向M、N中,都通入x mol A和y mol B的混合气体,初始M、N容积相同,保持温度不变.下列说法正确的是( )
M、N两个容器中均发生反应:A(g)+3B(g)?2C(g)△H=-192kJ•mol-1.隔板Ⅰ固定不动,活塞Ⅱ可自由移动.向M、N中,都通入x mol A和y mol B的混合气体,初始M、N容积相同,保持温度不变.下列说法正确的是( )| A. | 若x:y=1:2,则平衡时,M中的转化率:A>B | |
| B. | 若x:y=1:3,当M中放出热量172.8 kJ时,A的转化率为90% | |
| C. | 若x=1.2,y=1,N中达到平衡时体积为2 L,含有C 0.4 mol,再通入0.4mol A时,v正>v逆 | |
| D. | 起始时,分别向M、N两个容器中加入1molA和1molC,达到平衡时,容器M、N中物质A的体积分数:M<N |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com