
| A. | 中子数为18的氯原子:${\;}_{17}^{35}Cl$ | B. | 二氧化碳分子的比例模型: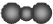 | ||
| C. | HClO的电子式: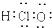 | D. | 甲烷分子的球棍模型: |
分析 A.中子数为20,则质量数为37,元素符号左上角的数字为质量数、左下角数字表示质子数;
B.比例模型主要体现C、O原子的相对体积大小及空间结构;
C.次氯酸的中心原子为O原子,不存在氢氯键;
D.甲烷的球棍模型用小球和短棍表示,图示为甲烷的比例模型.
解答 解:A.氯元素的质子数为17,中子数为20的氯原子的质量数为37,该原子的正确表示方法为:3517Cl,故A正确;
B.二氧化碳分子中碳原子半径大于氧原子半径,二氧化碳正确的比例模型为: ,故B错误;
,故B错误;
C.次氯酸为共价化合物,H原子最外层1个电子,Cl原子最外层7个电子,O原子最外层6个电子,则其电子式为 ,故C错误;
,故C错误;
D. 为甲烷的比例模型,甲烷的球棍模型为:
为甲烷的比例模型,甲烷的球棍模型为: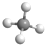 ,故D错误;
,故D错误;
故选A.
点评 本题考查了常见化学用语的判断,题目难度中等,注意掌握电子式、结构简式图、比例模型与球棍模型、元素符号的表示方法,试题有利于题干学生规范答题的能力.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①和② | B. | ②和④ | C. | ④和⑥ | D. | ③和⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (CH3)3COH的名称:2,2二甲基乙醇 | B. | 乙醛的结构式:CH3CHO | ||
| C. | CH4分子的比例模型: | D. | 聚丙烯的结构简式为: |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
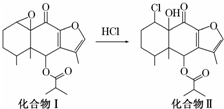 我国科研人员以蹄叶囊青为原料先制得化合物Ⅰ再转化为具有抗癌抑菌活性的倍半萜化合物Ⅱ,有关转化如图所示,下列有关说法不正确的是( )
我国科研人员以蹄叶囊青为原料先制得化合物Ⅰ再转化为具有抗癌抑菌活性的倍半萜化合物Ⅱ,有关转化如图所示,下列有关说法不正确的是( )| A. | 化合物Ⅰ能使酸性KMnO4溶液褪色 | |
| B. | 化合物Ⅰ分子中含有6个手性碳原子 | |
| C. | 化合物Ⅱ一定条件下能发生取代、消去及加成反应 | |
| D. | 检验化合物Ⅱ中是否含化合物Ⅰ可用Br2的CCl4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
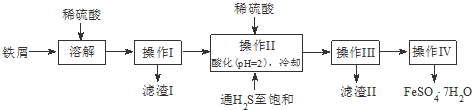
| 饱和H2S溶液 | SnS沉淀完全 | FeS开始沉淀 | FeS沉淀完全 | |
| pH值 | 3.9 | 1.6 | 3.0 | 5.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 生成1mol ClO2,转移电子数为NA | B. | 该反应为复分解反应 | ||
| C. | H2SO4发生氧化反应 | D. | NaClO3是氧化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
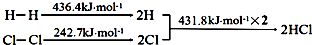
| A. | H-H键比Cl-Cl键稳定 | |
| B. | △H=-184.5 kJ•mol-1 | |
| C. | 正反应活化能比逆反应活化能高 | |
| D. | 在相同条件下,1mol H2(g)和1mol Cl2(g)分别在点燃和光照条件下反应生成2mol HCl(g),重新恢复到原来的状态时△H相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com