
【题目】将Cu片放入0.1 mol·L1 FeCl3溶液中,反应一定时间后取出Cu片,溶液中c(Fe3+)∶c(Fe2+)=2∶1,则Cu2+与原溶液中的Fe3+的物质的量之比为( )
A. 4∶1 B. 1∶4 C. 1∶6 D. 6∶1
科目:高中化学 来源: 题型:
【题目】常温下,0.1 mol/L的H2C2O4溶液中H2C2O4、HC2O4-、C2O42-三者中所占物质的量分数(分布系数)随pH变化的关系如右图所示。下列表述不正确的是
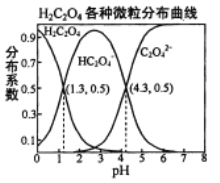
A. HC2O4-![]() H++C2O42-,K=1×10-4.3
H++C2O42-,K=1×10-4.3
B. 将等物质的量的NaHC2O4、Na2C2O4溶于水中,所得溶液pH恰好为4.3
C. 常温下HF的K=1×10-3.4,将少量H2C2O4溶液加入到足量NaF溶液中,发生的反应为:H2C2O4+F-=HF+HC2O4-
D. 在0.1 mol/L NaHC2O4溶液中,各离子浓度大小关系为:c(Na+)>c(HC2O4-)>c(H+)>c(C2O42-)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温条件下在醋酸、醋酸钠混合溶液中,当c(CH3COOH)+c(CH3COO-)=0.lmol.L-1时,c(CH3COOH)、c(CH3COO-)与pH的关系如图所示。下列有关叙述正确的是

A.pH=5.5的溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-)
B.向W点所表示的1.0L溶液中通人0.05molHCl气体(溶液体积变化可忽略):c(H+)=c(CH3COOH)+c(OH-)
C.W点所表示的溶液中:c(Na+)+c(H+)=c(CH3COOH)+c(OH)-
D.pH=3.5的溶液中:c(Na+)+c(H+)+c(OH-)+c(CH3COOH)=0.1mol.L-l
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将适量铜粉放入硫酸铁溶液中,完全反应后,溶液中的Cu2+和Fe3+的物质的量浓度相等,则已反应的Fe3+和原溶液中Fe3+总物质的量之比是
A.2 :3 B.3 :2 C.2 :5 D.1 :2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】+3价Co的八面体配合物CoClm·nNH3,中心原子的配位数为6,若1 mol配合物与AgNO3作用生成2 mol AgCl沉淀,则m和n的值是( )
A. m=1、n=5B. m=3、n=3C. m=3、n=4D. m=3、n=5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学研究性学习小组需配制含有NH![]() 、Cl-、K+、SO42—的植物培养液450 mL,且要求该培养液中c(Cl-)=c(K+)=c(SO42—)=0.4 mol·L-1。实验室提供的药品有:NH4Cl、KCl、(NH4)2SO4、K2SO4和蒸馏水;提供的实验仪器有:①药匙 ②托盘天平 ③烧杯 ④玻璃棒 ⑤胶头滴管 ⑥量筒。请回答下列问题:
、Cl-、K+、SO42—的植物培养液450 mL,且要求该培养液中c(Cl-)=c(K+)=c(SO42—)=0.4 mol·L-1。实验室提供的药品有:NH4Cl、KCl、(NH4)2SO4、K2SO4和蒸馏水;提供的实验仪器有:①药匙 ②托盘天平 ③烧杯 ④玻璃棒 ⑤胶头滴管 ⑥量筒。请回答下列问题:
(1)该植物培养液中,NH![]() 的物质的量浓度为_____________。
的物质的量浓度为_____________。
(2)该研究小组配制该植物培养液时,还须用到的实验仪器是________(填字母)。
A.450 mL容量瓶 B.500 mL容量瓶 C.两个250 mL容量瓶
(3)甲同学用KCl和(NH4)2SO4两种物质进行配制,则需称取m(KCl)=____g,m[(NH4)2SO4]=___g。
(4)若配制该培养液的其他操作均正确,则下列错误操作将使所配制溶液的浓度偏低的是_________(填选项)。
A.将溶液转移至容量瓶后,未洗涤烧杯和玻璃棒
B.将烧杯内的溶液向容量瓶中转移时,因操作不当使部分溶液溅出容量瓶
C.用胶头滴管向容量瓶中加水时,溶液的凹液面高于容量瓶刻度线
D.用胶头滴管向容量瓶中加水时,俯视容量瓶刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,对于可逆反应:X(g)+3Y(g) ![]() 2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.08 mol ·L-1,则下列判断正确的是( )
2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.08 mol ·L-1,则下列判断正确的是( )
A. c1∶c2=1∶3
B. 平衡时Y和Z的生成速率之比为2∶3
C. X、Y的转化率之比为1:3
D. c1的取值范围为0.04 mol·L-1<c1<0.14 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在组成生物体的各种元素中,下列组合中均属于大量元素的是
A. C、H、0、Zn B. P、S、Mg C. C、H、K、Fe D. O、N、P、Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】信息时代产生的大量电子垃圾对环境构成了极大的威胁。某“变废为宝”学生探究小组将一批废弃的线路板简单处理后,得到含 70%Cu、25%Al、4%Fe 及少量 Au、Pt 的合金,并设计出由合金制备硫酸铜和硫酸铝晶体的路线:

请回答下列问题:
(1)第①步 Cu与酸反应的离子方程式为__________________,得到滤渣 1的主要成分为_______________。
(2)第②步加 H2O2的作用是做氧化剂,将溶液中的 Fe2+氧化为 Fe3+,用 H2O2做氧化剂的优点是____________________。
(3)滤渣 2的主要成分是 Al(OH)3和 Fe(OH)3,在生产中如何分离两种沉淀,写出反应的离子方程式______________。
(4)第③步蒸发所需玻璃仪器为__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com