
在下述条件下,一定能大量共存的离子组是()
A. 无色透明的水溶液中:K+、Ba2+、I﹣、MnO4﹣
B. 含有大量NO3﹣的水溶液中:NH4+、Fe2+、SO42﹣、H+
C. c(HCO3﹣)=0.1mol•L﹣1的溶液中:Na+、K+、CO32﹣、Br﹣
D. 强碱性溶液中:ClO﹣、S2﹣、HSO3﹣、Na+
考点: 离子共存问题.
专题: 离子反应专题.
分析: A、从I﹣离子的还原性和MnO4﹣离子的氧化性考虑能共存;
B、在酸性溶液中NO3﹣离子具有强氧化性与具有还原性的Fe2+离子不能大量共存;
C、判断各离子之间能否发生复分解、水解、氧化等反应;
D、HSO3﹣离子在碱性条件下不能大量共存.
解答: 解:A、I﹣离子具有还原性与具有氧化性的MnO4﹣离子发生氧化还原反应而不能大量共存,故A错误;
B、在酸性溶液中NO3﹣离子具有强氧化性与具有还原性的Fe2+离子发生氧化还原反应而不能大量共存,故B错误;
C、在c(HCO3﹣)=0.1mol•L﹣1的溶液中,四种离子不发生任何反应,能大量共存,故C正确.
D、HSO3﹣离子在碱性条件下不能大量共存,故D错误.
故选C.
点评: 本题考查离子共存问题,题目难度不大,做题时注意离子的性质和溶液的酸碱性等问题.


科目:高中化学 来源: 题型:
在水溶液中能大量共存,且加入过量稀硫酸时,有气体生成的是()
A. Na+、Ag+、CO32﹣、Cl﹣ B. K+、Ba2+、SO42﹣、Cl﹣
C. Na+、K+、CO32﹣、Cl﹣ D. H+、K+、Cl﹣、HCO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与社会、生活密切相关,对下列现象或事实的解释正确的是()
选项 现象或事实 解释
A 用热的烧碱溶液洗去油污 Na2CO3可直接与油污反应
B 漂白粉在空气中久置变质 漂白粉中的CaCl2与空气中的CO2反应生成CaCO3
C 施肥时,草木灰(有效成分为K2CO3)不能与NH4Cl混合使用 K2CO3与NH4Cl反应生成氨气会降低肥效
D FeCl3溶液可用于铜质印刷线路板制作 FeCl3能从含Cu2+的溶液中置换出铜
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示,杠杆AB两端分别用导线挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其保持平衡,然后小心地向盛水的水槽中滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是()
A. 杠杆为导体或绝缘体时,均为A端高B端低
B. 杠杆为导体或绝缘体时,均为A端低B端高
C. 当杠杆为导体时,A端低B端高;杠杆为绝缘体时,A端高B端低
D. 当杠杆为导体时,A端高B端低;杠杆为绝缘体时,A端低B端高
查看答案和解析>>
科目:高中化学 来源: 题型:
如图1所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜.请按要求回答相关问题:
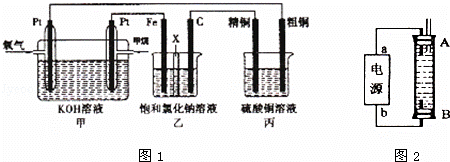
(1)甲烷燃料电池负极电极反应式是: ;
(2)石墨电极(C)的电极反应式为 ;
(3)若在标准状况下,有2.24L氧气参加反应,则乙装置中铁电极上生成的气体体积为 L;丙装置中阴极析出铜的质量为 g;
(4)某同学利甲烷燃料电池设计电解法制取漂白液或Fe(OH)2的实验装置(如图2所示).
若用于制漂白液时a为电池负极,电解质溶液最好用 .
若用于制Fe(OH)2,使用硫酸钠做电解质溶液,阳极选用铁作电极.
查看答案和解析>>
科目:高中化学 来源: 题型:
高铁酸钾是一种高效绿色水处理剂,其工业制备的反应原理为2Fe(OH)3+3KClO+4KOH═2K2FeO4+3KCl+5H2O,下列说法正确的是()
A. 制备高铁酸钾用ClO﹣做还原剂
B. 制备高铁酸钾时1 mol Fe(OH)3得到3 mol 电子
C. 高铁酸钾中铁的化合价为+7
D. 用高铁酸钾处理水时,其还原产物能水解产生具有强吸附能力的胶体
查看答案和解析>>
科目:高中化学 来源: 题型:
用FeCl3溶液腐蚀印刷电路板上的铜,所得的溶液中加入铁粉.对加入铁粉充分反应后的溶液分析合理的是()
A. 若无固体剩余,则溶液中一定有Fe3+
B. 若有固体存在,则溶液中一定有Fe2+
C. 若溶液中有Cu2+,则一定没有固体析出
D. 若溶液中有Fe2+,则一定有Cu析出
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于化学基本原理和基本概念的几点认识中正确的是()
A. 胶体区别于其他分散系的本质特征是丁达尔现象
B. 强电解质溶液的导电能力强于弱电解质溶液
C. NaCl既可表示氯化钠的组成,又能表示其分子式
D. 一般认为沉淀离子浓度小于1.0×10﹣5mol/L时,则认为已经沉淀完全
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述符合实验事实的是()
A. 金属钠在空气中燃烧生成氧化钠
B. 金属钠在空气中燃烧生成白色的Na2O2
C. 金属钠在水中可以生成使酚酞变红的物质
D. 金属钠与水反应放出氧气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com