苯乙烯是重要的基础有机原料.工业中用乙苯(C
6H
5-CH
2CH
3)为原料,采用催化脱氢的方法制取苯乙烯(C
6H
5-CH=CH
2)的反应方程式为:
C
6H
5-CH
2CH
3(g)?C
6H
5-CH=CH
2(g)+H
2(g)△H
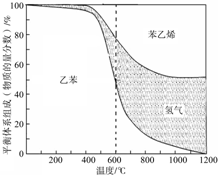
1(1)向体积为VL的密闭容器中充入a mol乙苯,反应达到平衡状态时,平衡体系组成(物质的量分数)与温度的关系如图所示:
由图可知:在600℃时,平衡体系中苯乙烯的物质的量分数为25%,则:
①氢气的物质的量分数为
;乙苯的物质的量分数为
;
②乙苯的平衡转化率为
;
③计算此温度下该反应的平衡常数(请写出计算过程).
(2)分析上述平衡体系组成与温度的关系图可知:△H
1
0(填“>、=或<”).
(3)已知某温度下,当压强为101.3kPa时,该反应中乙苯的平衡转化率为30%;在相同温度下,若反应体系中加入稀释剂水蒸气并保持体系总压为101.3kPa,则乙苯的平衡转化率
30%(填“>、=、<”).
(4)已知:
3C
2H
2(g)?C
6H
6(g)△H
2C
6H
6(g)+C
2H
4(g)?C
6H
5-CH
2CH
3(g)△H
3则反应3C
2H
2(g)+C
2H
4(g)?C
6H
5-CH=CH
2(g)+H
2(g)的△H=
.

 苯乙烯是重要的基础有机原料.工业中用乙苯(C6H5-CH2CH3)为原料,采用催化脱氢的方法制取苯乙烯(C6H5-CH=CH2)的反应方程式为:
苯乙烯是重要的基础有机原料.工业中用乙苯(C6H5-CH2CH3)为原料,采用催化脱氢的方法制取苯乙烯(C6H5-CH=CH2)的反应方程式为:

 快捷英语周周练系列答案
快捷英语周周练系列答案