
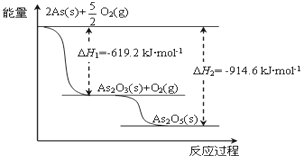
 氮是一种非常重要的元素,它的单质和化合物应用广泛,在科学技术和生产中有重要的应用.砷(As)位于周期表中的第4周期,与氮元素属同一主族元素,其广泛分布于自然界.试回答下列问题:
氮是一种非常重要的元素,它的单质和化合物应用广泛,在科学技术和生产中有重要的应用.砷(As)位于周期表中的第4周期,与氮元素属同一主族元素,其广泛分布于自然界.试回答下列问题:| m |
| M |
| N |
| NA |
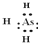 ,非金属性As<N,元素的非金属性越强,对应的氢化物越稳定,则稳定性比NH3弱,
,非金属性As<N,元素的非金属性越强,对应的氢化物越稳定,则稳定性比NH3弱,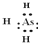 ;弱;
;弱;| 46g |
| 46g/mol |


科目:高中化学 来源: 题型:
| A、WX2分子中所有原子最外层都已满足8电子结构 |
| B、WX2、ZX2的化学键类型相同 |
| C、原子半径大小顺序为:X<W<Y<Z |
| D、乙醇、乙酸、葡萄糖、油脂中均含W、X两种元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、(a) 可用于定容并量取15.00 mL NaOH溶液 |
| B、(b)装置放置一段时间后,饱和CuSO4溶液中出现蓝色晶体 |
| C、(c)可用于高温煅烧石灰石 |
| D、(d)可用于易溶于水的尾气吸收 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 燃煤废气中的氮氧化物(NOx)、二氧化碳等气体,常用下列方法处理,以实现节能减排、废物利用等.
燃煤废气中的氮氧化物(NOx)、二氧化碳等气体,常用下列方法处理,以实现节能减排、废物利用等.| 催化剂 |
| 1 |
| 6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 水煤气(CO 和H2)是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:
水煤气(CO 和H2)是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 模拟海水中的 离子浓度/mol?L-1 | Na+ | Mg2+ | Ca2+ | Br- | Cl- | HCO3- |
| 0.439 | 0.050 | 0.011 | 0.008 | 0.552 | 0.001 |
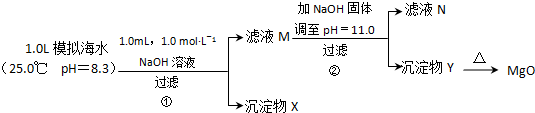
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图中各物质均由常见元素(原子序数≤20)组成.已知A、B、K为单质,且在常温下A和K为气体,B为固体.D为常见的无色液体.I是一种常用的化肥,在其水溶液中滴加AgNO3溶液有不溶于稀HNO3的白色沉淀产生.J是一种实验室常用的干燥剂.它们的相互转化关系如图所示(图中反应条件未列出).
如图中各物质均由常见元素(原子序数≤20)组成.已知A、B、K为单质,且在常温下A和K为气体,B为固体.D为常见的无色液体.I是一种常用的化肥,在其水溶液中滴加AgNO3溶液有不溶于稀HNO3的白色沉淀产生.J是一种实验室常用的干燥剂.它们的相互转化关系如图所示(图中反应条件未列出).查看答案和解析>>
科目:高中化学 来源: 题型:
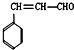 和化合物Ⅱ
和化合物Ⅱ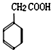 在一定条件下发生反应能生成化合物Ⅲ
在一定条件下发生反应能生成化合物Ⅲ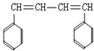 ,请回答以下问题.
,请回答以下问题.查看答案和解析>>
科目:高中化学 来源: 题型:
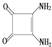 )代替两个NH3与铂配位,则生成的产物
)代替两个NH3与铂配位,则生成的产物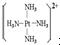 和氯化钠溶液反应制取
和氯化钠溶液反应制取 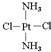 的离子反应方程式
的离子反应方程式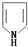 )及呋喃(
)及呋喃(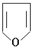 )形成的配合物[Pt(C4H4O)(C4H5N)Cl2],写出其结构简式
)形成的配合物[Pt(C4H4O)(C4H5N)Cl2],写出其结构简式查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com