
【题目】某铁红涂料中添加有CuO或FeO中的一种,为探究添加物的成分设计如下实验方案。
(1)请写出实验步骤、预期现象,对应的离子方程式。
(限选试剂:铁粉、3mol/LH2SO4、0.1mol/L酸性KMnO4溶液、10%H2O2、KSCN溶液)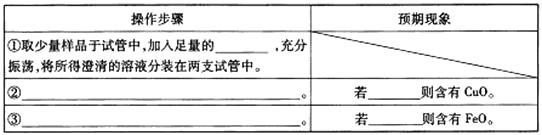
① , ② , , ③ ,
④操作步骤③中反应的离子方程式为。
(2)经分析该铁红涂料中有FeO,为测定铁红中铁的质量分数,兴趣小组的同学称量11.6g该铁红涂料进行了如下实验。
已知:气体由草酸晶体受热分解得到:H2C2O4·2H2O ![]() CO2↑+CO↑+3H2O。且除铁红外所用试剂均过量。
CO2↑+CO↑+3H2O。且除铁红外所用试剂均过量。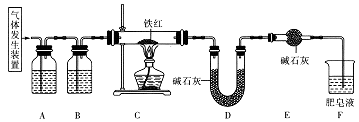
①装置A、B中的试剂依次是、。
②气体通入后,接下来的操作是 , 然后对C装置加热。
③实验前后称得D装置增重8.8g,则此铁红中铁的质量分数是。
【答案】
(1)3mol/LH2SO4,取少许溶液于试管中,加入足量铁粉,充分振荡;再加入足量3mol?L-1H2SO4,充分振荡.,试管中出现红色固体,说明试样中有CuO,取少许溶液于试管中,逐滴加入0.01mol?L-1酸性KMnO4溶液,紫红色褪去,5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O
(2)氢氧化钠溶液,浓硫酸,用点燃的小木条靠近肥皂泡,直到肥皂泡安静燃烧,72.41%
【解析】(1)氧化铜可以溶解于强酸溶液中,得到含有铜离子的盐,加入足量铁粉可以将金属铜置换出来,据此可以检验固体是氧化铜,氧化亚铁可以和强酸反应生成亚铁盐,能使高锰酸钾褪色,据此可以检验固体中含有氧化亚铁,
实验方案设计为:
实验操作 | 预期现象和结论 |
①加入足量的3molL-1H2SO4,充分振荡. | 样品全部溶解 |
②取少许溶液于试管中,加入足量铁粉,充分振荡;再加入足量3molL-1H2SO4,充分振荡. | 试管中出现红色固体,说明试样中有CuO |
③取少许溶液于试管中,逐滴加入0.01molL-1酸性KMnO4溶液 | 如果紫红色褪去,发生的离子反应方程式为5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O说明试样中有FeO; |
故答案为:①3mol/LH2SO4;②向一支试管中加入足量铁粉,充分振荡;再加入足量3mol/LH2SO4,充分振荡; 出现红色固体;③向另一支试管中加入0.01mol/L酸性KMnO4溶液;紫红色褪去;④5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O;
(2)①草酸分解生成的气体中含有二氧化碳和一氧化碳,C中发生一氧化碳与铁红的反应生成二氧化碳,D是吸收二氧化碳的装置,通过D装置的质量变化来测定的,因此需要除去加入C中气体中的二氧化碳,并干燥,装置A、B中的试剂依次是氢氧化钠溶液和浓硫酸,故答案为:氢氧化钠溶液;浓硫酸;
②一氧化碳具有可燃性,需要验纯,操作为用点燃的小木条靠近肥皂泡,直到肥皂泡安静燃烧,一氧化碳纯净后才能对C装置加热,故答案为:用点燃的小木条靠近肥皂泡,直到肥皂泡安静燃烧;
③实验前后称得D装置增重8.8g,表示生成的二氧化碳为8.8g,物质的量为 ![]() =0.2mol,说明样品中含有0.2molO元素,质量为0.2mol×16g/mol=3.2g,则此铁红中铁的质量分数是
=0.2mol,说明样品中含有0.2molO元素,质量为0.2mol×16g/mol=3.2g,则此铁红中铁的质量分数是 ![]() ×100%=72.41%,故答案为:72.41%。
×100%=72.41%,故答案为:72.41%。
(1)氧化铜可以溶解于强酸溶液中,得到含有铜离子的盐,加入足量铁粉可以将金属铜置换出来,据此可以检验固体是氧化铜,氧化亚铁可以和强酸反应生成亚铁盐,能使高锰酸钾褪色,据此可以检验固体中含有氧化亚铁;
(2)气体发生装置由草酸晶体受热分解CO2、CO、H2O,通过装置A中氢氧化钠溶液除去二氧化碳,通过装置B中浓硫酸除去水蒸气,得到干燥纯净的一氧化碳气体,通过装置C中的铁红发生氧化还原反应,生成的二氧化碳被装置D吸收,装置E是防止肥皂液则水蒸气进入;
①装置AB是对生成的气体进行除杂和干燥,除去二氧化碳用氢氧化钠溶液,除去水蒸气用浓硫酸;
②气体还原铁红样品需要检验气体的纯度,防止混有空气发生爆炸;
③实验前后称得D装置增重8.8g为生成二氧化碳的质量,其中一半来源于CO,一半来源于铁的氧化物,计算铁红中氧元素质量,结合元素守恒计算铁元素含量.


科目:高中化学 来源: 题型:
【题目】将下列各组物质按酸、碱、盐分类依次排列,正确的是( )
A. 硫酸、纯碱、小苏打
B. 磷酸、熟石灰、苛性钠
C. 硫酸氢钠、生石灰、醋酸钠
D. 硫酸、烧碱、胆矾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是( )
A.物质溶于水有吸热现象和放热现象
B.结晶水合物受热失去结晶水,发生了风化
C.潮解是指有些晶体吸收空气里的水蒸气,在晶体表面逐渐形成溶液的现象
D.化学反应都伴随能量的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如果25℃时,Kw=1.0×10﹣14 , 100℃下Kw=1.0×10﹣12 . 下列说法错误的是( )
A.100℃下水的电离程度较大
B.前者的C(H+)较后者小
C.水的电离过程是一个放热过程
D.温度越高,Kw越大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有五种短周期主族元素,它们在周期表中的位置如图所示,已知R元素的最高正化合价与最低负化合价的代数和为0。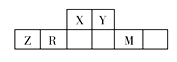
完成下列问题:
(1)Z元素在周期表中的位置是 , 同周期原子半径最大的元素是(填元素符号)。
(2)X的简单氢化物与M的单质,在一定条件下可以发生置换反应,化学方程式为 , 还原产物中含有的化学键类型有。
(3)我国发射“神舟”系列飞船的长征火箭,常以X、Y的液态氢化物做燃料。已知X、Y的两种氢化物电子数相等,并且反应时生成两种无毒、无污染的物质。
①写出两种氢化物反应的化学方程式 , 反应中氧化剂和还原剂的物质的量之比为。
②X的液态氢化物的电子式。
(4)下列说法能证明R、Y非金属性强弱的是____________。
A.R和Y的单质在一定条件下能生成RY2
B.Y单质常温下是气体,R单质是固体
C.Y的氢化物稳定性大于R的氢化物
D.自然界中存在Y单质不存在R单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于制备Fe(OH)3胶体的说法正确的是
A. 向NaOH溶液中滴加FeCl3饱和溶液
B. 向冷水中滴加饱和FeCl3溶液然后加热煮沸
C. 向加热煮沸的蒸馏水中逐滴加入少量饱和FeCl3溶液,继续加热至呈红褐色
D. 向饱和的FeCl3溶液中滴加少量的热水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.
某同学依据溴乙烷的性质,用右图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究.
实验操作Ⅰ:在试管中加入5mL 1mol/L NaOH溶液和5mL 溴乙烷,振荡.
实验操作II:将试管如图固定后,水浴加热.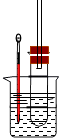
(1)用水浴加热而不直接用酒精灯加热的原因是 .
(2)观察到现象时,表明溴乙烷与NaOH溶液已完全反应.
(3)鉴定生成物中乙醇的结构,可用的波谱是 .
(4)为证明溴乙烷在NaOH乙醇溶液中发生的是消去反应,在你设计的实验方案中,需要检验的是 , 检验的方法是(需说明:所用的试剂、简单的实验操作及预测产生的实验现象).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com