
[2012���Ϸ��еڶ����ʼ�]��13�֣�ij��ѧ��ȤС��Լӵ�ʳ���е���ؽ����о����������ϵ�֪���������һ�ְ�ɫ��ĩ�������º��ȶ�,������5600C��ʼ�ֽ⡣�����������µ������һ�ֽ�ǿ����������������ᡢ����������������ã�����ԭΪ���ʵ⡣
��1��ѧ�������ʵ�����ӵ�ʳ���е�Ԫ�صĺ������������£�
a����ȡwg�ӵ��Σ�����������ˮ�ܽ⣻
b����ϡ�����ữ���ټ������KI��Һ��
c���Ե���Ϊָʾ���������ʵ���Ũ��Ϊ1.00��10��3mol/L��Na2S2O3��Һ�ζ����ζ�ʱ�ķ�Ӧ����ʽ����I2��2S2O32����2 I����2S4O62������
�ζ�ʱNa2S2O3��ҺӦ����_________ (���ʽ�ζ��ܡ���ʽ�ζ��ܡ������ζ����յ�ʱ����Na2S2O3��Һ20. 00mL�����յ���ɫ�仯Ϊ_________���ӵ�ʳ����Ʒ�еĵ�Ԫ�غ�����_________mg/kg(�Ժ�w�Ĵ���ʽ��ʾ����
��2��ѧ���ҶԴ�����NaCl(����KIO3)����������ʵ�飺
|
˳�� |
���� |
ʵ������ |
|
�� |
ȡ����������NaCl��������ˮ�ܽ� |
��Һ�ޱ仯 |
|
�� |
�������KI��Һ���� |
��Һ�ޱ仯 |
|
�� |
Ȼ���ٵμ�H2SO4���� |
��Һ����ɫ |
���Ʋ�ʵ����в�����ɫ����Ŀ���ԭ��__________________������ѧ���ҵ�ʵ���������ѧ����ʵ����������Ҫ����___________________________��
��3����ҵ��ͨ���õ��KI��Һ�ķ������Ʊ�����أ����������������ѧ�������ʵ�����жϵ���Ƿ���ȫ���������ޣ���ѡ���Լ���������Һ��H2O2��Һ��ϡ���ᡣ
|
ʵ����� |
ʵ�������� |
|
|
|
��13�֣���1����ʽ�ζ��� ��ɫ����ɫ���ұ��ְ���Ӳ���ɫ 
��2��I���������������ܱ��ܽ�����Һ�е�O2������I2 ��ͬѧ��ʵ��������ƫ��
��3��
|
ʵ����� |
ʵ�������� |
|
ȡ�����������Һ���Թ��У��ȵμӵ�����Һ���ٵμ�ϡ�����ữ |
����Һ�������ⲻ��ȫ��������������������ȫ�� |
����������1����S2O32��ˮ��Na2S2O3��Һ�ʼ��ԣ���Na2S2O3��ҺӦ���ڼ�ʽ�ζ��ܣ�����a��b�з����ķ�ӦΪ��5KI��KIO3��3H2SO4��3I2��3K2SO4��3H2O�����Դ�����Һ�к�I2���ӵ��ۺ������Һ����ɫ���ζ��յ�ʱI2��ȫ��S2O32����ԭΪI������Һ����ɫ��Ϊ��ɫ����5KI��KIO3��3H2SO4��3I2��3K2SO4��3H2O��I2��2S2O32����2 I����2S4O62���ɵã�n(KIO3) ��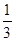 n(I2)��
n(I2)��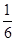 n(Na2S2O3)��
n(Na2S2O3)��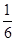 ��20.00��10��3L��1.00��10��3mol/L��
��20.00��10��3L��1.00��10��3mol/L��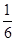 ��2.00��10��5mol�����Լӵ�ʳ����Ʒ�еĵ�Ԫ�غ���Ϊ
��2.00��10��5mol�����Լӵ�ʳ����Ʒ�еĵ�Ԫ�غ���Ϊ ��
�� ��
��
��2��ʵ����в�����ɫ�����ԭ���ǣ�I���������������ܱ��ܽ�����Һ�е�O2������I2������������һԭ���¼�ͬѧ��ʵ���д�����Һ��I2��Ũ��ƫ�Ӷ�ʹʵ����ƫ�ߡ�
��3�����ʵ�鷽��ʱ��Ҫ����I���������������ܱ��ܽ�����Һ�е�O2������I2��I2��������Һ��������ơ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2013���¿α���������¿����ģ���ѧ�Ծ���A�������������� ���ͣ�ʵ����
[2012���Ϸ��еڶ����ʼ�]��13�֣�ij��ѧ��ȤС��Լӵ�ʳ���е���ؽ����о����������ϵ�֪���������һ�ְ�ɫ��ĩ�������º��ȶ�,������5600C��ʼ�ֽ⡣�����������µ������һ�ֽ�ǿ����������������ᡢ����������������ã�����ԭΪ���ʵ⡣
��1��ѧ�������ʵ�����ӵ�ʳ���е�Ԫ�صĺ������������£�
a����ȡwg�ӵ��Σ�����������ˮ�ܽ⣻
b����ϡ�����ữ���ټ������KI��Һ��
c���Ե���Ϊָʾ���������ʵ���Ũ��Ϊ1.00��10��3mol/L��Na2S2O3��Һ�ζ����ζ�ʱ�ķ�Ӧ����ʽ����I2��2S2O32����2 I����2S4O62������
�ζ�ʱNa2S2O3��ҺӦ����_________ (���ʽ�ζ��ܡ���ʽ�ζ��ܡ������ζ����յ�ʱ����Na2S2O3��Һ20. 00mL�����յ���ɫ�仯Ϊ_________���ӵ�ʳ����Ʒ�еĵ�Ԫ�غ�����_________mg/kg(�Ժ�w�Ĵ���ʽ��ʾ����
��2��ѧ���ҶԴ�����NaCl(����KIO3)����������ʵ�飺
| ˳�� | ���� | ʵ������ |
| �� | ȡ����������NaCl��������ˮ�ܽ� | ��Һ�ޱ仯 |
| �� | �������KI��Һ���� | ��Һ�ޱ仯 |
| �� | Ȼ���ٵμ�H2SO4���� | ��Һ����ɫ |
| ʵ����� | ʵ�������� |
| | |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ���¿α���������¿����ģ���ѧ�Ծ���A�����������棩 ���ͣ�ѡ����
[2012�������еڶ����ʼ�]��ʵ���н�������ʵ�飬�����ڵ�ʵ����Ʒ�����õ����ǣ� ��
A�������ʵ��������Թܡ�����Ǧ��Һ����������Һ��
B����Һ��Fe3+�ļ��飨�Թܡ���ˮ��KSCN��Һ��
C���ⶨNa2CO3��NaHCO3�������Na2CO3�������������Թܡ��ƾ��ơ�������ƽ��
D����NaOH����Һ�ⶨδ֪Ũ�ȵ�������Һ��ʯ����Һ����ʽ�ζ��ܡ���ƿ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ���¿α���������¿���������ѧ�Ծ���B�����������棩 ���ͣ�ѡ����
[2012�����ŵڶ��ε���]�й��������жϻ��ʾ������ȷ���ǣ� ��
A���ɣ�H+(aq)��OH��(aq)�� H2O(l) ��H����57.3kJ/mol����֪����1mol CH3COOH����Һ�뺬1mol NaOH����Һ��ϣ��ų���������57.3 kJ
B����C��ʯī����C�����ʯ�� ��H����1.9kJ/mol����֪ʯī�Ƚ��ʯ���ȶ�
C�����������������������ֱ���ȫȼ�գ����߷ų���������
D��2gH2��ȫȼ������Һ̬ˮ�ų�285.8kJ������������ȼ�յ��Ȼ�ѧ����ʽΪ��2H2(g)��O2(g) �� 2 H2O(l) ��H����285.8kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013���¿α���������¿���������ѧ�Ծ���B�������������� ���ͣ���ѡ��
[2012�����ŵڶ��ε���]�й��������жϻ��ʾ������ȷ���ǣ� ��
| A���ɣ�H+(aq)��OH��(aq)��H2O(l)��H����57.3kJ/mol����֪����1mol CH3COOH����Һ�뺬1mol NaOH����Һ��ϣ��ų���������57.3 kJ |
| B����C��ʯī����C�����ʯ����H����1.9kJ/mol����֪ʯī�Ƚ��ʯ���ȶ� |
| C�����������������������ֱ���ȫȼ�գ����߷ų��������� |
| D��2gH2��ȫȼ������Һ̬ˮ�ų�285.8kJ������������ȼ�յ��Ȼ�ѧ����ʽΪ��2H2(g)��O2(g)��2 H2O(l)��H����285.8kJ/mol |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com