
分析 (1)将pH=11的氨水稀释100倍后,稀释后的溶液中氢氧根离子浓度大于原来的$\frac{1}{100}$;
(2)氨水是弱电解质存在电离平衡,向溶液中加入相同的离子能抑制氨水电离;
(3)根据物料守恒和电荷守恒来分析;
(4)①任何电解质溶液中都存在OH-、H+,如果溶液中只存在一种溶质,根据溶液中存在的离子知,溶质只能是氯化铵,NH4+水解导致其溶液呈酸性,但水解程度较小;
②若上述关系中④是正确的,c(OH-)>c(H+)则溶液呈碱性,氯化铵溶液呈酸性,要使混合溶液呈碱性,则溶液中溶质为一水合氨和氯化铵;
③该溶液中由体积相等的稀盐酸和氨水混合而成,溶液呈中性,根据电荷守恒分析.
解答 解:(1)一水合氨为弱电解质,存在电离平衡,稀释后一水合氨的电离程度增大,溶液中氢氧根离子的物质的量增大,所以将pH=11的氨水稀释100倍后,稀释后的溶液中氢氧根离子浓度大于原来的$\frac{1}{100}$,溶液的pH应该9-11之间,
故答案为:D;
(2)氯化铵溶于水电离出铵根离子,使氨水中的铵根离子浓度增大平衡向左移动,从而抑制氨水电离,故答案为:C;
(3)根据物料守恒知,C(NH4+)+C(NH3.H2O)=0.1mol,根据溶液中电荷守恒得C(Cl-)+c(OH-)=c(H+)+C(NH4+)+C(Na+),c(H+)+C(NH4+)-c(OH-)=C(Cl-)-C(Na+)=0.1mol-0.05mol=0.05mol,
故答案为:①NH4+、NH3.H2O;②NH4+、H+;
(4)①溶液中只存在OH-、H+、NH4+、Cl-四种离子,可能为NH4Cl溶液,因NH4+水解而显酸性,溶液中离子浓度大小顺序为c(Cl-)>c(NH4+)>c(H+)>c(OH-),故答案为:氯化铵;A;
②若上述关系中D是正确的,溶液呈碱性,且c(NH4+)>c(Cl-),应为NH3•H2O和NH4Cl的混合物,
故答案为:NH3•H2O和NH4Cl;
③溶液呈中性,据c(Cl-)+c(OH-)=c(NH4+)+c(H+)可得c(Cl-)=c(NH4+),因氨水为弱电解质,若该溶液中由体积相等的稀盐酸和氨水混合而成,则氨水浓度大于盐酸浓度,如小于或等于,则溶液呈酸性,
故答案为:<;=.
点评 本题综合考查盐类的水解、弱电解质的电离以及离子浓度的大小比较,为高频考点,侧重于学生的分析能力的考查,题目难度较大,注意把握盐类的水解以及弱电解质电离的特征,把握比较离子浓度大小顺序的方法.


科目:高中化学 来源: 题型:推断题
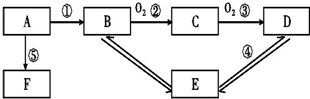
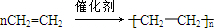 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4Cl和NaCl的固体混合物可用升华法分离 | |
| B. | 所有铵盐都易溶于水,所有铵盐中的氮均呈-3价 | |
| C. | 硝铵中不含铵根离子 | |
| D. | 铵态氮肥不能与碱性物质如草木灰混合施用 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
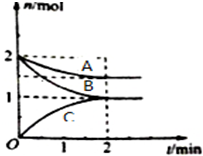 一定温度下,某容积为2L的密闭容器内,某一反应中A、B、C三种气体的物质的量随反应时间变化的曲线如图所示:
一定温度下,某容积为2L的密闭容器内,某一反应中A、B、C三种气体的物质的量随反应时间变化的曲线如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
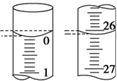 氧化还原滴定实验与酸碱中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之).现用0.1000mol•L-1KMnO4酸性溶液滴定未知浓度的无色H2C2O4溶液,按要求完成下列问题:
氧化还原滴定实验与酸碱中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之).现用0.1000mol•L-1KMnO4酸性溶液滴定未知浓度的无色H2C2O4溶液,按要求完成下列问题:| 滴定次数 | 待测H2C2O4溶液的体积/mL | 0.1000mol•L-1 KMnO4的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
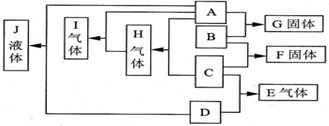
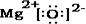 ,其化学键的类型为离子键.
,其化学键的类型为离子键.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
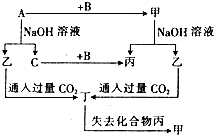 由短周期元素组成的单质A、B、C和四种化合物甲、乙、丙、丁有如图所示的转化关系,已知C是密度最小的气体,甲是电解质.根据图示转化关系回答问题:
由短周期元素组成的单质A、B、C和四种化合物甲、乙、丙、丁有如图所示的转化关系,已知C是密度最小的气体,甲是电解质.根据图示转化关系回答问题: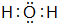 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com