
已知碳有三种常见的同位素:12C、13C、14C,氧也有三种同位素:16O、17O、18O,由这六种原子构成的二氧化碳分子最多有
A. 18种 B. 6种 C. 9种 D. 12种
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2017届河北省张家口市高三第一学期期末教学质量监测化学试卷(解析版) 题型:选择题
下列实验操作和现象所得结论正确的是
选项 | 操作 | 现象 | 结论 |
A | 向等物质的量浓度的NaNO3溶液和Na2SiO3溶液中分别滴加3滴酚酞溶液 | NaNO3溶液为无色,Na2SiO3溶液变成红色 | 非金属性:N>Si |
B | 将湿润的KI—淀粉试纸置于集满某气体的集气瓶口 | 试纸变蓝 | 该气体为Cl2 |
C | 将浓盐酸滴入NaHSO3溶液,所得气体依次通过浓硫酸和CuSO4,收集气体 | CuSO4颜色未发生改变 | 收集到纯净的SO2 |
D | 向含有少量FeCl3的FeCl2溶液中加入铜粉 | 铜粉有剩余 | 所得溶液中的溶质只有FeCl2 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省南昌市、洪都中学、麻丘中学、十七中、桑海中学高二3月联考化学试卷(解析版) 题型:选择题
下列各有机物的分类或命名正确的是 ( )
A.  2-甲基-3-丙基戊烷 B.
2-甲基-3-丙基戊烷 B. 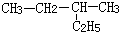 2-乙基丁烷
2-乙基丁烷
C. 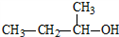 2-甲基-1-丙醇 D.
2-甲基-1-丙醇 D.  3-甲基-1-丁烯
3-甲基-1-丁烯
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省枣庄市北校区高一下学期第一次月考化学试卷(解析版) 题型:选择题
根据原子结构及元素周期律的知识,下列推断正确的是( )
A. 同主族元素含氧酸的酸性随核电荷数的增加而减弱
B. 核外电子排布相同的微粒化学性质也相同
C. Cl-、S2-、Ca2+、K+半径逐渐减小
D. 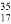 Cl 与
Cl 与 Cl 得电子能力相同
Cl 得电子能力相同
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省枣庄市北校区高一下学期第一次月考化学试卷(解析版) 题型:选择题
下列说 法正确的是
法正确的是
A.SiH4比CH4稳定
B.O2-半径比F-的小
C.Na和Cs属于第IA族元素,Cs失电子能力比Na强
D.P和As属于第VA族元素,H3PO4酸性比H3AsO4弱
查看答案和解析>>
科目:高中化学 来源:2017届安徽省安庆市高三第二次模拟考试理科综合化学试卷(解析版) 题型:简答题
钨是熔点最高的金属,是重要的战略物资,广泛用于钢铁工业,电真空照明材料等方面。黑钨矿是一种有开采价值的钨矿石,其主要成分是铁和锰的钨酸盐(常用FeWO4、MnWO4表示)。它的传统冶炼工艺的第一阶段如下图所示:

注:①上述流程中钨的化合价不变 ②钨酸(H2WO4)是一种难溶性酸
(1)写出C的化学式:______;写出生成B的化学方程式:_________
(2)上述流程中,第一次过滤所得滤渣的主要成份除MnO2外,还含有_________,请写出FeWO4在熔融条件下发生反应生成该成分的化学方程式_________
(3)冶炼金属钨是用非整比的钨氧化物为原料,钨元素在其中存在两种价态:+5价和+6价,试确定组成为WO2.7的氧化钨中两种对应价态的钨原子个数的整数比为_____________。
(4)黑钨矿还含少量Si、As的化合物,上述流程需优化(见下图)。向含Na2WO4的滤液中加硫酸调节pH=10后,再除杂净化。
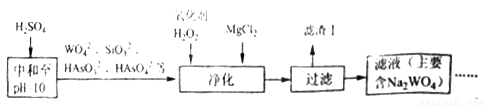
则“净化”过程中,加入H2O2的目的是__________,滤渣Ⅰ的主要成分是____________。
(5)某温度下,Ca(OH)2、CaWO4的相关数据见下表
项目 | CaWO4 | Ca(OH)2 |
-lgc(阴离子) | 4 | 2 |
-lgc(Ca2+) | 6 | 4 |
将钨酸钠溶液加入石灰乳中,发生反应的离子方程式为WO42-(aq)+Ca(OH)2(s)  CaWO4(s)+2OH-(aq)该温度下此反应的平衡常数为______mol/L。
CaWO4(s)+2OH-(aq)该温度下此反应的平衡常数为______mol/L。
查看答案和解析>>
科目:高中化学 来源:2017届安徽省安庆市高三第二次模拟考试理科综合化学试卷(解析版) 题型:选择题
下列关于有机化合物的说法不正确的是
A. 1,2-二甲苯也称邻二甲苯
B. 氨基乙酸与a-氨基丙酸的混合物一定条件下脱水能生成4种二肽
C. 苯与溴水不能发生加成反应,所以两者混合后无明显现象
D. C5H10O2属于羧酸的同分异构体有4种
查看答案和解析>>
科目:高中化学 来源:2016届湖南省高三2月模拟理科综合化学试卷(解析版) 题型:简答题
硫代硫酸钠(Na2S2O3)商品名“海波”,俗名“大苏打”,分析化学上常用于 滴定实验。某化学兴趣小组在实验室制备硫代硫酸钠晶体并探究其化学性质。
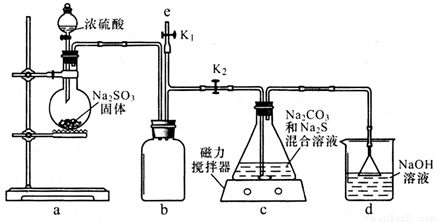
I.制备 Na2S2O3
(1)如图,关闭K1打开K2, 反应开始后,装置c中的产物除 了 Na2S2O3外还有一种无色无味 的气体,这种气体是______。
(2)装置c中反应结束后, 先关闭分液漏斗旋塞,在e处连 接盛NaOH溶液的注射器,再关闭K2打开K1 ,其目的是_______________。待c中溶液冷却后,倒入蒸发皿,通过加热蒸发、冷却结晶和干燥等操作获得Na2S2O3 CH2O晶体。
(3)实验结束后,装置d中的溶质可能有__________________。
探究Na2S2O3的部分化学性质
【分析推理】Na2S2O3可以看成是一个S原子取代了 Na2SO4中一个O原子形成的。据此 推测,下列说法正确的是____________。
A.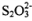 和
和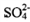 都是正四面体结构 B.
都是正四面体结构 B.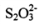 中硫硫键的键长大于硫氧键
中硫硫键的键长大于硫氧键
C.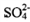 中的键角均为
中的键角均为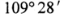 D.
D.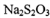 中所有原子都满足8电子结构
中所有原子都满足8电子结构
【提出假设】①Na2S2O3与Na2SO4结构相似,化学性质也应该相似,因此室温时Na2S2O3 溶液pH=7。②从S元素的化合价推测Na2S2O3具有较强的还原性。
【验证假设】配制适量Na2S2O3溶液,进行如下实验(请填空):
实验操作 | 实验现象 | 现象解释(用离子方程式表示) | |
① | ___________________ | 溶液pH=8 | ___________ |
② | 向新制氯水中滴入适量Na2S2O3溶液 | 氯水褪色 | _____________ |
【实验结论】__________________
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省枣庄市南校区高一3月月考化学试卷(解析版) 题型:选择题
下表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是

A. 常压下五种元素的单质中,Z单质的沸点最高
B. Y、Z的阴离子电子层结构都与R原子的相同
C. W的氢化物的沸点比X的氢化物的沸点高
D. Y元素的非金属性比W元素的非金属性强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com