
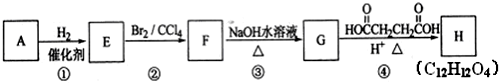
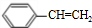 +Br2→
+Br2→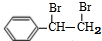
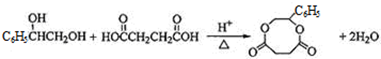
分析 A是芳香烃,令A的分子式为CxHy,1mol A完全燃烧消耗9.5molO2,则x+$\frac{y}{4}$=9.5,由转化关系可知A与氢气发生加成反应生成E,E与溴发生取代反应生成F,F发生取代反应生成G,G中含有2个醇-OH,G与发生酯化反应生成H,由H的分子式可知,A中含有8个C原子,则y=6,故A的分子式为C8H6,则A为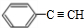 ,A与等物质的量的H2反应生成E为
,A与等物质的量的H2反应生成E为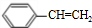 ,F为
,F为 ,G为
,G为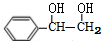 ,G与HOOCHCH2CH2COOH脱去2分子水生成环酯H为
,G与HOOCHCH2CH2COOH脱去2分子水生成环酯H为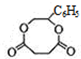 ,据此解答.
,据此解答.
解答 解:A是芳香烃,令A的分子式为CxHy,1mol A完全燃烧消耗9.5molO2,则x+$\frac{y}{4}$=9.5,由转化关系可知A与氢气发生加成反应生成E,E与溴发生取代反应生成F,F发生取代反应生成G,G中含有2个醇-OH,G与发生酯化反应生成H,由H的分子式可知,A中含有8个C原子,则y=6,故A的分子式为C8H6,则A为 ,A与等物质的量的H2反应生成E为
,A与等物质的量的H2反应生成E为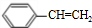 ,F为
,F为 ,G为
,G为 ,G与HOOCHCH2CH2COOH脱去2分子水生成环酯H为
,G与HOOCHCH2CH2COOH脱去2分子水生成环酯H为 .
.
(1)由上述分析可知,A的结构简式是 ,名称是苯乙炔,
,名称是苯乙炔,
故答案为:苯乙炔;
(2)由E转化为F的化学方程式是: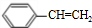 +Br2→
+Br2→ ,
,
故答案为: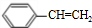 +Br2→
+Br2→ ;
;
(3)由G转化为H的化学方程式是: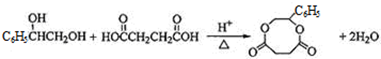 ,
,
故答案为: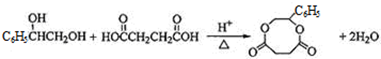 ;
;
(4)反应③卤代烃的水解反应,属于取代反应,
故答案为:取代反应;
(5)G( )的同分异构体有:①遇氯化铁溶液显紫色,说明含有酚羟基,②苯环上有三个取代基,③核磁共振氢谱显示苯环上有两种不同环境的氢原,应含有2个-OH、1个-CH2CH3,且3个取代基处于间位,或者3个取代基相邻,且-CH2CH3处于2个-OH之间,故符合条件的同分异构体共有2种,
)的同分异构体有:①遇氯化铁溶液显紫色,说明含有酚羟基,②苯环上有三个取代基,③核磁共振氢谱显示苯环上有两种不同环境的氢原,应含有2个-OH、1个-CH2CH3,且3个取代基处于间位,或者3个取代基相邻,且-CH2CH3处于2个-OH之间,故符合条件的同分异构体共有2种,
故答案为:2.
点评 本题考查有机物推断,综合分析确定A的结构简式,较好的考查学生分析推理能力,是对有机化合物知识的综合考查,需要学生熟练掌握官能团的性质与转化,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | SO2可用于杀菌、消毒,但不可用来加工食品 | |
| B. | 液氨汽化时要吸收大量热,因此氨常用作制冷剂 | |
| C. | PM2.5是指大气中直径小于或等于2.5微米的细小可吸入颗粒物,其分散在空气中能形成气溶胶 | |
| D. | 铝箔在酒精灯上加热铝熔化但不滴落,说明氧化铝的熔点高于铝的熔点 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当a≥2b时,发生的离子反应为:2OH-+CO2═CO32-+H2O | |
| B. | 当a≤b时,发生的离子反应为:OH-+CO2═HCO3- | |
| C. | 当2a=3b时,发生的离子反应为:3OH-+2CO2═CO32-+HCO3-+H2O | |
| D. | 当$\frac{a}{2}$<b<a时,溶液中HCO3-与CO32-的物质的量之比为(a-b):(2b-a) |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
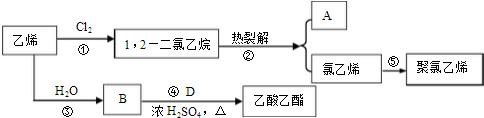
 ,D中官能团的名称为羧基.
,D中官能团的名称为羧基.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{m(A-N)}{A}$ mol | B. | $\frac{m(A-N-2)}{A}$ mol | C. | $\frac{(A-N+2)}{Am}$ mol | D. | $\frac{m(A-N+2)}{A}$ mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
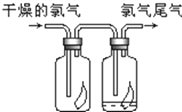 (1)瑞典化学家舍勒将软锰矿(主要成分MnO2)与浓盐酸混合加热,在世界上首先制得了氯气.写出该反应的离子方程式,并用双线桥画出电子转移的方向和数目.
(1)瑞典化学家舍勒将软锰矿(主要成分MnO2)与浓盐酸混合加热,在世界上首先制得了氯气.写出该反应的离子方程式,并用双线桥画出电子转移的方向和数目.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
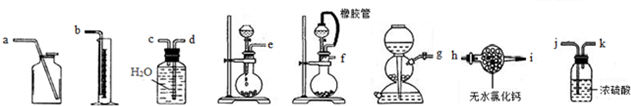
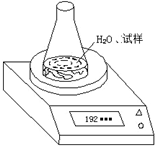
| 锥形瓶+水+试样 | |||||
| 读数次数 | 第一次 | 第二次 | 第三次 | 第四次 | 第五次 |
| 质量/g | 192.80 | 192.30 | 192.10 | 192.00 | 192.00 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com